БИЛЕТ № 34. Алюминий. Свойства. Применение. Получение
Алюминий легкий серебристо-белый металл. В чистом виде алюминий мягок, обладает высокой пластичностью, хорошо отливается, прокатывается, температура плавления составляет 657 °С. Уникальность алюминия заключается в совокупности ценных свойств: легкость (плотность 2,7 г/см3), высокая электропроводность, повышенная коррозионная стойкость и др. Он не реагирует с водой, концентрированной азотной кислотой, в которой происходит упрочнение оксидной пленки (пассивирование), поэтому для хранения и транспортировки той кислоты используются емкости и цистерны из алюминия. Алюминий разрушается щелочами, соляной и серной кислотами.
Широко применяют алюминиевые покрытия, которые различными способами наносят на стальные изделия для повышения их коррозионной стойкости.
Одним из ценных свойств алюминия является его высокая электропроводность, равная 60 % проводимости чистой меди, и так как алюминий в три с лишним раза легче меди, то алюминиевые шины и провода в два раза легче медных при одинаковой электропроводности. В электротехнике используется около 10 % получаемого алюминия.
Широкое применение алюминий получил в химической промышленности для изготовления различных емкостей и аппаратуры для хранения и производства жиров, спиртов и других веществ, в пищевой промышленности (алюминий нетоксичен) - для изготовления аппаратуры, посуды, фольги. В строительстве чистый алюминий как конструкционный материал используется мало ввиду невысокой прочности. В этих целях применяют сплавы алюминия.
Производство алюминия
Из многочисленных минералов, содержащих алюминий, исходным сырьем являются бокситы, нефелины, алуниты, каолины.
Бокситы содержат в основном 50-60 % А12О3, 10-30 % Н2О, 1-15 % SiО2, 2-25 % Fe2О3, 2-4 % TiО2. Нефелин отвечает формуле 3Na2O·K2O·Al2О3·9SiО2. Богатейшие запасы нефелина в нашей стране имеются на Кольском полуострове в виде апатито-нефелиновых пород. Алунитам отвечает формула K2SО4·A12(SО4)3·4A1(ОH)3; залегают в России, США, Италии, Австралии, Корее. Каолины содержат до 40 % А12О3.
Глинозем получают несколькими способами, выбор которого определяется составом природного сырья, содержащего алюминий.
Наиболее распространенный мокрый щелочной способ (Байера) применяется для переработки высокосортных бокситов с низким содержанием кремнезема (до 5-6 %). По способу Байера боксит выщелачивают в концентрированным раствором гидроксида натрия в автоклавах (стальных герметичных сосудах) при температуре 250 °С и давлении 2500-3000 кПа. При этом алюминий переходит в раствор в виде алюмината натрия (NaA1О2). Далее алюминатные растворы в специальных аппаратах с мешалкой разбавляют воюй, при этом вводят небольшое количество А1(ОН)3, играющего роль затравки (центров кристаллизации). В результате процесса гидролиза образуется гидроксид алюминия, который после промывки фильтруют и обжигают до полного обезвоживания:
2А1(ОН)3 →А12О3 + ЗН2О.
По второму способу (способ Яковкина) высококремнистую измельченную руду (нефелин или боксит с повышенным содержанием кремнезема) смешивают с содой и известняком и спекают во вращающихся печах при температуре 1250-1300 °С. В результате получаются окатыши, содержащие метаалюминат натрия, а также не растворимые в воде двухклльциевый силикат 2CaO·SiО2, метаферрит натрия Na2O·Fe2О3 и другие соединения.
Далее спек выщелачивают содовым раствором, переводя алюминат натрия в раствор, и разлагают алюминат газообразным СО2:
2NaA1О2 + СО2 + ЗН2О → 2А1(ОН)3 + Na2CО3
Полученный А1(ОН)3 отделяют от раствора и прокаливают при температуре 1200 °С. При переработке нефелина наряду с глиноземом получают Na2CО3, K2CО3 и цемент. Полученный глинозем А12О3 для получения алюминия подвергают электролизу. Алюминий, так же как натрий, калий и другие щелочные и шелочно-земельные металлы, имеющие наиболее электроотрицательные электродные потенциалы, может быть получен только электролизом расплавленных соединений. Однако глинозем имеет очень высокую температуру плавления 2050 °С, т.е. близкую к температуре кипения алюминия (2452 °С). Для снижения температуры, при которой ведут процесс электролиза (950 °С), глинозем растворяют в расплавленном криолите Na3[AlF6]. Криолит в природе встречается крайне редко (Гренландия), поэтому его получают искусственно.
Сырьем для получения криолита является плавиковый шпат CaF2, который нагревают во вращающихся печах с серной кислотой, получая при этом сульфат кальция и фтористый водород:
CaF2 + H2SО4 → CaSО4 + 2HF
Затем в очищенную плавиковую кислоту вводят гидроксид алюминия в количестве, необходимом для протекания реакции:
12HF + 2А1(ОН)3 → 2H3A1F6 + 6H2О
Полученную H3A1F6 нейтрализуют содой с получением криолита:
2H3A1F6 + 3Na2CО3 → 2Na3[AlF6] + 3H2О + 3CО2
Электролиз глинозема ведут в ваннах очень сложной конструкции (электролизеры), в которых катодом служит подина ванны, а анодом - самообжигающиеся угольные блоки, погруженные в расплавленный электролит.
На рисункепредставлена схема одной из существующих конструкций электролизной ванны, которая состоит из стального кожуха, выложенного изнутри шамотным кирпичом. Подина и стены ванны составлены из углеродистых блоков, к которым подведены катодные шины. Собственно катодом и является поверхность жидкого алюминия. Самообжигающиеся угольные аноды по мере сгорания опускаются и наращиваются сверху за счет размягченной угольной массы.
Упрощенно, как один из вариантов процессов, протекающих на электродах при электролизе, можно представить следующую схему. В расплавленном электролите происходит диссоциация криолита и глинозема:
Na3[AlF6] = 3Na+ + AlF63-
А12О3 = А13+ + АlO33-
На катоде при электролизе восстанавливаются ионы А13+ с образованием металлического алюминия:
А13+ + Зе = А1.
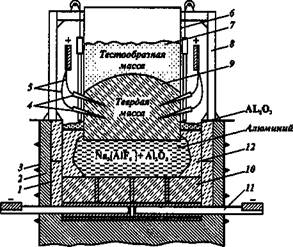 Рис. Схема электролизера с самообжигающимися анодами:
Рис. Схема электролизера с самообжигающимися анодами:
1 - угольные плиты; 2 - огнеупорный кирпич; 3 - кожух; 4 - стальные штыри;
5 - токоподводящие шины; 6 - алюминиевая рама анода; 7 - анод; 8 - рама;
9 - анодная масса; 10 - угольные блоки; 11 - катодный токоподвод; 12 – гарниссаж.
Температуру электролита поддерживают 940-960 °С. В этих условия поверхность электролита всегда покрывается коркой А12О3. Подобный же слой из застывшего электролита образуется на боковой поверхности футеровки ванны (гарниссаж). Такой гарниссаж предохраняет футеровочные материалы от разрушающего действия расплавленного электролита, утепляет ванну и предупреждает утечку тока через угольную футеровку.
Алюминиевая промышленность существует более 100 лет. Однако дo сих пор не создана научно обоснованная единая теория электролиза криoлито-глиноземных расплавов вследствие сложности как состава электролита, так и протекающих на электродах процессов.
На аноде в результате процесса окисления образуется газообразный кислород:
4АlO33- - 12 e = 2А12О3 + 3О2
который вызывает постепенное сгорание угольных анодов. Жидкий алюминий, который накапливается на дне ванны, периодически (каждые 1 - 2 суток) отбирают сифоном или вакуум-ковшом. Чистота электролитического алюминия составляет 98,5-99,8 %. Сырой металл сначала переплавляют, а затем подвергают электролитическому рафинированию, при этом достигается чистота алюминия 99,9 %. Особо чистый алюминий, используемый в электронной технике, получают зонной плавкой.
