III. Взаимодействие с азотистой кислотой
Химические свойства аминов
Амины, являясь производными аммиака, имеют сходное с ним строение и проявляют подобные ему свойства.
Модели молекул
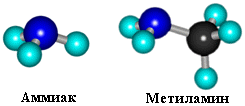
Как в аммиаке, так и в аминах атом азота имеет неподеленную пару электронов:
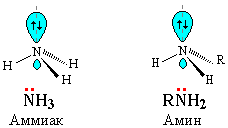
Поэтому амины подобно аммиаку проявляют свойства оснований.
I. Свойства аминов как оснований (акцепторов протонов)
1. Водные растворы алифатических аминов проявляют щелочную реакцию, т.к. при их взаимодействии с водой образуются гидроксиды алкиламмония, аналогичные гидроксиду аммония:
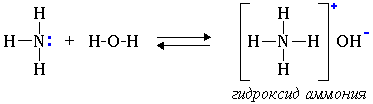
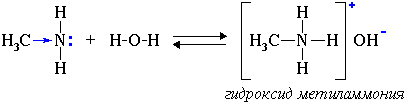
Связь протона с амином, как и с аммиаком, образуется по донорно-акцепторному механизму за счет неподеленной электронной пары атома азота.
Алифатические амины – более сильные основания, чем аммиак, т.к. алкильные радикалы увеличивают электронную плотность на атоме азота за счет +I-эффекта. По этой причине электронная пара атома азота удерживается менее прочно и легче взаимодействует с протоном.
2. Взаимодействуя с кислотами, амины образуют соли:
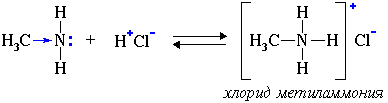
Соли аминов – твердые вещества, хорошо растворимые в воде. При нагревании щелочи вытесняют из них амины:
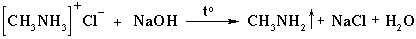
Ароматические амины являются более слабыми основаниями, чем аммиак, поскольку неподеленная электронная пара атома азота смещается в сторону бензольного кольца, вступая в сопряжение с его p-электронами.
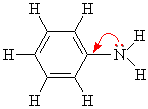 или
или 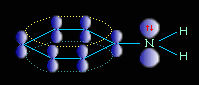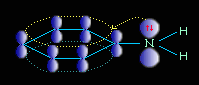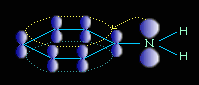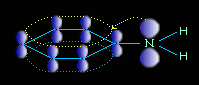
Уменьшение электронной плотности на атоме азота приводит к снижению способности отщеплять протоны от слабых кислот. Поэтому анилин взаимодействует лишь с сильными кислотами (HCl, H2SO4), а его водный раствор не окрашивает лакмус в синий цвет.
Таким образом, основные свойства изменяются в ряду:
C6H5NH2 < NH3 < RNH2 < R2NH < R3N (в газовой фазе)
II. Окисление аминов
Амины, особенно ароматические, легко окисляются на воздухе. В отличие от аммиака, они способны воспламеняться от открытого пламени.
4СH3NH2 + 9O2 ® 4CO2 + 10H2O + 2N2
III. Взаимодействие с азотистой кислотой
Азотистая кислота HNO2 – неустойчивое соединение. Поэтому она используется только в момент выделения. Образуется HNO2, как все слабые кислоты, действием на ее соль (нитрит) сильной кислотой:
KNO2 + HCl ® НNO2 + KCl
или NO2- + H+ ® НNO2
Строение продуктов реакции с азотистой кислотой зависит от характера амина. Поэтому данная реакция используется для различения первичных, вторичных и третичных аминов.
- Первичные алифатические амины c HNO2 образуют спирты:
R-NH2 + HNO2 ® R-OH + N2 + H2O
- Первичные ароматические амины при повышенной температуре реагируют аналогично, образуя фенолы. При низкой температуре (около 0° С) реакция идет иначе (см. ниже, раздел 2.4).
- Вторичные амины (алифатические и ароматические) под действием HNO2 превращаются в нитрозосоединения (вещества с характерным запахом):
R2NH + H-O-N=O ® R2N-N=O + H2O
алкилнитрозамин
- Реакция с третичными аминами приводит к образованию неустойчивых солей и не имеет практического значения.
