Распространенные элементы. строение атомов. Электронные оболочки. Орбитали
Лидин Р.А.
Химия.
Полный справочник для подготовки к ЕГЭ

Содержание
Предисловие
Распространенные элементы. строение атомов. Электронные оболочки. Орбитали
Периодический закон. Периодическая система. Электроотрицательность. Степени окисления
Молекулы. Химическая связь. Строение веществ
Классификация и взаимосвязь неорганических веществ
5. Металлы главных подгрупп I–III групп
5.1. Натрий
5.2. Калий
5.3. Кальций
5.4. Жёсткость воды
5.5. Алюминий
Переходные металлы 4-го периода. Свойства, способы получения. Общие свойства металлов
6.1. Хром
6.2. Марганец
6.3. Железо
6.4. Общие свойства металлов. Коррозия
7. Неметаллы главных подгрупп IV–VII групп
7.1. Водород
7.2. Галогены
7.2.1. Хлор. Хлороводород
7.2.2. Хлориды
7.2.3. Гипохлориты. Хлораты
7.2.4. Бромиды. Иодиды
7.3. Халькогены
7.3.1. Кислород
7.3.2. Сера. Сероводород. Сульфиды
7.3.3. Диоксид серы. Сульфиты
7.3.4. Серная кислота. Сульфаты
7.4. Неметаллы VA-группы
7.4.1. Азот. Аммиак
7.4.2. Оксиды азота. Азотная кислота
7.4.3. Нитриты. Нитраты
7.4.4. Фосфор
7.5. Неметаллы IVA-группы
7.5.1. Углерод в свободном виде
7.5.2. Оксиды углерода
7.5.3. Карбонаты
7.5.4. Кремний
Теория строения, многообразие, классификация и номенклатура органических соединений. Типы химических реакций
Углеводороды. Гомология и изомерия. Химические свойства и способы получения
9.1. Алканы. Циклоалканы
9.2. Алкены. Алкадиены
9.3. Алкины
9.4. Арены
Кислородсодержащие органические соединения
10.1. Спирты. Простые эфиры. Фенолы
10.2. Альдегиды и кетоны
10.3. Карбоновые кислоты. Сложные эфиры. Жиры
10.4. Углеводы
Азотсодержащие органические соединения
11.1. Нитросоединения. Амины
11.2. Аминокислоты. Белки
Химические реакции. Скорость, энергетика и обратимость
12.1. Скорость реакций
12.2. Энергетика реакций
12.3. Обратимость реакций
Водные растворы. Растворимость и диссоциация веществ. Ионный обмен. Гидролиз солей
13.1. Растворимость веществ в воде
13.2. Электролитическая диссоциация
13.3. Диссоциация воды. Среда растворов
13.4. Реакции ионного обмена
13.5. Гидролиз солей
Окислительно-восстановительные реакции. Электролиз
14.1. Окислители и восстановители
14.2. Подбор коэффициентов методом электронного баланса
14.3. Ряд напряжений металлов
14.4. Электролиз расплава и раствора
Решение расчетных задач
15.1. Массовая доля растворенного вещества. Разбавление, концентрирование и смешивание растворов
15.2. Объемное отношение газов
15.3. Масса вещества (объем газа) по известному количеству другого реагента (продукта)
15.4. Тепловой эффект реакции
15.5. Масса (объем, количество вещества) продукта по реагенту в избытке или с примесями
15.6. Масса (объем, количество вещества) продукта по реагенту с известной массовой долей в растворе
15.7. Нахождение молекулярной формулы органического соединения
Ответы
Предисловие
Справочник включает весь теоретический материал школьного курса химии, необходимый для сдачи ЕГЭ, – итоговой аттестации учащихся. Этот материал распределен по 14 разделам, содержание которых соответствует темам, проверяемым на ЕГЭ, – четырем содержательным блокам: «Химический элемент», «Вещество», «Химическая реакция», «Познание и применение веществ и химических реакций». К каждому разделу даны тренировочные задания из частей А и В – с выбором ответа и кратким ответом. Раздел 15 полностью посвящен решению расчетных задач, включенных в экзаменационную часть С.
Тестовые задания составлены таким образом, что, отвечая на них, учащийся сможет более рационально повторить основные положения школьного курса химии.
В конце пособия приводятся ответы к тестам, которые помогут школьникам и абитуриентам проверить себя и восполнить имеющиеся пробелы.
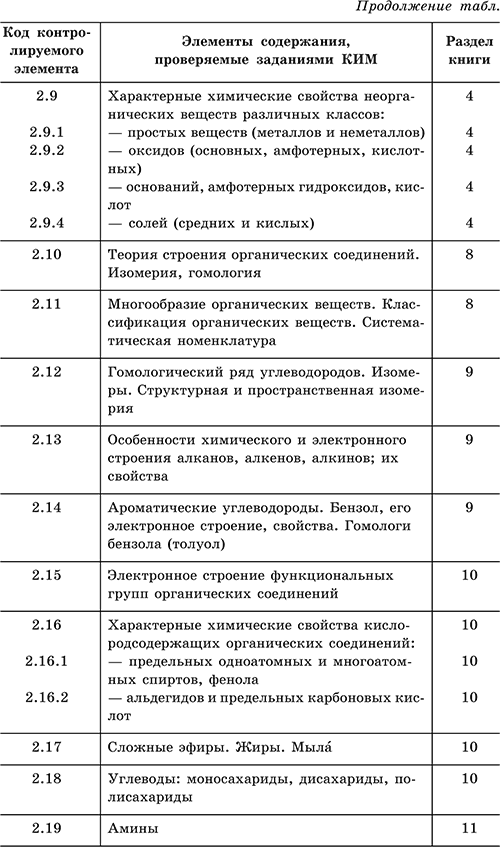
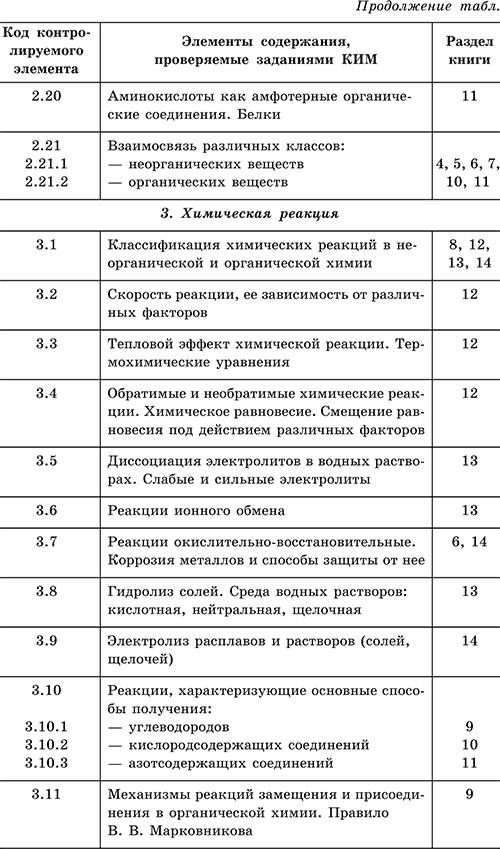
Для удобства работы с данным справочником приведена таблица, где указано соответствие между тематикой экзамена и разделами книги.
Пособие адресовано старшим школьникам, абитуриентам и учителям.





Распространенные элементы. строение атомов. Электронные оболочки. Орбитали
Химический элемент– определенный вид атомов, обозначаемый названием и символом и характеризуемый порядковым номером и относительной атомной массой.
В табл. 1 перечислены распространенные химические элементы, приведены символы, которыми они обозначаются (в скобках – произношение), порядковые номера, относительные атомные массы, характерные степени окисления.
Нулевая степень окисления элемента в его простом веществе (веществах) в таблице не указана.
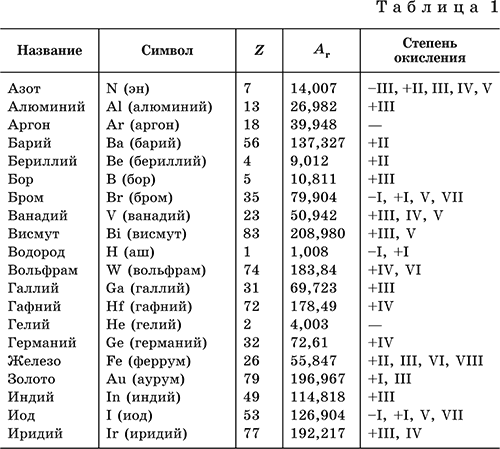
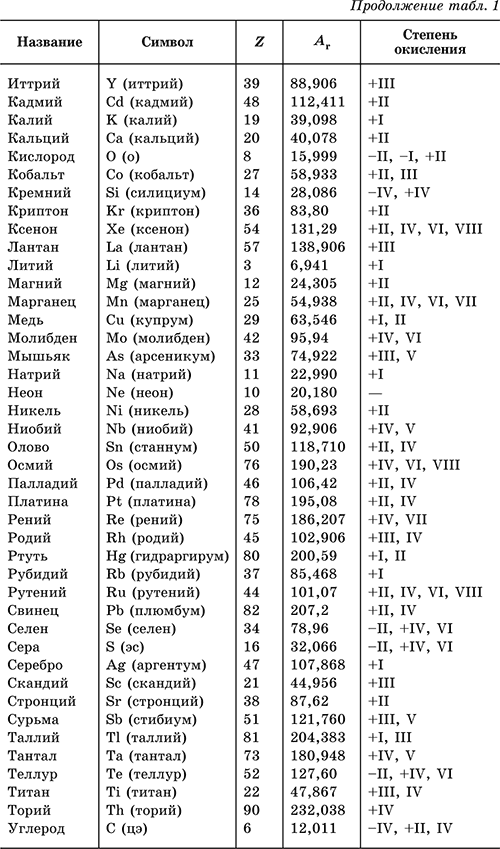
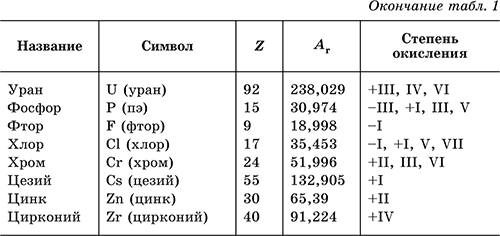
Все атомы одного элемента имеют одно и то же число протонов в ядре и число электронов в оболочке. Так, в атоме элемента водород Н находится 1р+ в ядре и на периферии 1е‑; в атоме элемента кислород О находится 8р+ в ядре и 8е‑ в оболочке; атом элемента алюминий Аl содержит 13р+ в ядре и 13е‑ в оболочке.
Атомы одного элемента могут различаться числом нейтронов в ядре, такие атомы называются изотопами. Так, у элемента водород Н три изотопа: водород‑1 (специальное название и символ протий 1H) с 1 р+ в ядре и 1е‑ в оболочке; водород‑2 (дейтерий 2Н, или D) с 1р+ и 1п0 в ядре и 1е‑ в оболочке; водород‑3 (тритий 3Н, или Т) с 1р+ и 2п0 в ядре и 1е‑ в оболочке. В символах 1Н, 2Н и 3Н верхний индекс указывает массовое число– сумму чисел протонов и нейтронов в ядре. Другие примеры:
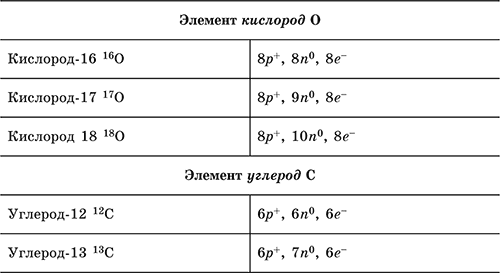
Электронную формулу атома любого химического элемента в соответствии с его расположением в Периодической системе элементов Д. И. Менделеева можно определить по табл. 2.

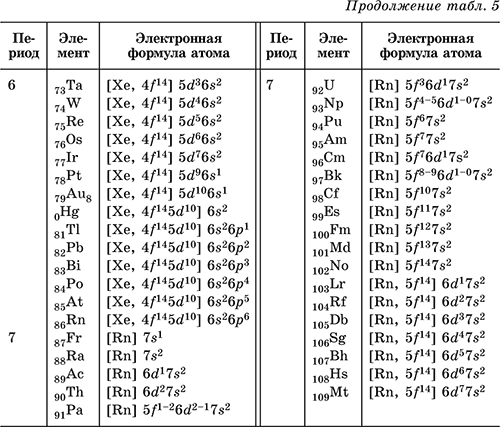
Электронная оболочка любого атома делится на энергетические уровни (1, 2, 3‑й и т. д.), уровни делятся на подуровни (обозначаются буквами s, р, d, f). Подуровни состоят из атомных орбиталей – областей пространства, где вероятно пребывание электронов. Орбитали обозначаются как 1s (орбиталь 1‑го уровня s‑подуровня), 2s, 2р, 3s, 3р, 3d, 4s… Число орбиталей в подуровнях:

Заполнение атомных орбиталей электронами происходит в соответствии с тремя условиями:
1) принцип минимума энергии
