Перекисное окисление липидов
Действие на липидный бислой
– Увеличение вязкости
– Рост поверхностного заряда
– Увеличение проницаемости для ионов
– Снижение электрической прочности

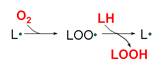
LH+O2=LOOH
№39. Антиоксиданты и ингибиторы радикальных окислительных процессов:
А). Ферментативные антиоксиданты (супероксиддисмутаза, каталаза, глутатионзависимые ферменты
Б). Соединения, содержащие енольные группы: фенольные антиоксиданты, аскорбиновая кислота, SH-содержащие соединения.
В).Хелаторы ионов металлов переменной валентности
Г). Гуморальные антиоксидантные факторы: церулоплазмин и трансферрин
Антиоксиданты-вещ-ва, препятствующие образованию свободных радикалов.
А). Ферментативные:
1.Супероксиддиссмутаза
Локализац:цитозоль клеток, много в печени, лёгких, эритроцитах, митхондриях эукариотических клеток
Катализирует дисмутацию супероксида в кислород и пероксид водорода.
O2− + O2−+ 2H+ àH2О2+О2
2. Каталаза разлагает образующуюся в процессе биологического окисления перекись водорода на воду и молекулярный кислород (2H2O2 → 2H2O + O2), а также окисляет в присутствии перекиси водорода низкомолекулярные спирты и нитриты. Содержится почти во всех организмах. Участвует в тканевом дыхании.
3. Глутатионпероксидаза-инактивирует гидроперекиси липидов, катализируют восстановление перекисей липидов в соответствующие спирты и восстановление пероксида водорода до воды
Локализац: в эритроцитах: для того, чтобы регенерировать фермент требуется NADPH2(продукт оксиления глюкозы), в составе селена
S-CHО2(гидроперекись)+Глу-SHà2H2О+Глу-Глу
Б). фенольные антиоксиданты, витамины
Витамины-осуществляют обрыв цепной реакции за счёт захвата электрона и превращ. в стабильн. Св-R частицу
1.ВитЕ(токоферол)-связывает жирорастворимые св-R: ROO*+Е-OHà ROOH+ Е-О*
ROO*-имеет выс.активн., стрем-ся снова вступ. в реакц.
Е-О*(витЕ)-стабилен, малоактивен, тк. у него ароматичек структура. Он поступ-ет в печень, конъюгирует с глюкуроновой к-той и выводится с калом.
При выс.дозе Е-О* стан-ся прооксидантом
Локализац:встроен в мембр, в тканях, где выс.парциальн.p-эритроциты
2.бэта-каротин-в раст пище, перце, моркови
Локализ:в ткан.с низк, парц.p
Его недостаток приводит к разв. онкологич. заболев.
3. Вит C(аскорбинов)-связывает водорастворимые св-R
Организм человека усваивает только двухвалентное железо (Fe2+), в то время как трехвалентное не усваивается и приносит много вреда, инициируя реакции перекисного окисления липидов. Восстановление Fe3+ в Fe2+ осуществляется аскорбиновой кислотой.
4. Убихинон (коэнзим Q) - фенол, по химической структуре близок к токоферолам. Он содержится в митохондриях, где участвует в работе дыхательной цепи
В).Хелаторы ионов металлов переменной валентности- связывают ионы Ме в прочные комплексы, предотвращая их окисление(при отравлении Мg, Fe)
1. Унитол(зоракс)-используется при интоксикации(напр, если разбили ртуть)
Г). Гуморальные антиоксидантные факторы.
Гликопротеин крови-действ. в основном на предотвращение оксиления Fe2+ в Fe3+ путём его связывания.
Церулоплазмин(голуб цв) и трансферрин-гликозилированные белки которые прочно, но обратимо связывают ионы железа, переводя их из Fe2+ в Fe3+.
№40 Микросомальное окисление. Механизм действия цитохрома Р450. Роль цит Р450 в метаболизме ксенобиотиков.
Микросомальное окисление совокупность реакций первой фазы биотрансформации ксенобиотиков и эндогенных соединений,
катализирующихся ферментными системами мембран эндоплазматического ретикулума гепатоцитов при участии цитохрома Р-450. 2 цепи: монооксигеназная цепь окисления, источник протонов и электронов восстановленный НАДФ, а другая редуктазная цепь ок., в которой источником электронов служит восстановленный НАД.
Цтохром Р450 образует комплексы с СО., Р450 активирует кислород путем переноса на него электронов и использует актив. кислород для окислен. вещ. и образования воды, 1 атом О включается в окисляемое вещ., а другой связывает 2 Н+ из среды, входя в состав воды. Сначала поступающие в организм чужеродные соединения (канцерогены, лекарства, промышленныя яды и пр.) активируются с помощью ферментов семейства цитохромов Р450Ее основные функции заключаются в образовании в молекуле субстрата ксенобиотика гидрофильных групп, благодаря чему происходит детоксикация десятков тысяч веществ
№41 Механизм монооксигеназных реакций. Значение монооксигеназных реакций в пластическом обмене.
Механизм монооксигеназных реакций. Значение монооксигеназных реакций в пластическом обмене.
Монооксигеназный механизм реакций предусматривает включение одного атома О2 в окисляемый субстрат, а другого – в молекулу воды. Монооксигеназы сущ-ют или в виде растворимых ферментов, находящихся в клеточном соке, или в виде специальных цепей окисления, расположенных в мембранах ЭПС печеночных клеток, митохондрий клеток коры надпочечников и т.д. к растворимым монооксигеназам относятся медьсодержащие монооксигеназы, например дофамин-бета-монооксигеназа, тирозиназа. Монооксигеназные цепи окисления представляют собой короткие цепи переноса электронов и протонов.
Монооксигеназные цепи исп-ся для окисления природных органич.вещ-в в ходе синтеза желчных кислот, стероидных гормонов из холестерина, а также для обезвреживания лекарств и ядов.
№42 Биотрансформация лекарственных средств. Влияние лекарств на ферменты, участвующие в обезвреживании ксенобиотиков.
Лекарства, поступившие в организм, проходят следующие превращения: всасывание; связывание с белками и транспорт кровью; взаимодействие с рецепторами; распределение в тканях; метаболизм и выведение из организма.В результате биотрансформации лекарственных веществ может произойти: инактивация лекарственных веществ, т.е. снижение их фармакологической активности; повышение активности лекарственных веществ; образование токсических метаболитов.В первую фазу обезвреживания под действием монооксигеназ образуются реакционно-способные группы -ОН, -СООН, -NH2, -SH и др. Химические соединения, уже имеющие эти группы, сразу вступают во вторую фазу обезвреживания - реакции конъюгации.При патологии печени, сопровождающейся снижением активности микросомальных ферментов, продолжительность действия ряда лекарственных веществ увеличивается. Некоторые препараты снижают активность монооксигеназной системы. Например, левомицетин и бутадиен ингибируют ферменты микросомального окисления. Антихолинэстеразные средства, ингибиторы моноаминооксидазы, нарушают функционирование фазы
конъюгации, поэтому они пролонгируют эффекты препаратов, которые инактивируются этими ферментами. Кроме того, скорость каждой из реакций биотрансформации лекарственного вещества зависит от генетических, физиологических факторов и экологического состояния окружающей среды.
№43 Роль реакций коньюгации в осуществлении детоксицирующей функции печени
Продукты метаболизма чужеродных веществ, образовавшихся на первой стадии биотрансформации, подвергаются дальнейшей детоксикации с помощью ряда реакций второй стадии. Образующиеся при этом соединения менее полярны и в связи с этим легко удаляются из клеток. Преобладающим является процесс конъюгации, катализируемый глутатион-S-трансферазой, сульфотрансферазой и UDP-глюкуронилтрансферазой. Конъюгацию с глутатионом, приводящую к образованию меркаптуровых кислот, принято рассматривать в качестве основного механизма детоксикации.Восстановление окисленного глутатиона осуществляет фермент - глутатионредуктаза, используя как кофермент НАДФН. Коньюгаты с глутатионом, серной и глюкуроновой кислотами выводятся из организма преимущественно с мочой.
№44 Совместимость лекарственных препаратов и микросомальное окисление
Индукция ферментов приводит к увеличению синтеза Ц-450. В результате, ускоряется метаболизм лекарственных препаратов, что может привести к снижению или отсутствию их эффекта. Таким действием обладают, например, барбитураты и рифампицин, которые ускоряют как собственные метаболизм, так и метаболизм других лекарственных веществ. Ингибирующее влияние на ферменты биотрансформации приводит к замедлению метаболизма препаратов. В результате повышается их концентрация в плазме крови и увеличивается риск токсического действия. Подобным образом действуют такие препараты как флуконазол, эритромицин и тетурам.
№45 Особенность применения лекарственных средств при хроническом алкоголизме
При хроническом употреблении алкоголя происходит активация ферментов, обеспечивающих разрушение алкоголя в печени. При этом повышается активность других ферментов, осуществляющих превращение лекарств в организме и ускоряющих их распад. Это относится в первую очередь к снотворным, болеутоляющим, противодиабетическим средствам. Люди, постоянно употребляющие спиртные напитки, становятся невосприимчивы к действию наркозных и обезболивающих средств, что значительно усложняет проведение наркоза во время операций и снижает эффективность анестезии при стоматологических и других лечебных манипуляциях.
Регулярный прием спиртных напитков усиливает токсическое действие парацетамола на печень.Парацетамол не следует назначать больным, страдающим алкоголизмом! Одновременное употребление алкоголя и метронидазола, цефалоспориновых антибиотиков, хлорамфеникола, гризеофульвина, сульфаниламидных препаратов вызывает симптомы (головную боль, покраснение кожных покровов, тошноту или рвоту, головокружение).
Алкоголь усиливает действие антиагрегантов и антикоагулянтов (аспирин, дикумарин, синкумар, фенилин и др.), применяемых в лечении сосудистых заболеваний. В результате могут возникнуть обильные внутренние кровотечения. Если такое кровоизлияние произойдет в мозг (возможен инсульт), можно ожидать паралича конечностей, нарушение речи, дыхания, сердечно-сосудистой деятельности) вплоть до смертельного исхода.
