Качественные реакции катионов
Первая аналитическая группа (К+, Na+, NH 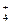 )
)
К первой аналитической группе катионов относятся ионы калия, натрия, а также ион аммония NH 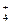 . Большинство образуемых ими солей хорошо растворимо в воде. Группового реагента, осаждающего все три катиона данной группы нет.
. Большинство образуемых ими солей хорошо растворимо в воде. Группового реагента, осаждающего все три катиона данной группы нет.
Реакции катиона К+
Реакции открытия катиона К+, основанные на образование осадков, очень немногочисленные. Важнейшие из них следующие.
1. Винная кислота Н2С4Н4О6 и ее кислота натриевая соль – гидротартрат натрия дают с растворами солей калия кристаллический осадок белого цвета
 KCl + NaHC4H4O6 =KHC4H4O6 + NaCl
KCl + NaHC4H4O6 =KHC4H4O6 + NaCl
K+ + HC4H4O 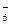 = KHC4H4O6 ↓
= KHC4H4O6 ↓
Выполнение опыта
В пробирку налейте 4-5 капель раствора соли калия и прибавьте столько же капель раствора гидротартрата натрия. Перемешайте содержимое пробирки стеклянной палочкой – выпадает белый кристаллический осадок.
Вывод:
2. Катион К+ пламя горелки окрашивает в бледно-фиолетовый цвет.
Реакции катиона Na+
Большинство солей натрия хорошо растворимо в воде. Поэтому реакции, основанные на образовании труднорастворимых осадков, для иона Na+ весьма немногочисленны.
Гексагидроксоантимонат калия, дает с растворами солей натрия белый кристаллический осадок гексагидроксоантимонат натрия.
 NaCl + K[Sb(OH)6] = Na[Sb(OH)6] + KCl
NaCl + K[Sb(OH)6] = Na[Sb(OH)6] + KCl
Na+ + [Sb(OH)6]- = Na[Sb(OH)6]
 Выполнение опыта
Выполнение опыта
В пробирку налейте 5-6 капель соли натрия и прибавьте такой же объем раствора гексагидроксоантимоната калия и потрите стенки пробирки стеклянной палочкой. Выпадает белый кристаллический осадок.
Реакции катиона NH 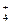
1. Едкие щелочи разлагают соли аммония, с выделением газообразного аммиака, который можно обнаружить по запаху.
NH4Cl + NaOH 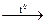 NaCl + NH3↑ + H2O
NaCl + NH3↑ + H2O
NH 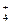 + OH-
+ OH- 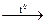 NH3↑ + H2O
NH3↑ + H2O
Выполнение опыта
Поместите 1-2 мм раствора соли аммония в пробирку, добавьте 2-3 мл растра щелочи и нагрейте до кипения, при этом выделяется газ с резким запахом. Аммиак можно обнаружить также и по посинению влажной красной лакмусовой бумажки, поднесенной к отверстию пробирки. Ни один из других катионов не дает аналогичной реакции.
Вывод:
Вторая аналитическая группа (Ag+, Pb2+, Hg 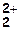 )
)
Реакции катиона Ag+
Хромат калия дает с катионом Ag+ осадок хромата серебра кирпично-красного цвета.
2AgNO3 + K2CrO4 = Ag2CrO4↓ + 2KNO3
2Ag+ + . . . . →
Выполнение опыта
В пробирку возьмите 2-3 капли раствора нитрата серебра, добавьте 3-4 капли дистиллированной воды и 1-2 капли хромата калия. Обратите внимание на цвет
Вывод:
Реакции катиона Pb2+
1. Хромат калия образует малорастворимый хромат свинца желтого цвета.
Pb(NO3)2 + K2CrO4 = PbCrO4↓ + 2KNO3
Pb2+ + . . . . . →
Выполнение опыта
В пробирку налейте 3-4 капли раствора нитрата синца и 2-3 капли раствора хромата калия.
2. Иодид калия образует и ионами свинца осадок желтого цвета.
Pb(NO3)2 + 2KI = PbI2 + 2KNO3
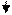
 Pb2+ + . . . . . →
Pb2+ + . . . . . →
Выполнение опыта
К 2-3 каплям раствора нитрата свинца, помещенным в пробирку, прилейте 3-5 капель раствора иодида калия.
Вывод:
Третья аналитическая группа катионов (Ba2+, Sr2+, Ca2+)
Реакции катиона Ва2+
Особо характерных реакций на катион Ва2+ указать трудно, но наиболее широко используют следующие.
1. Хромат калия и дихромат калия дают с катионам Ва2+ осадок хромата бария желтого цвета.
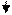
 BaCl2 + K2CrO4 = BaCrO4 + 2KCl
BaCl2 + K2CrO4 = BaCrO4 + 2KCl
Ba2+ + . . . →
.Выполнение опыта
В пробирку поместите 3 капли раствора хлорида (или нитрата) бария, добавьте каплю раствора хромата калия, перемешайте стеклянной палочкой. Полученный осадок испытайте на растворимость в соляной и уксусной кислотах.
Вывод:
2. Оксалат аммония (и другие растворимые соли щавелевой кислоты) образует с катионом Ва2+ белый кристаллический осадок
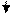
 BaCl2 + (NH4)2C2O4 = BaC2O4 + 2NH4Cl
BaCl2 + (NH4)2C2O4 = BaC2O4 + 2NH4Cl
Ba2+ + . . . . → . . .
Выполнение опыта
В пробирку налейте 3 капли раствора соли бария (хлорида или нитрата) и прилейте 3-4 капли раствора оксалата аммония. Полученный осадок разделите на 2 части и прилейте к одной части соляную кислоту, а к другой – уксусную. Что наблюдается?
Вывод:
3. Соли бария окрашивают бесцветное пламя в желто-зеленый цвет.
Реакции катиона Са2+
Для открытия катиона Са2+ используют общеаналитические реакции, из которых следует отметить реакцию с оксалатом аммония.
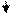
 CaCl2 + (NH4)2C2O4 = CaC2O4 + 2NH4Cl
CaCl2 + (NH4)2C2O4 = CaC2O4 + 2NH4Cl
Са2+ + . . . →
Выполнение опыта
В пробирку налейте 3 капли раствора хлорида кальция (или нитрата кальция), прибавьте 3-4 капли оксалата аммония. Полученный осадок испытайте на растворимость в соляной и уксусной кислотах.
Вывод:
Четвертая аналитическая группа катионов (Al3+, Zn2+, Cr3+, Sn2+)
Реакции катиона Cr3+
Хром образует два ряда устойчивых солей: соли хрома (III) и соли хромовой и двухромовой кислот. Растворы солей, содержащие катион Cr3+, имеют зеленую или фиолетовую окраску, растворы хроматов (CrO 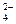 ) – желтую, растворы дихроматов – (Cr2O
) – желтую, растворы дихроматов – (Cr2O 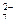 ) – оранжевую окраску.
) – оранжевую окраску.
Для ионов хрома характерны реакции окисления – восстановления Cr(III) 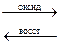 Cr(VI)
Cr(VI)
Реакции окисления Cr(III) в Cr(VI) можно проводить в щелочной и кислой средах
1. Окисление в щелочной среде чаще всего проводят пероксидом водорода (пероксидом натрия) или бромной (хлорной) водой.
Cr2(SO4)3 + 3H2O2 + 10NaOH = 2Na2CrO4 + 3Na2SO4 + 8H2O
 2 Cr3+ + 8OH- - 3ē → CrO
2 Cr3+ + 8OH- - 3ē → CrO 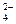 + 4H2O
+ 4H2O
3 H2O2 + 2ē → 2OH-
 2 Cr3+ + 16OH- + 3H2O2 = 2CrO
2 Cr3+ + 16OH- + 3H2O2 = 2CrO 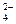 + 8H2O + 6OH-
+ 8H2O + 6OH-
2Cr3+ + 10OH- + 3H2O2 = 2CrO 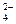 +8H2O
+8H2O
Выполнение опыта
К 2-3 каплям раствора соли хрома (III), помещенным в пробирку, приливайте по каплям раствор NаOH до растворения образовавшегося осадка, затем добавьте 2-3 капли Н2О2 и нагрейте. Обратите внимание на измене цвета растворов.
Вывод:
