Тема 2.5. теоретические основы и классификация физико-химических методов анализа
Изучение данной темы по рекомендуемой литературе.
РЕКОМЕНДУЕМАЯ ЛИТЕРАТУРА
Основная литература:
1.Ахметов, Н.С. Общая и неорганическая химия: учебник /Н.С. Ахметов. - М.: Высшая школа, 2005.
2. Хомченко, Г.П. Неорганическая химия: учебник для с.-х. вузов / Г.П. Хомченко, И.К. Цитович. – СПб.: ИТК Гранит: ООО ИПК «КОСТА», 2009. – 464 с.
3. Цитович, И.К. Курс аналитической химии: учебник / И.К. Цитович.- СПб.: Лань, 2007.
4. Саргаев, П.М. Неорганическая химия [Электронный ресурс]/ П.М. Саргаев.- СПб.: Лань, 2013.- Режим доступа: http://www.Lanbook.ru, свободный.
Дополнительная литература:
1. Глинка, Н.Л. Задачи и упражнения по общей химии: учебное пособие/ Н.Л. Глинка. - М.: КноРус, 2012.- 240 с.
2. Глинка, Н.Л. Общая химия: учебное пособие / Н.Л. Глинка.- М.: Юрайт, 2010. – 886 с.
3. Ершов, Ю.А. Общая химия. Биофизическая химия. Химия биогенных элементов: учебник / Ю.А. Ершов [и д.р.]- М.: Высшая школа, 2009.– 560 с.
4. Келина, Ю. Общая и неорганическая химия в таблицах и схемах: учебное пособие/ Ю. Келина, Н. В. Безручко.- М.: Феникс, 2008.
5. Князев, Д. А. Неорганическая химия: учебник/ Д. А. Князев, С. Н. Смарыгин.- М.: Юрайт, 2012. – 886 с.
Ресурсы интернета:
1. Открытый колледж http://www.college.ru/chemistry/index/php.
2. Рубрикон: энциклопедии, словари, справочники http://www.en.edu.ru/db/msg/7030/sp/3368/2794/2761/
3. Информационно-справочные и образовательные системы по химии http://www.chemnet.ru/,http://www.alhimik.ru/,http://www.chemport.ru/,http://www.chemworld.narod.ru/
ПриложениЕ
Приложение 1
Основные физические постоянные
| Постоянная | Обозначение | Значение |
| Число Авогардо | NA | 6,02 · 1023 моль-1 |
| Заряд электрона | e | 1,60 · 10-19 Кл |
| Молярный объем газа | Vm | 22,4 л/моль* |
| Постоянная Больцмана | k | 1,38 · 10-23 Дж/К |
| Постоянная Планка | h | 6,63 · 10-34 Дж·с |
| Постоянная Фарадея | F | 9,65 · 104 Кл/моль |
| Универсальная газовая постоянная | R | 8,31 Дж/(моль·К) |
* При нормальных условиях.
Приложение 2
Групповые названия химических элементов
| Актиноиды | Ac, Th, Pa, U, Np, Pu, Am, Cm, Bk, Cf, Es, Fm, Md, No, Lr |
| Благородные газы | He, Ne, Ar, Kr, Xe, Rn |
| Галогены | F, Cl, Br, I, At |
| Лантаноиды | La, Ce, Pr, Nd, Pm, Sm, Eu, Gd, Tb, Dy, Ho, Er, Tm, Yb, Lu |
| Халькогены | O, S, Se, Te, Po |
| Семейство железа | Fe, Co, Ni |
| Семейство платины | Ru, Rh, Pd, Os, Ir, Pt |
| Щелочные металлы | Li, Na, K, Rb, Cs, Fr |
| Щелочноземельные металлы | Ca, Sr, Ba, Ra |
Приложение 3
Множители и приставки для образования десятичных кратных и дольных единиц
| Множитель | Приставка | Обозначение | Множитель | Приставка | Обозначение | |
| 1012 | тера | Т | 10-1 | деци | д | |
| 109 | гига | Г | 10-2 | санти | с | |
| 106 | мега | М | 10-3 | милли | м | |
| 103 | кило | к | 10-6 | микро | мк | |
| 102 | гекто | г | 10-9 | нано | н | |
| 101 | дека | да | 10-10 | пико | п |
Приложение 4
Термодинамические константы некоторых веществ
| Вещество | 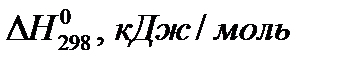 | 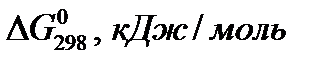 | 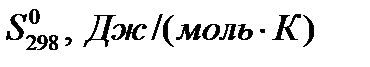 | ||||
| Al (к) | 28,31 | ||||||
| Al2O3 (к) | – 1675,0 | – 1576,4 | 50,94 | ||||
| – 981,57 | – 944,75 | 199,4 | ||||
| C (алмаз) | 1,897 | 2,866 | 2,38 | ||||
| С (графит) | 5,74 | ||||||
| CO (г) | – 110,5 | – 137,27 | 197,4 | ||||
| CO2(г) | – 393,51 | – 394,38 | 213,6 | ||||
| COCl2(г) | – 223,0 | –210,5 | 289,2 | ||||
| CS2 (г) | – 115,3 | 65,1 | 237,8 | ||||
| CS2 (ж) | – 87,8 | 63,6 | 151,0 | ||||
| C2H2 (г) | 226,75 | 209,2 | 200,8 | ||||
| C2H4 (г) | 52,28 | 68,12 | 219,4 | ||||
| CH4 (г) | – 74,85 | – 50,79 | 186,19 | ||||
| C2H6 (г) | – 84,67 | – 32,89 | 229,5 | ||||
| C6H6 (ж) | 49,04 | 124,50 | 173,2 | ||||
| CH3 OH (ж) | – 238,7 | – 166,31 | 126,7 | ||||
| C2H5 OH (ж) | – 227,6 | – 174,77 | 160,7 | ||||
| Ca (к) | 41,62 | ||||||
| CaО (к) | – 635,1 | – 604,2 | 39,7 | ||||
| Ca(OH)2 (к) | – 986,2 | – 896,76 | 83,4 | ||||
| CaCО3(к) | – 1206,0 | – 1128,8 | 92,9 | ||||
| Cl2 (г) | 223,0 | ||||||
| HCl (г) | – 92,30 | – 95,27 | 186,7 | ||||
| HCl (ж) | – 167,5 | – 131,2 | 55,2 | ||||
| Cu (к) | 33,3 | ||||||
| Cu2O (к) | – 167,36 | – 146,36 | 93,93 | ||||
| CuO (к) | – 165,3 | – 127,19 | 42,64 | ||||
| Cu2S (к) | – 82,01 | – 86,19 | 119,24 | ||||
| Fe (к) | 27,15 | ||||||
| FeO (к) | – 263,68 | – 244,35 | 58,79 | ||||
| FeCl2(к) | – 341,0 | – 302,08 | 119,66 | ||||
| Fe2O3(к) | – 821,32 | 740,99 | 89,96 | ||||
| Fe3O4(к) | – 1117,1 | – 1015,5 | 146,2 | ||||
| Ge (к) | 31,09 | ||||||
| GeO (к) | – 305,4 | – 276,1 | 50,2 | ||||
| GeO2 (к) | – 539,74 | – 531,4 | 52,30 | ||||
| H2 (г) | 130,6 | ||||||
| H2O (г) | – 241,84 | – 228,8 | 188,74 | ||||
| H2O (ж) | 285,84 | – 237,5 | 69,96 | ||||
| N2 (г) | 191,5 | ||||||
| N2О (г) | 81,55 | 103,6 | 220,0 | ||||
| NО (г) | 90,37 | 86,69 | 210,62 | ||||
| NО2(г) | 33,89 | 51,84 | 240,45 | ||||
| NН3(г) | – 46,19 | – 16,64 | 192,5 | ||||
| NН4Cl (к) | – 315,39 | – 343,64 | 94,56 | ||||
| NН4OH(ж) | – 366,69 | – 263,8 | 179,9 | ||||
| NaOH (к) | – 426,6 | – 377,0 | 64,18 | ||||
| NaCl (к) | – 410,9 | – 384,0 | 72,36 | ||||
| O2 (г) | 205,03 | ||||||
| Pb (к) | 64,9 | ||||||
| PbO (к) | – 217,86 | – 188,49 | 67,4 | ||||
| PbO2 (к) | – 276,6 | – 218,99 | 76,44 | ||||
| SO2 (г) | – 296,9 | – 300,37 | 248,1 | ||||
| H2S (г) | – 20,15 | – 33,02 | 205,64 | ||||
| H2S (ж) | – 39,33 | – 27,36 | 122,2 | ||||
| Sn (к) | 51,55 | ||||||
| SnO (к) | – 286,0 | – 257,32 | 56,74 | ||||
| SnO2 (к) | – 580,8 | – 519,65 | 52,34 | ||||
| Ti (к) | 30,6 | ||||||
| TiO2 (к) | – 938,6 | – 852,2 | 49,92 |
Приложение 5
Коэффициенты активности ионов при различных ионных силах раствора
| Ионная сила раствора | Заряд иона z | Ионная сила раствора IC | Заряд иона z | ||||
| ±1 | ±2 | ±3 | ±1 | ±2 | ±3 | ||
| 0,05 0,1 0,2 | 0,84 0,81 0,80 | 0,50 0,44 0,41 | 0,21 0,16 0,14 | 0,3 0,4 0,5 | 0,81 0,82 0,84 | 0,42 0,45 0,50 | 0,14 0,17 0,21 |
Приложение 6
Константы диссоциации некоторых слабых электролитов
в водных растворах, 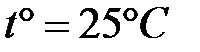
| Электролит | Кд | 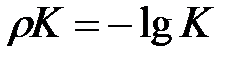 | |
| HNO2 | 4.0·10 – 4 | 3.40 | |
| NH4OH | 1.8·10 – 5 | 4.75 | |
| H2SiO3 | K1 | 2.2·10 – 10 | 9.66 |
| K2 | 1.6·10 – 12 | 11.80 | |
| H2SO4 | K2 | 1.2·10 – 2 | 1.92 |
| H2SO3 | K1 | 1.6·10 – 2 | 1.80 |
| K2 | 6.3·10 – 8 | 7.21 | |
| H2S | K1 | 6.0·10 – 8 | 7.22 |
| K2 | 1.0·10 – 14 | 14.0 | |
| H2CO3 | K1 | 4.5·10 – 7 | 6.35 |
| K2 | 4.7·10 – 11 | 10.33 | |
| CH3COOH | 1.8·10 – 5 | 4.75 | |
| H3PO4 | K1 | 7.5·10 – 3 | 2.12 |
| K2 | 6.3·10 – 8 | 7.20 | |
| K3 | 1.3·10 – 12 | 11.89 | |
| HF | 6.6·10 – 4 | 3.18 | |
| HCN | 7.9·10 – 10 | 9.10 |
Приложение 7
Степень диссоциации кислот, щелочей и солей
в водных растворах, 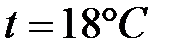 .
.
| Электролит и его ионы | α % | |
| 1Н | 0,1Н | |
| Кислоты | ||
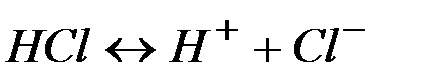 | ||
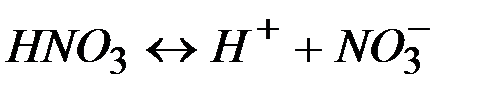 | ||
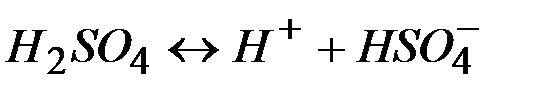 | ||
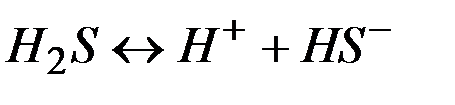 | - | 0,07 |
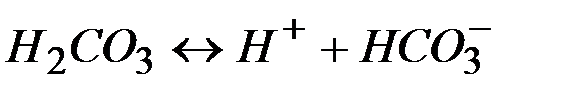 | - | 0,17 |
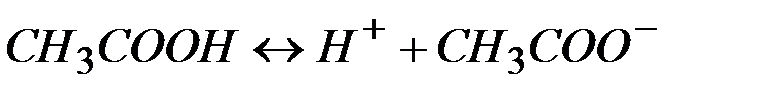 | 0,4 | 1,3 |
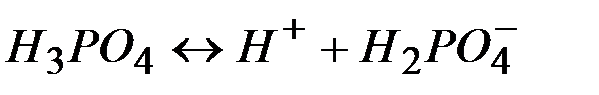 | ||
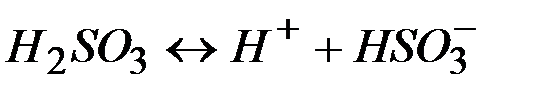 | - | |
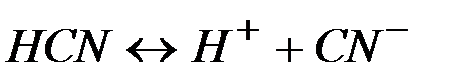 | - | 0,01 |
| Основания | ||
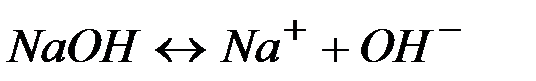 | ||
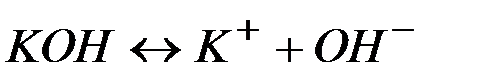 | ||
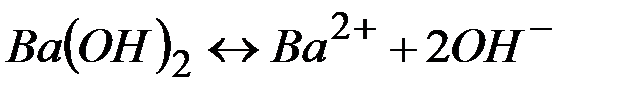 | - | |
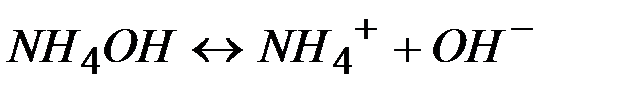 | 0,4 | 1,3 |
| Соли | ||
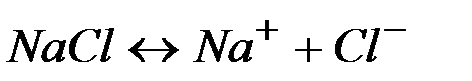 | ||
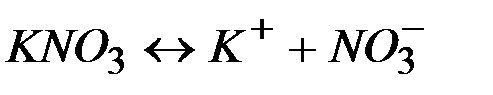 | ||
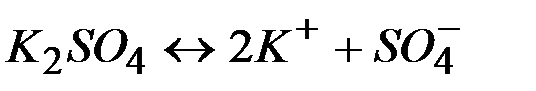 | ||
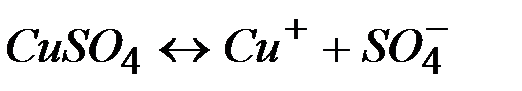 |
Приложение 8
Ионное произведение воды (Kw) при разных значениях температуры
| t, 0C | Kw · 10-14 | t, 0C | Kw · 10-14 | |
| 0,11 | 2,40 | |||
| 0,17 | 2,95 | |||
| 0,30 | 5,50 | |||
| 0,46 | 9,55 | |||
| 0,69 | 15,8 | |||
| 1,00 | 25,8 | |||
| 1,48 | 38,8 | |||
| 2,09 | 55,0 |
Приложение 9
Плотности водных растворов некоторых растворов при 200C
| Вещество | Масса % | |||||||||
| 1н. | ||||||||||
| NaCl | 1,01 | 1,04 | 1,07 | 1,12 | 1,15 | 1,19 | 1,04 | |||
| KCl | 1,01 | 1,04 | 1,06 | 1,10 | 1,13 | 1,16 | 1,04 | |||
| Na2SO4 | 1,02 | 1,05 | 1,09 | 1,15 | 1,06 | |||||
| K2SO4 | 1,02 | 1,05 | 1,08 | 1,07 | ||||||
| MgSO4 | 1,02 | 1,06 | 1,10 | 1,17 | 1,22 | 1,27 | ||||
| NaNO3 | 1,03 | 1,07 | 1,14 | 1,23 | 1,05 | |||||
| BaCl2 | 1,04 | 1,09 | 1,20 | 1,27 | 1,09 | |||||
| NH4NO3 | 1,01 | 1,04 | 1,08 | 1,13 | 1,18 | 1,23 | ||||
| (NH4) 2SO4 | 1,01 | 1,06 | 1,12 | 1,17 | 1,23 | |||||
| NH4Cl | 1,00 | 1,03 | 1,06 | 1,07 | ||||||
| FeSO4 | 1,02 | 1,10 | 1,17 | 1,20 | ||||||
| Al2(SO4)3 | 1,02 | 1,10 | 1,23 | 1,31 |
Приложение 10
Произведения растворимости некоторых малорастворимых электролитов при 25оС.
| Электролит | ПР (KS) | Электролит | ПР (KS) |
| AgBr | 6,3×10-13 | CdS | 7,9×10-27 |
| AgBrO3 | 5,5.10-5 | CoS (18oC) | 2,0.10-27 |
| AgCl | 1,56×10-10 | Cu(OH)2 | 5,6.10-20 |
| Ag2CrO4 | 1,1×10-12 | CuS | 4,0×10-38 |
| AgI | 1,5×10-16 | Fe(OH)2 | 8,0×10-16 |
| Ag2SO4 | 7,7.10-5 | Fe(OH)3 (18oC) | 3,8×10-38 |
| Ag2S | 5,7.10-51 | FeS | 3,7.10-19 |
| Al(OH)3 | 1,9×10-33 | Mg(OH)2 | 5,5×10-12 |
| BaCO3 | 7,0×10-9 | MnS розовый | 2,5×10-10 |
| BaCrO4 | 2,3.10-10 | NiS (18oC) | 2,0.10-28 |
| BaC2O4 | 1,2×10-7 | PbCl2 | 2,4×10-5 |
| Ba3(PO4)2 | 6,0.10-39 | PbI2 | 8,7.10-9 |
| BaSO4 | 1,08×10-10 | PbS (18oC) | 1,1.10-29 |
| CaCO3 | 4,8×10-9 | PbSO4 | 2,2×10-8 |
| CaC2O4 | 2,6×10-9 | SrCO3 | 1,1×10-10 |
| CaF2 | 4,0.10-11 | SrSO4 | 2,3×10-7 |
| Ca3(PO4)2 | 1,0.10-29 | Zn(OH)2 (20oC) | 4,0.10-16 |
| CaSO4 | 6,1×10-5 | ZnS | 1,6×10-24 |
Приложение 11
Константы гидролиза некоторых протолитов в водных растворах при 250С
| Электролит | Константа протолиза, моль/л | |
| Название | Формула | |
| Пероксид водорода | Н2О2 | КК1~10−12 (Н2О2, НО2−,Н2О) КК2~10−25 (Н2О −, НО22−,Н2О) |
| Циановодород | HCN | КК =7∙10−10 (НCN, CN−,Н2О) |
| Метакремниевая кислота | Н2SiO3 | КК1~10−10 (Н2 SiO3, НSiО3−,Н2О) КК2~10−12 (НSiO3 −, SiО32−,Н2О) |
| Cероводород | Н2S | КК1=6 ∙10−8 (Н2S, НS−,Н2О) КК2=1 ∙10−14 (НS −, S2−,Н2О) |
| Угольная кислота | Н2СО3 | КК1=4,5 ∙10−7 (Н2СО3, НСО3−,Н2О) КК2=4,7∙10−11 (НСО3−, СО32−,Н2О) |
| Гидрат аммиака | NH3 ∙HOH | Кo=2 ∙10−5 (NН3∙HOH, NН4+,Н2О) |
| Уксусная кислота | СН3СООН | КК=2 ∙10−5 (СН3СООН,СН3СОО−,Н2О) |
| Азотистая кислота | НNO2 | КК=4∙10−4 (НNО2, NО2−,Н2О) |
| Фтороводород | HF | КК=7∙10−4 (НF, F−,Н2О) |
| Ортофосфорная кислота | Н3РО4 | КК1=8∙10−3 (Н3РО4, Н2РО4−,Н2О) КК2=6∙10−8 (Н2РО4−, НРО42−,Н2О) КК3=1∙10−12 (НРО42−,РО43−, Н2О) |
| Сернистая кислота | Н2SO3 | КК1=2∙10−2 (Н2SO3, НSО3−,Н2О) КК2=6∙10−8 (НSO3 −, SО32−,Н2О) |
| Азотная кислота | HNO3 | КК=43,6(НNО3, NО3−,Н2О) |
| Марганцовая кислота | HMnO4 | КК=200(НMnО4, MnО4−,Н2О) |
| Серная кислота | H2SO4 | КК1=1000(Н2SO4, НSО4−,Н2О) КК2=1∙10−2 (НSO4 −, SО42−,Н2О) |
| Хлороводород | HCI | КК=1∙107 (НСI,СI−,Н2О) |
| Бромоводород | HBr | КК=1∙109 (НBr, Br−,Н2О) |
| Йодоводород | HJ | КК=1∙1011 (НJ, J−,Н2О) |
Приложение 12
Свойства важнейших двухцветных кислотно-основных индикаторов
| Индикатор | Переход окраски | Интервал pH |
| Метиловый оранжевый | Красная → оранжевая | 3,1 – 4,0 |
| Лакмоид | Красная → синяя | 4,0 – 6,4 |
| Метиловый красный | Красная → желтая | 4,2 – 6,2 |
| Бромтимоловый | Желтая → синяя | 6,0 – 7,6 |
Приложение 13
Стандартные электродные потенциалы (∆Еº) некоторых металлов
| Электрод | Е0, В | Электрод | Е0, В | |
| Li+/Li Rb+/Rb K+/K Cs+/Cs Ba2+/Ba Ca2+/Ca Na+/Na Mg2+/Mg AI3+/AI Ti2+/Ti Zr4+/Zr Mn2+/Mn V2+/V Cr2+/Cr Zn2+/Zn Cr3+/Cr Fe2+/Fe | −3,045 −2,925 −2,924 −2,923 −2,90 −2,87 −2,714 −2,37 −1,70 −1,603 −1,58 −1,18 −1,18 −0,913 −0,763 −0,74 −0,44 | Cd+/Cd Co2+/Co Ni2+/Ni Sn2+/Sn Pb2+/Pb Fe3+/Fe 2H+/H Sb3+/Sb Bi3+/Bi Cu2+/Cu Cu+/Cu Fe Hg22+/2Hg Ag+/Ag Hg2+/Hg Pt2+/Pt Au3+/Au Au+/Au | −0,403 −0,277 −0,25 −0,136 −0,127 −0,037 −0,000 +0,20 +0,215 +0,34 +0,52 +0,77 +0,79 +0,80 +0,85 +1,19 +1,50 +1,70 |
Приложение 14
Стандартные восстановительные потенциалы, 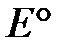 при
при 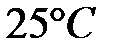 .
.
| Процесс | 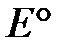 , В , В | |
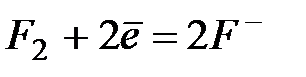 | +2,87 | |
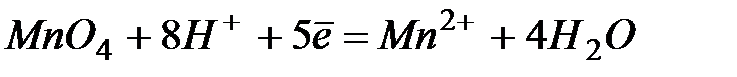 | +1,51 | |
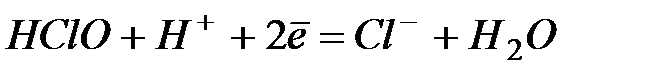 | +1,50 | |
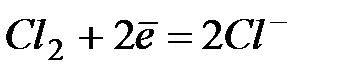 | +1,36 | |
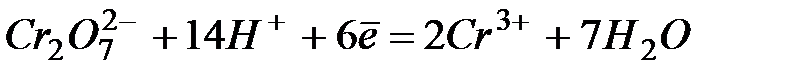 | +1,33 | |
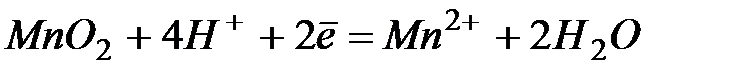 | +1,23 | |
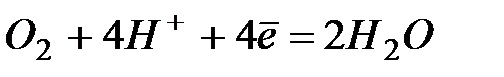 | +1,23 | |
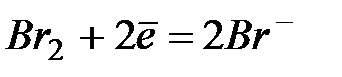 | +1,07 | |
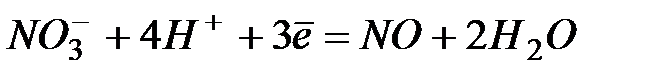 | +0,96 | |
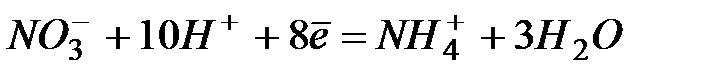 | +0,87 | |
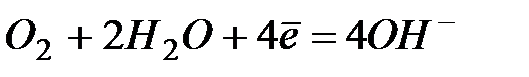 | +0,815 | |
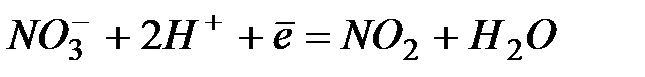 | +0,80 | |
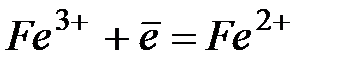 | +0,77 | |
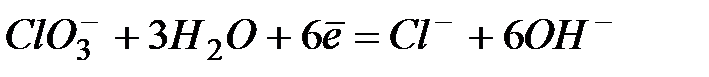 | +0,63 | |
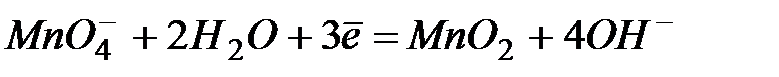 | +0,60 | |
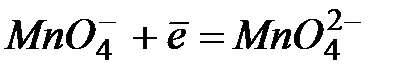 | +0,56 | |
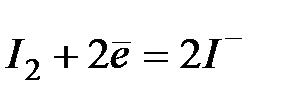 | +0,54 | |
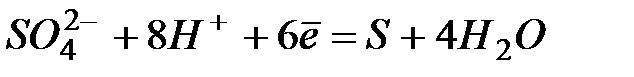 | +0,36 | |
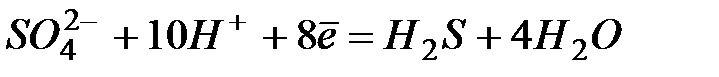 | +0,31 | |
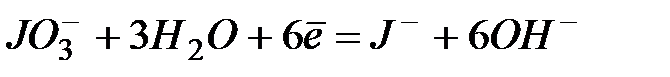 | +0,26 | |
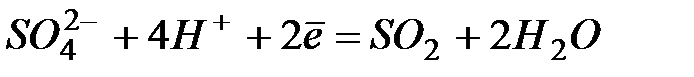 | +0,17 | |
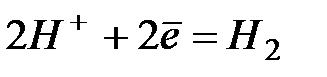 | 0,000 | |
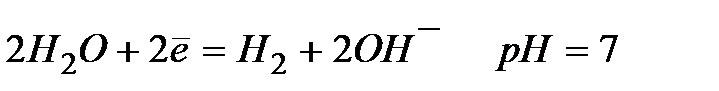 (pH=9) (pH=9) | -0,413 (-0,53) | |
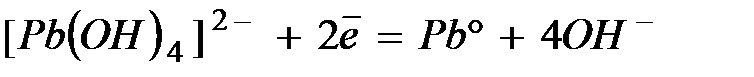 | -0,54 | |
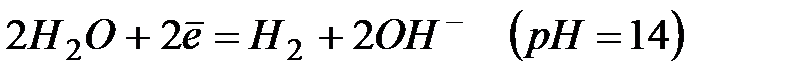 | -0,83 | |
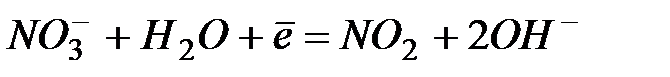 | -0,86 | |
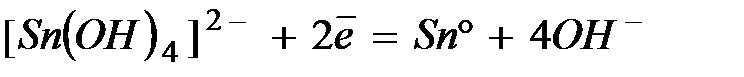 | -0,91 | |
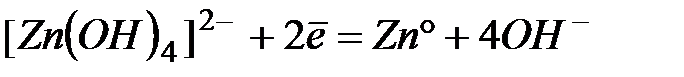 | -1,22 | |
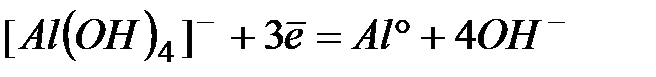 | -2,35 | |
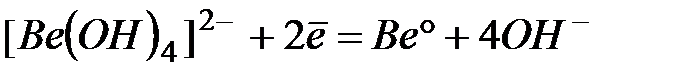 | -2,55 |
Приложение 15
Константы нестойкости комплексных ионов в водных растворах при 25оС.
| Схема диссоциации комплексного иона | Кнестойкости | рК |
| [Ag(NH3)2]+DAg+ + 2NH3 | 5,89×10-8 | 7,23 |
| [Ag(NO2)2]-D Ag+ + 2NO2- | 1,3×10-3 | 2,89 |
| [Ag(S2O3)2]3-D Ag+ + 2S2O32- | 2,5×10-14 | 13,60 |
| [Ag(CN)2]-D Ag+ + 2CN- | 1,4×10-20 | 19,85 |
| [AgI2]-D Ag+ + 2I- | 5,5.10-12 | 11,74 |
| [Al(OH)4(H2O)2]-D Al3+ + 2OH- + 2H2O | 1,0.10-33 | 33,0 |
| [AlF6]3-D Al3+ + 6F- | 5,01.10-18 | 17,30 |
| [AuCl4]-D Au3+ + 4Cl- | 5,0.10-22 | 21,30 |
| [Be(OH)4]2-D Be2+ + 4OH- | 1,0.10-15 | 15,0 |
| [BeF4]2-D Be2+ + 4F- | 4,17 .10-17 | 16,30 |
| [CaЭДТА]2-D Ca2+ + ЭДТА | 2,57.10-11 | 10,59 |
| [Cd(CN)4]2-D Cd2+ + 4CN- | 7,76.10-18 | 17,11 |
| [Cd(En)2]2+D Cd2+ + 2En | 6,0.10-11 | 10,22 |
| [Cd(NH3)6]2+D Cd2+ + 6NH3 | 2,76.10-5 | 4,56 |
| [Co(C2O4)3]3-D Co3+ + C2O42- | 5,0.10-12 | 11,30 |
| [Co(En)3]3+D Co3+ + 3En | 2,04.10-49 | 48,69 |
| [Co(NH3)6]2+D Co2+ + 6NH3 | 4,07.10-5 | 4,39 |
| [Co(NH3)6]3+D Co3+ + 6NH3 | 6,15.10-36 | 35,21 |
| [Co(NO2)6]3-D Co3+ + 6NO2- | 1,0.10-22 | 22,0 |
| [Co(SCN)4]2-D Co2+ + 4SCN- | 5,50.10-3 | 2,26 |
| [CoЭДТА]2-D Co2+ + ЭДТА | 4,90.10-17 | 16,31 |
| [CoЭДТА]3-D Co3+ + ЭДТА | 2,51.10-41 | 40,60 |
| [Cr(OH)4]-D Cr3+ + 4OH- | 1,26.10-30 | 29,90 |
| [CrЭДТА]3-D Cr3+ + ЭДТА | 3,98.10-24 | 23,40 |
| [Cu(CN)2]- D Cu+ + 2CN- | 1,0.10-24 | 24,00 |
| [Cu(CN)4]3-D Cu+ + 4CN- | 5,13.10-31 | 30,29 |
| [Cu(H2O)2Br2]oD Cu2+ + 2Br - + 2H2O | 2,22.10-6 | 5,75 |
| [Cu(NH3)4]2+D Cu2+ + 4NH3 | 9,33.10-13 | 12,03 |
| [Fe(CN)6]4-D Fe2+ + 6CN- | 1,4×10-37 | 36,84 |
| [Fe(CN)6]3-D Fe3+ + 6CN- | 1,5×10-44 | 43,82 |
| [Fe(SCN)3] D Fe3+ + 3SCN- | 2,9×10-5 | 4,54 |
| [FeCl3] D Fe3+ + 3Cl- | 7,4×10-2 | 1,13 |
| [FeF6]3-D Fe3+ +6F- | 7,94×10-17 | 16,10 |
| [FeЭДТА]2-D Fe2+ + ЭДТА | 6,31.10-15 | 14,20 |
| [FeЭДТА]3-D Fe3+ + ЭДТА | 5,89.10-25 | 24,23 |
| [HgBr4]2-D Hg2+ + 4Br- | 1,0×10-21 | 21,0 |
| [HgI4]2-D Hg2+ + 4I- | 1,4×10-30 | 29,85 |
| [Hg(CN)4]2-D Hg2+ + 4CN- | 4,0×10-42 | 41,40 |
| [Hg(SCN)4]2-D Hg2+ + 4SCN- | 8,0×10-22 | 21,10 |
| [MgЭДТА]2-D Mg2+ + ЭДТА | 7,59.10-10 | 9,12 |
| [NH4]+D NH3 + H+ | 6,0.10-10 | 9,22 |
| [Ni(En)3]2+D Ni2+ + 3En | 7,76.10-20 | 19,11 |
| [Ni(NH3)4]2+D Ni2+ + 4NH3 | 1,12.10-8 | 7,95 |
| [Ni(NH3)6]2+D Ni2+ + 6NH3 | 9,77.10-9 | 8,01 |
| [NiЭДТА]2-D Ni2+ + ЭДТА | 2,40.10-19 | 18,62 |
| [PtBr4]2-D Pt2+ + 4Br- | 3,0.10-21 | 20,52 |
| [PtCl4]2-D Pt2+ + 4Cl- | 1,0.10-16 | 16,00 |
| [SnCl6]4-D Sn2+ + 6Cl- | 5,1×10-11 | 10,29 |
| [Zn(CN)4]2-D Zn2+ + 4CN- | 6,3×10-18 | 17,20 |
| [Zn(NH3)4]2+D Zn2+ + 4NH3 | 2,0.10-9 | 8,70 |
| [Zn(OH)4]2-D Zn2+ + 4OH- | 3,6.10-16 | 15,44 |
| [ZnЭДТА]2-D Zn2+ + ЭДТА | 5,50.10-17 | 16,26 |
Приложение 16
