Вопрос №1 История возникновения химии как науки. Роль химии в пожарном деле (25 мин.)
МЕТОДИЧЕСКАЯ РАЗРАБОТКА
Проведения лекционного занятия
по дисциплине «Химия»
для курсантов 1 курса по специальности 280705.65 –
«Пожарная безопасность»
РАЗДЕЛ I
ВВЕДЕНИЕ В ОБЩУЮ ХИМИЮ
ТЕМА 1
ОСНОВНЫЕ ПОНЯТИЯ И ЗАКОНЫ ХИМИИ.
РОЛЬ ХИМИИ В ПОЖАРНОМ ДЕЛЕ.
ЗАНЯТИЕ № 1.1.
ВВЕДЕНИЕ В ПРЕДМЕТ.
ОСНОВНЫЕ ПОНЯТИЯ И ЗАКОНЫ ХИМИИ.
Обсуждена на заседании ПМК
протокол №____ от «___»________2015 г.
Владивосток
2015 г.
I. Цели занятия
Учебная: ознакомить с историей возникновения химии как науки, ввести основные понятия химической науки, основные стехиометрические законы;
Воспитательная: воспитывать у обучаемых ответственность за подготовку к практической деятельности.
II. Расчет учебного времени
| Содержание и порядок проведения занятия | Время, мин |
| ВВОДНАЯ ЧАСТЬ | |
| ОСНОВНАЯ ЧАСТЬ | |
| Учебные вопросы | |
| 1. История возникновения химии как науки. Роль химии в пожарном деле | |
| 2. Основные понятия химии | |
| 3. Стехиометрические законы химии | |
| ЗАКЛЮЧИТЕЛЬНАЯ ЧАСТЬ |
III. Литература
Основная
1. Глинка Н.Л. Общая химия: Учебное пособие для вузов/ Под ред. А.И. Ермакова. – изд. 30-е, исправленное-М.: Интеграл-Пресс, 2007.-728 с.
2.Е.Г. Коробейникова, А.П. Чуприян, В.Р. Малинин, Г.К. Ивахнюк, Н.Ю. Кожевникова. Химия. Курс лекций Учебное пособие по спец. 280104.65 – Пожарная безопасность. /Под ред. Проф. В.С.Артамонова /СПб.: Санкт-Петербургский университет ГПС МЧС России, 2011 г. – 425 с.
3. Некрасов Б.В. Основы общей химии. – 4-е изд.,- СПб: Изд-во «Лань», 2003. - 656 с.
Дополнительная
1. Суворов А.В., Никольский А.Б. Вопросы и задачи по общей химии., - СПб: Химиздат, 2002.- 304 с.
Нормативно-правовые документы
1. ГОСТ 12.1.004 – 91 *. Пожарная безопасность. Общие требования
IV. Учебно-материальное обеспечение
1. Технические средства обучения: телевизор, графопроектор, видеомагнитофон, DVD-проигрыватель, компьютерная техника, интерактивная доска.
2. Периодическая система элементов Д.И. Менделеева, демонстрационные плакаты, схемы.
V. Текст лекции
Тема 1. ОСНОВНЫЕ ПОНЯТИЯ И ЗАКОНЫ ХИМИИ
ВВОДНАЯ ЧАСТЬ (3 мин.)
Преподаватель проверяет наличие слушателей (курсантов), объявляет тему, учебные цели и вопросы занятия.
ОСНОВНАЯ ЧАСТЬ ( 85 мин)
Вопрос №1 История возникновения химии как науки. Роль химии в пожарном деле (25 мин.)
Химия – наука о веществах и их превращениях.
В общей системе наук химию относят к естественным наукам, т.к. она занимается изучением явлений и объектов природы.
Существует несколько толкований названия “химия”.
Согласно одному ‘chymeia” – наливание, настаивание. Это можно связать с древней практикой восточных врачей и фармацевтов, извлекавших соки лекарственных растений.
Согласно другому “khem” или “khame” означает черную страну, чернозем. Так называли Древний Египет.
Химики занимались и изучением земных недр, латинское слово “humus” означает “земля“.
Но есть еще и греческие слова “хюмос” – сок; “хюма” – литье, поток река; “химевсис” – смешивание.
А древнекитайское слово “ким” означает золото. Золотоделие – одно из первых занятий химиков.
И хотя мы не знаем точного происхождения слова “химия”, можно восстановить основные этапы развития этой науки.
1 этап: Древний мир – конец XVII века
Считается, что химия зародилась в Древнем Египте в III – IV веках до н.э. – технически передовой стране древнего мира. Обработка металлов, крашение, стеклоделие, бальзамирование достигли там значительного развития. Химия в Египте считалась наукой божественной, находилась в руках жрецов и тщательно скрывалась от всех посвященных.
Однако некоторые химические сведения все же просачивались за пределы Египта. Именно арабы прибавили к первоначальному слову характерную приставку “ал”. Понятие “алхимия” стало впоследствии характеризовать целую эпоху в развитии химической науки.
Само название “алхимия” появилось лишь в XII веке и существовало вплоть до конца XVII века. Основателем алхимии считают Гермеса Трисмегиста (Гермеса Трижды Величайшего). Он владел так называемыми герметическими знаниями – астрологией, кабалой (учением о магическом значении чисел) и алхимией, причем алхимию он считал искусством.
Вся работа алхимиков была направлена на поиски философского камня, превращающего любой металл в золото, и на поиски эликсира молодости.
Алхимический этап был важным этапом накопления химических знаний. В процессе поиска несуществующего философского камня алхимики освоили методику основных химических операций (перегонка, фильтрование, возгонка, кристаллизация), получили ряд новых веществ (мышьяк, сурьма, фосфор, серную и азотную кислоты, множество солей).
К сожалению, алхимики сохраняли результаты своих работ в строжайшей тайне, поэтому многие из их открытий были утеряны и открывались позднее вновь. Коренная перестройка алхимии произошла в начале XVI века. Реформаторами алхимии выступили Парацельс и Агрикола.
Врач Парацельс (Теофаст Гогенгейм) считал, что “цель химии состоит не в изготовлении золота и серебра, а в изготовлении лекарств”. Многие врачи примкнули к теории Парацельса и занялись химией.
Георгий Агрикола работал в области горного дела и металлургии. Книги Агриколы дошли до наших дней, и некоторые описанные им методы не потеряли своего значения до сих пор.
В начале XVI века работал и Ванноччо Бирингуччо - автор известного труда “Пиротехния”, в котором описаны состав пороха, его свойства, рассмотрено действие огня на металлы.
Все сколько-нибудь заметные химики XVI – XVII века были еще и алхимиками. Знание алхимии – признак тогдашней учености.
На Руси критически относились к попыткам получения золота из металлов. Здесь развивалась так называемая ремесленная химия: кожевенное дело, крашение, изготовление лекарств, металлургия. В XV веке было налажено производство селитры, в XVI веке в Туле – производство железа, а в Костроме – мыла. В начале XVII века при содействии Петра I начал работу первый стекольный завод. Петр I рассматривал все проекты, кроме алхимических, поскольку был уверен, что “тот, кто выдает себя делателем золота, должен быть или обманщиком, или невежей в химии”.
II этап: середина XVII - середина XIX века
В XVII веке химическая практика настолько переросла алхимическую теорию, что положение стало тормозящим для дальнейшего развития науки.
В 1660 году появляется первая теория – флогистонная теория Георга-Эрнеста Шталя – придворного врача короля Фридриха-Вильгельма I.
Так случилось, что первая химическая теория была ошибочной. Согласно этой теории во всех телах, способных гореть и окисляться, содержится особое вещество – флогистон. Чем больше флогистона в веществе, тем оно более способно к горению. По мнению Шталя, уголь целиком состоял из флогистона, а металлы – сложные вещества, теряя флогистон, превращались в простые вещества – оксиды. Единственное, что смущало исследователей, что металлы, теряя флогистон, увеличивали свой вес, но и этому нашли “объяснение”: решили, что флогистон имел отрицательный вес.
Поиски самого флогистона ни к чему не привели. Первый удар по этой теории нанес в 1775 году французский химик Лавуазье после открытия им кислорода. Он показал, что никакого флогистона в природе не существует, металлы под воздействием кислорода превращаются в оксиды, увеличивая свой вес, а уголь – в углекислый газ.
Датой рождения химии как точной науки можно считать сороковые годы XVIII века, когда великий русский ученый Михаил Васильевич Ломоносов изложил основы атомно-молекулярного учения (1741 г.) и впервые сформулировал закон сохранения массы (1748 г.).
Через 40 лет в 1789 году закон сохранения массы был независимо от Ломоносова открыт Лавуазье.
Именно на этом этапе химия формируется как самостоятельная наука, у которой имеются в наличии все признаки точных наук: наличие отвлеченных рассуждений (теории, гипотезы, законы); воспроизводимость фактов; применимость на практике.
Второй этап развития химии был связан с изучением свойств и технологией получения главным образом неорганических веществ. Было установлено, что свойства веществ определяются его составом.
III этап: середина XIX века – начало XX века
Третий этап развития химии ознаменовался формированием фундаментальных теоретических основ этой науки. Это открытие Д.И. Менделеевым в 1869 году Периодического закона и открытие А.М. Бутлеровым в 1861 году теории строения органических соединений.
Именно на этом этапе были заложены основы промышленной технологии органических веществ, началось “ триумфальное шествие органической химии”. Было доказано, что свойства веществ определяются не только составом, но и химическим строением.
IV этап: XX век – современный период
В начале XX века были сделаны фундаментальные открытия, прежде всего открытие сложного строения атома. На основе этих открытий были осуществлен синтез новых элементов. На этом этапе развития химии получило развитие учение о процессе – основе нефтехимического синтеза, а также теория и практика катализа. Огромные достижения были достигнуты в области биологической химии, которая изучает превращение химических веществ в живых организмах.
Но развитие науки и техники поставило перед человечеством и вопрос о безопасности и самих веществ, и технологии их производств. Здесь уместно привести слова академика В.А. Легасова: “Человечество в своем промышленном развитии достигло такого уровня использования энергии всех видов, построили инфраструктуру с высоким уровнем концентрации энергетических мощностей, что беды от их аварийного разрушения стали соизмеримы с бедами от военных действий и стихийных бедствий”.
Эти слова в полной мере могут быть отнесены и к состоянию пожарной безопасности в стране и в мире.
На Земле каждый час происходит около 600 пожаров, каждые 30 минут в нашей стране в огне погибает человек.
Развитие науки, в том числе и достижения химии, с одной стороны, делают мир более пожароопасным, а с другой стороны, создают все более совершенные способы, методы и средства борьбы с огнем. Важно сделать так, чтобы второй процесс не отставал от первого. Именно это – стратегическая задача любой системы обеспечения пожарной и промышленной безопасности.
(Все определения, формулы, графики и уравнения реакций даются под запись.)
Вопрос № 2 Основные понятия химии (30 мин.)
По определению М.В. Ломоносова, “Химическая наука рассматривает свойства и изменения тел, состав тел, объясняет причину того, что с веществами при химических превращениях происходит”.
Вещество – конкретный вид материи, обладающий массой покоя и определенными физическими свойствами. Из различных веществ состоят все окружающие нас тела.
Свойства веществ проявляются в их изменениях. Изменения эти очень разнообразны. Снег под воздействием солнечных лучей тает, металл на открытом воздухе ржавеет, дрова сгорают в печи, пролитая жидкость испаряется. В одних случаях в результате превращений вещества остаются теми же самыми, а в результате других превращений образуются новые вещества. В этом различие химических и физических явлений (превращений).
| Явления (превращения) | |
| физические | химические |
| Явления, при которых вещества не изменяются. | Явления, при которых из одних веществ образуются другие, новые вещества. |
| Примеры: изменения агрегатного состояния твердое вещество ® жидкость ® газ; изменение температуры, плотности. | Примеры: реакция горения, коррозия металлов. |
В 1741 году в книге “Элементы математической химии” великий русский ученый М.В. Ломоносов изложил основы атомно-молекулярного учения. Сущность учения Ломоносова сводится к следующему:
1. Все вещества состоят из корпускул (молекул).
2. Молекулы состоят из элементов (атомов).
3. Молекулы и атомы находятся в непрерывном движении. Теплота состоит во внутреннем движении этих частиц.
4. Молекулы простых веществ состоят из одинаковых атомов. Молекулы сложных веществ - из разных атомов.
Через 67 лет после указанной работы Ломоносова вышла книга английского ученого Джона Дальтона «Новая система химической философии» (1808) в которой были изложены основные положения химической атомистики. Дальтон впервые определил атомные массы известных и ввел свои знаки для обозначения атомов. Для обозначения атомов Дальтон использовал кружки, в которых помещались точки, черточки, начальные буквы английских названий металлов и другие условные знаки. Широкое распространение эта символика не получила. В 1814 году шведский химик Якоб Берцелиус предложил буквенные химические знаки.
Атомно-молекулярное учение в химии окончательно утвердилось лишь в середине XIX века, на международном съезде химиков в Карлсруэ в 1860 году впервые были приняты определения понятий молекулы и атома.
Молекула - это наименьшая частица вещества, обладающая его химическими свойствами. Химические свойства молекулы определяются ее составом и химическим строением.
Атом- наименьшая частица химического элемента, обладающая его химическими свойствами. Химические свойства атома определяются его
строением.
Молекулы могут состоять из разного числа атомов.
| Из 1 атома: | благородные газы Не, Ne, Ar, Kr, Xe |
| Из 2 атомов | Н2, О2, N2, F2, Cl2, Br2, I2, CO |
| Из 3 атомов | Н2О, СО2, HCN, O3 |
| Из 4 атомов | NH3, H2O2 |
| … | |
| Самая большая молекула (2000 г.) (не полимер) 19913 атомов | С5750Н7227N2215O4131S590 |
| Сотни тысяч атомов | Полимерные молекулы |
Химический элемент – вид атомов с одинаковым зарядом ядра.
Химические элементы могут существовать в различных формах: одиночные атомы, простые вещества и сложные вещества.
Простые вещества образованы атомами одного элемента (например, Н2, Р, О3).
Сложные вещества образованы атомами различных элементов (например, Н2О, СаСО3).
С точки зрения пожарной опасности гореть могут как простые, так и сложные вещества. Приведем несколько примеров простых и сложных веществ с различными пожароопасными свойствами.
| Характеристики веществ | Вещества | |
| простые | сложные | |
| Горючие вещества | Н2, С, Р, S, Na, Fe | CO, NH3, CH3COOH |
| Негорючие вещества | N2, Ar, He | H2O, HCl, NaOH, H2SO4 |
| Негорючие вещества, представляющие пожарную опасность | O2, O3, галогены – F2, Cl2, Br2, I2 | CaC2, сильные окислители – HNO3, KMnO4, NH4NO3, CrO3 |
| Вещества, представляющие опасность при взаимодействии с водой | Na, K, Ca | CaC2, SiH4, BH3, NaH |
| Огнетушащие вещества | N2, Ar, He | H2O, CO2, хладоны –галогенпроизводные метана и этана (CF2Br2) |
Чуть более 100 химических элементов, известных на сегодняшний день, образуют около 400 простых веществ. Это объясняется тем, что многие химические элементы образуют несколько простых веществ.
Аллотропия – явление существования простых веществ в нескольких формах, различных по строению и свойствам. Сами формы называются аллотропными модификациями.
Явление аллотропии вызывается двумя основными причинами.
1. Различное число атомов в молекуле, например в кислороде О2 и озоне О3.
2. Различная структура молекул. Так, например, углерод образует четыре аллотропные модификации: алмаз, графит, карбин и фуллерены (шарообразные структуры, содержащие 60, 70 и более атомов углерода).
Рассмотрим понятия относительной атомной и молекулярной массы.
Масса атома чрезвычайно мала и составляет 10-27 – 10-25 кг. Для большинства элементов масса атомов определена достаточно точно. Например,
| Н | 1,674 × 10-27 кг |
| О | 2,667 × 10-26 кг |
| С | 1,993 × 10-26 кг |
При расчетах пользоваться такими числами чрезвычайно неудобно. И еще в 1804 году Дальтон ввел представление об относительной атомной массе как числе, показывающем во сколько раз атом какого-либо элемента тяжелее атома другого элемента, взятого в качестве единицы измерения.
С 1961 года за единицу относительных атомных масс принята атомная единица массы, равная 1/12 части массы изотопа углерода 12С.
1 а.е.м. = 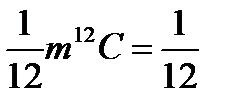 × 1,993 × 10-26 = 1,667 × 10-27 кг
× 1,993 × 10-26 = 1,667 × 10-27 кг
Относительной атомной массой (Аr) элемента называется отношение массы его атома ma(Э) к 1/12 массы атома 12С.
Индекс r – “relative” - относительный.
Аr = 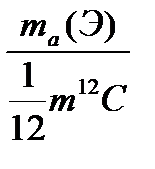 ,
, 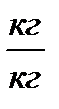 безразмерная величина
безразмерная величина
Для примера рассчитаем относительные атомные массы водорода и кислорода.
Аr (Н) = 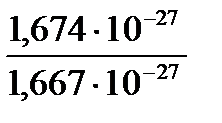 = 1,0079 Аr (О) =
= 1,0079 Аr (О) = 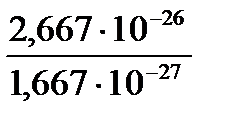 = 15,9994
= 15,9994
Полученные значения численно равны величинам, указанным в периодической системе элементов Д.И. Менделеева.
Относительной молекулярной массой Мr называется отношение массы молекулы вещества mм(в-ва) к 1/12 массы атома 12С.
Мr = 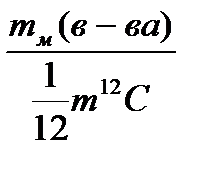 ,
, 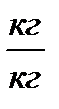 безразмерная величина
безразмерная величина
Рассчитаем по этой формуле относительную молекулярную массу воды. Масса молекулы воды mм(Н2О) = 3,002 × 10-26 кг.
Мr (Н2О) = 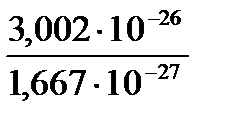 = 18,007 » 18
= 18,007 » 18
Чаще относительную молекулярную массу определяют более простым способом. Молекулярная масса численно равна сумме атомных масс всех атомов, входящих в молекулу вещества (а эти данные указаны в периодической системе элементов Д.И. Менделеева). В качестве примера еще раз рассчитаем относительную молекулярную массу воды:
Мr(Н2О) = 2Аr(Н) + Аr(О) = 2× 1,0079 + 15,9994 = 18,01 » 18
В химии часто необходимо сравнивать абсолютные количества вещества. С этой целью была введена единица измерения количества вещества, которая называется “моль”.
Количеством вещества (n) называется физическая величина, определяемая числом структурных элементов системы (атомов, молекул, ионов).
Моль вещества – это такое его количество, которое содержит одно и то же число частиц. В моле любого вещества содержится число частиц, равное числу Авогадро NA, т.е. 6,02 × 1023.
NA = 6,02 × 1023 1/моль.
Молярная масса (М) – это масса одного моля вещества. Численно она равна относительной молекулярной массе, но в отличие от безразмерной относительной молекулярной массы молярная масса имеет размерность г/моль или кг/кмоль.
Рассчитаем молярную массу воды:
М(Н2О) = mм(Н2О) × NА = 3,002 × 10-26 × 6,02 × 1023 = 0,018 кг/моль =
= 18 г/моль = 18 кг/кмоль.
Число моль (n) может быть рассчитано несколькими способами:
n = 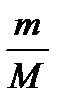 n =
n = 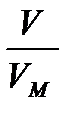 n =
n = 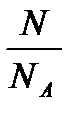
m – масса вещества, г (кг);
M – молярная масса г/моль (кг/кмоль);
V – объем газа или пара, л (м3);
VM – молярный объем газа или пара, л/моль (м3/кмоль);
N – число частиц в образце вещества;
NA – число Авогадро, 1/моль.
Одна из важнейших характеристик атома – это валентность. Связь между валентностью элемента и его положением в периодической системе была установлена Менделеевым. С развитием теории строения атомов и молекул понятие валентности получило физическое обоснование.
Валентность – способность атомов соединяться с другими атомами в определенных соотношениях, т.е. образовывать химические связи. Число связей равно валентности.
За единицу валентности принята валентность атома водорода: он во всех соединениях одновалентен. Если атом элемента присоединяет 1 атом водорода – элемент в этом соединении одновалентен (НCl), если 2 атома водорода – двухвалентен (Н2S) и т.д. Валентность элемента можно определять и по другим элементам, валентность которых известна.
В каждой химической реакции участвуют исходные вещества (реагенты) и образуются продукты реакции (конечные вещества).
С2Н5СООСН3 + 5О2 ® 4СО2 + 4Н2О
исходные вещества конечные вещества
(реагенты) (продукты реакции)
Коэффициенты, стоящие перед веществами в уравнении реакции, называются стехиометрическими коэффициентами.
(Все определения, формулы, графики и уравнения реакций даются под запись.)
