Ионные кристаллы - гигантские полимерные молекулы.
▼ Понятие валентности к ионной связи неприменимо.
Чисто ионная связь не существует - доля ионности связи ( Na+0.9Cl-0.9 )
▼ Ионные связи - прочные.
▼ Твердые кристаллические вещества ионного типа - тугоплавкие, высокопрочные, но хрупкие, растворяются в полярных растворителях (в Н2О).
Формулы (NаСl, СаF2, Аl2(SО4)3 ) - отражают лишь состав.


Силы И.Ван-дер-Ваальса (голланд.ученый, 1873 г.) – силы межмолекулярного взаимодействия (взаимодействия между молекулами), проявляющиеся на расстояниях, превосходящих размеры частиц.

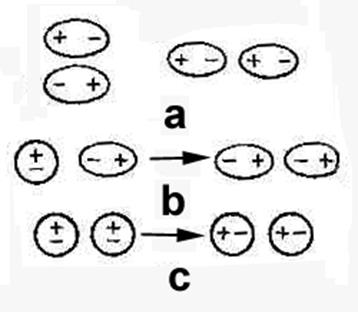
1. ОРИЕНТАЦИОННАЯ СОСТАВЛЯЮЩАЯ ИЛИ ДИПОЛЬ-ДИПОЛЬНОЕ ВЗАИМОДЕЙСТВИЕ (эффект Кьезома) – электростатическое взаимодействие полярных молекул при сближении (рис.а)
Еориен увеличивается с увеличением mмол и уменьшением расстояния между молекулами.
 |
|
3. дисперсионная составляющая(эффект Лондона)
-электростатическое взаимодействие мгновенных диполей, возникающих за счет флуктуации электрической плотности (рис.с). В результате взаимодействия мгновенных диполей энергия системы понижается.
Едисп пропорциональна поляризуемости молекул и обратно пропорциональна расстоянию между центрами частиц.
Для неполярных молекул - единственная составляющая вандерваальсовых сил.
| вещество | mдиполя | Поляризуемость, М3×1030 | Энергия взаимодействия, кДж/моль | Ткип,К | |||
| ориентационная | Индукционная | Дисперсионная | Суммарная | ||||
| H2 Ar Xe HCl HBr HI NH3 | 1,03 0,78 0,38 1,52 | 0,8 1,64 4,16 2,64 3,62 5,42 2,23 | 3,3 1,1 0,6 13,3 | 1,0 0,70 0,3 1,5 | 0,17 8,5 18,4 16,8 28,5 60,6 14,7 | 0,17 8,5 18,4 21,1 30,3 61,5 29,5 | 20,2 239,6 |
Минимальная энергия системы обеспечивается при расстояниях между центрами молекул 0,4 – 0,5 нм, т. е. существенно больше длины химической связи.
Как видно из табл., с увеличением размера молекул в ряду Аr – Хе и НСl – НI растет их поляризуемость и энергия дисперсионного притяжения. Ориентационное взаимодействие вносит значительный вклад в вандерваальсовы силы для молекул с большим mдип. ]
С увеличением åЕ возрастет Ткип жидкостей, а также теплота их испарения.

|
 |  |
М е ж м о л е к у л я р н а я внутримолекулярная
Межмолекулярная Н-связь
А – Н + В – R ® А – Н×××В – R
водород способен глубоко внедряться в электронную оболочку соседнего отрицательно поляризованного атома.
