Риунок 10. Значения логарифмов ионизационного отношения
нитроанилинов в водной серной кислоте.
(Нумерация как в табл.5).
Если постулат Гаммета выполняется, то
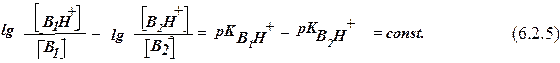
Проверка показала, что эта разность для соединений 1 и 2 сохраняется примерно постоянной (1.24-1.31) во всей области перекрывания величин lg I (рис.10), что позволило установить величину рКВН+ 2-нитроанилина (-0.29).
Далее на основании этой величины были определены таким же методом значения Но для области 24-35% H2SO4 и найдено значение рКВН+ следующего по основности индикатора – 2-нитро-4-хлоранилина (-1.03).
Подобная операция перекрывания повторялась для широкого ряда индикаторов - нитро- и галогеннитроанилинов, значения рКВН+ которых приведены в табл. 5.
Согласно ур-нию (6.2.4) зависимость логарифма ионизационного отношения от функции Но является линейной, с угловым коэффициентом, равным единице. Однако некоторые слабые основания (триарилкарбинолы, амиды карбоновых кислот и т.д.) не подчиняются этому уравнению. Это обусловлено различиями в эффектах сольватации протонированных форм и сопряженных оснований по сравнению с Гамметовскими индикаторами, что влияет на их коэффициенты активности. Для таких оснований были выведены другие функции кислотности. Например, функция HR применима для измерения основности триарилкарбинолов (RC6H4)3C-OH, которые являются вторичными основаниями, т.к. их протонированная форма (RC6H4)3C-OH2+ отщепляет молекулу воды, превращаясь в триарилкарбониевый ион (RC6H4)3C+. Равновесие протонизации триарилкарбинолов описывается уравнением (6.2.6):
 (RC6H4)3C-OH + H+ (RC6H4)3C+ + H2O (6.2.6)
(RC6H4)3C-OH + H+ (RC6H4)3C+ + H2O (6.2.6)
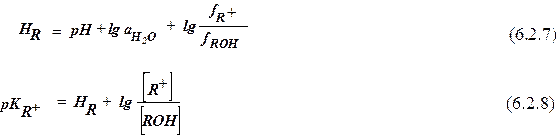 Для этого равновесия по аналогии с ур. (6.2.2) получаем:
Для этого равновесия по аналогии с ур. (6.2.2) получаем:
| Значение функции кислотности | 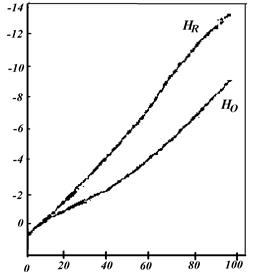 Рисунок 11. Значения функций кислотности Hо и НR растворов серной кислоты Содержание H2SO4, % Рисунок 11. Значения функций кислотности Hо и НR растворов серной кислоты Содержание H2SO4, % |
Уравнение (6.2.7) отличается от ур-ния (6.2.2) наличием дополнительного члена – логарифма активности воды. Поскольку аН2О при увеличении концентрации минеральной кислоты падает, функция HR становится более отрицательной, чем Ho (рис.11)
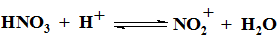
Азотная кислота в среде H2SO4 тоже представляет собой вторичное основание; протонирование ее сопровождается отщеплением молекулы воды (ур-ние 6.2.9):
 (6.2.9)
(6.2.9)
Поэтому для описания ее основности должна быть применима функция HR. Так, в шкале Ho величина рК NO2+ = -8.74±0.25, а в шкале HR -17.1±0.1, что соответствует полупревращению HNO3 в NO2+ в 88%-ной H2SO4. Эффективная бимолекулярная константа скорости нитрования аренов в смесях HNO3/H2SO4 (ур-ние 6.2.10)
RC6H5 + HNO3 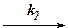 RC6H4NO2 + H2O (6.2.10)
RC6H4NO2 + H2O (6.2.10)
подчиняется функции HR, а не Ho, о чем свидетельствует линейная зависимость dlgk2/d[H2SO4] от функции –dHR/d[H2SO4] с угловым коэффициентом, равным единице.
Это говорит о том, что нитрующим агентом является нитроний-ион, а не H2NO3+, и позволяет из ур-ния (6.2.8) определить его значение pKNO2+. В этих кислотных смесях эффективная константа скорости нитрования второго порядка уменьшается в 104 раз при уменьшении концентрации серной кислоты на 10%.
