Определение константы калориметра
Для определения константы калориметра необходимо нагреть систему. Установите на универсальном блоке питания переменный ток напряжением в 10 В. На измерители работы и мощности нажмите кнопку <Reset> (<Сброс>) и вставьте свободные концы нагревательного элемента в «Out». Когда на дисплее измерителя работы и мощности отобразится значение в 4000 Ws, выключите нагрев и определите точное значение сообщенной электрической энергии. Через 3 минуты остановите запись температуры. Повторите эксперимент. Во избежание ошибок измерения следует провести не менее двух измерений и найти среднее значение.
Обработка экспериментальных данных. На рис. 3 представлен график измерений, построенные в программе в момент остановки измерений. При помощи опции <Обзор> в меню инструментов найдите данные разницы температуры.
.
Рис. 3. График кривой зависимости температуры раствора соли от времени, определение константы калориметра.
Для нахождения величины DТ к участкам кривой до и после температурного скачка проводят касательные. На участке до скачка температуры находят последнюю точку (т.1), а на участке после – первую точку (т.2), одновременно принадлежащие кривой и касательной. Эти точки сносят на ось ординат и определяют величину отрезка, численно равного DТ. Энтальпию растворения соли  рассчитывают по уравнению
рассчитывают по уравнению
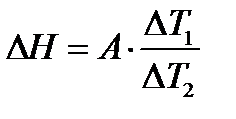
где А– электрическая энергия, сообщенная системе;
DН – тепловой эффект растворения соли, Дж/моль;
DТ1 - изменение температуры в процессе растворения соли, К;
DТ2 - изменение температуры при нагревании системы, К;
Задания для контроля уровня сформированности компетенций в учебное время.
Задача № 1
а) Вычислите теплоту сгорания этанола С2Н5ОН(ж)+ 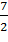 О2(г)→2СО2(г)+3Н2О(ж).
О2(г)→2СО2(г)+3Н2О(ж).
б) Проделайте то же самое для глюкозы С6Н12О6(т).
в) Сопоставьте удельные теплоты сгорания (в кДж/г) этанола и глюкозы. На основании расчёта укажите, что является лучшим источником энергии – водка или конфета? Примите к сведению, что водка содержит 40 вес % этанола, а конфета – 100 вес % глюкозы.
Задача № 2
В стакане молока с низкой жирностью содержится приблизительно 8 г белков, 12 г углеводов и 4 г жиров. Вычислите приблизительную калорийность стакана такого молока в кДж и ккал.
9.Учебно – материальное обеспечение.
9.1. Литература:
а) обязательная
1. Попков В.А., Пузаков С.А. Общая химия. М.: ГЭОТАР-МЕДИА, 2007,с. 35-45.
2.Общая и неорганическая химия А.В. Бабков, Т.И. Барабанова, В.А. Попков. учебник М.: ГЭОТАР-Медиа, 2014. - 384 с. .
3. Общая химия А.В. Жолнин; под. ред. В.А. Попкова, А.В. Жолнина. учебник М.:ГЭОТАР-Медиа, 2014.-400 с.:ил.
4.Сборник задач и упражнений по общей химии С.А. Пузаков, В.А. Попков, А.А. Филиппова. учеб. пособие для вузов 5-е изд.-М.:Юрайт,2013.-255, [1] с.:ил.-(Бакалавр. Базовый курс)..
5. Практикум по общей и биоорганической химии [И.Н. Аверцева, О.В. Нестерова, В.А. Попков и др.]; под ред. В.А. Попкова.- учеб. пособие для вузов 2-е изд., испр.-М.:Академия,2007.-240 с.:ил
б) дополнительная
1. Пузаков С.А. Химия. – М.: ГЭОТАР-МЕДИА, 2006,с.32-44.
2.Химия. Теоретические основы. Вопросы. Тесты. Задачи с решениями: Тюрина, Е.Ф. учеб. пособие для медвузов ВГМУ.-2-е изд., перераб. и доп.-Владивосток: Медицина ДВ,2008.-248 с..
3. Общая химия А. В. Жолнин ; под ред. В. А. Попкова, А. В. Жолнина. - М.: учебник ГЭОТАР-Медиа, 2012. - 400 с.: ил. (ЭБС)
4. Химия С.А. Пузаков учебник -е изд., испр. и доп..-М.: ГЭОТАР-Медиа, 2006.-640 с.(ЭБС)
5. Общая химия В.А. Попков, С.А. Пузаков учебник для вузов М.: ГЭОТАР-Медиа, 2010.-976 с.:ил. (ЭБС)
6.интернет-ресурсы:
http://www.studmedlib.ru
http://www.books-up.ru
10. Материальное обеспечение:
а) наглядные пособия – Периодическая система элементов Д.И. Менделеева;
б) оборудование – мешалка магнитная, весы электронные, установка для определения ΔΗ растворения соли, набор химической посуды;
в) технические средства обучения – компьютер с обучающей программой «Measure», калькулятор.
Оценивание уровня сформированности компетенций обучающихся проводится по балльно-рейтинговой системе.
Приложение
Термодинамические свойства некоторых элементов, неорганических и органических соединений в стандартных условиях
| Соединение | ΔΗ0обр., кДж/моль |
| Н2S (газ) | -20,0 |
| H2O (жидк.) | -286,0 |
| H2SO4 (жидк.) | -814,0 |
| C2H5OH (жидк.) | -277,63 |
| CO2 (газ) | -393,51 |
| C6H12O6 (твёрд.) | -1260,0 |
| Соединение | ΔΗ0сгор.., кДж/моль |
| С2Н5ОН (жидк.) | - 1371,0 |
| (С2Н5)2О (жидк.) | -2733,0 |
