Методы очистки органических соединений
РАЗДЕЛЕНИЕ ЖИДКОСТЕЙ МЕТОДОМ ПЕРЕГОНКИ /I/
Работа начата 6.02.03
На каких физических закономерностях основан этот метод очистки ?
Получено 25 мл смеси уксусно-этилового и бензойно-этилового эфиров
Таблица I - Константы соединений
| Название и структурная формула соединения | Молекулярная масса | Тпл., оС | Ткип., оС | Плотность, г/см3 | Показатель преломления | Растворимость | Примечание (токсичность) | Ссылка на литературные источники |
| Уксусно-этиловый эфир СН3СООС2Н5 | 88,11 | -82,4 | 77,15 | 0,901 | 1,3723 | В воде 8,0825 бз., эт. | Обладает наркотическим действием, раздражает слизистую оболочку | 2, с.500 3, с.360 |
| Бензойно-этиловый эфир С6Н5СООС2Н5 | 150,18 | -34,7 | 212,4 | 1,01515 | 1,5051 | В воде 0,1 | -"- | 2, с.500 3, с.46 |
Посуда и оборудование:
1. Колба перегонная (колба Вюрца) вместимостью 100 мл
2. Термометр химический от 0 до 250 оС
3. Холодильник прямой водяной
4. Холодильник прямой воздушный
Аллонж
6. Приемник вместимостью 50 мл – З шт.
7. Баня водяная
8. Плитка электрическая
СХЕМЫ ПРИБОРОВ
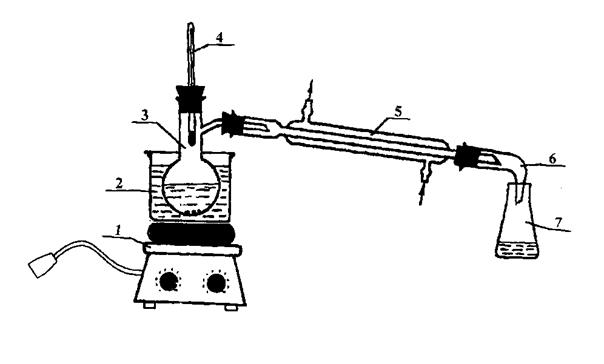
1 - плитка; 2 - водяная баня; 3 - перегонная колба (колба Вюрца); 4 - химический термометр; 5 - прямой водяной холодильник; 6 - аллонж; 7 - приемник
Рисунок 1 - Прибор для перегонки уксусно-этилового эфира
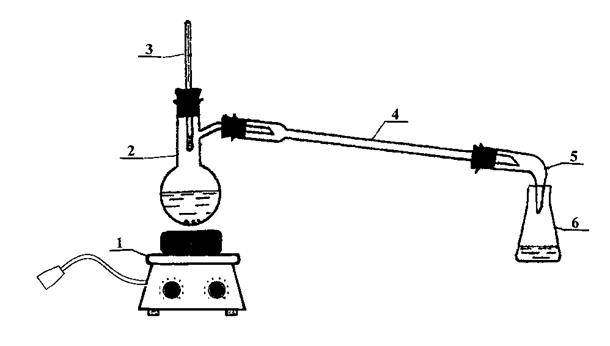
1 - плитка; 2 - перегонная колба; 3 - химический термометр; 4 - прямой воздушный холодильник; 5 - аллонж; 6 - приемник
Рисунок 2 - Прибор для перегонки бензойно-этилового эфира
Таблица 2 - Описание работы
| Ход работы | Наблюдения, объяснения |
| Собираю прибор (рис.1) с приемником для промежуточной фракции. Используя колбу Вюрца, т.к. разность между температурами кипения перегоняемых жидкостей больше 80 оС. Первая фракции кипит при температуре ниже 100 °С, поэтому в качестве нагревателя использую водяную баню. В перегонную колбу вливаю смеси, бросаю кусочки битого фарфора для равномерного кипения. При температуре смеси, меньшей на 5 оС температуры кипения уксусно-этилового эфира (72 оС), подставляю взвешенный приемник для первой фракции (приемник I). Подставляю приемник для промежуточной фракции. Убираю водяную баню, обтираю колбу, подставляю плитку. При температуре 130 оС отставляю плитку. Заменяю водяной холодильник на воздушный. Вновь подставляю плитку. При температуре смеси меньшей на 5 оС температуры кипения бензойно-этилового эфира (207 оС), подставляю взвешенный приемник для второй фракции (приемник 2). Нагревание заканчиваю. Определяю показатели преломления первой и второй фракции. | При температуре 76 оС в приемник начинают поступать первые капли уксусно-этилового эфира. При температуре 78 оС капли стали редкими, температура упала. Это означает, что перегонка первой фракции закончена. Температурой кипения является интервал температур, в котором собирали фракцию, т.е. 76-78 оС. При температуре 208 оС начинает собираться вторая фракция. В перегонной колбе остается немного жидкости(с поверхностью с двухрублевую монету). Отмечаю температуру смеси 211 оС. Температура кипения второй фракции 208-211 оС. |
Таблица 3 - Результаты работы
| Название соединений | Масса | Ткип., оС | Показатель преломления |
| I фракция – уксусно-этиловый эфир | 7,3 | 76 - 78 | 1,3740 |
| II фракция – бензойно-этиловый эфир | 12,2 | 208 - 211 | 1.5072 |
Работа окончена 6.02.03
РАБОТА № 2
МЕТОДЫ ОЧИСТКИ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ КРИСТАЛЛИЗАция /I/
Работа начата 13.02.03
На каких физических закономерностях основан этот метод очистки?
Получено: 4г бензанилида
20 мл этанола
Таблица I - Константы соединений
| Название и структурная формула соединения | Молекулярная масса | Тпл., оС | Ткип., оС | Плотность, г/см3 | Показатель преломления | Растворимость | Примечание (токсичность) | Ссылка на литературные источники |
| Бензанилид, N-фенилбензамид C6H5CONHC6H5 | 197,2 | 117-119 (1,33 кПа) | 1,31 | сп., э., бз. | - | 2, с.418 | ||
| Этанол С2Н5ОН | 46,1 | -113,3 | 78,5 | 0,7893 | 1,3611 | Х: в, эф., ац., хлф., укс., р: бз | Наркотик, ПДК 1 мг/дм3, пожароопасен | 3, с. 439 |
Посуда, оборудование, реактивы
1. Колба круглодонная вместимостью 100 мл
2. Холодильник обратный водяной
3. Воронка для горячего филътрования
4. Воронка химическая
5. Стакан вместимостью 50 мл
6. Колба Бунзена
7. Воронка Бюхнера
8. Баня водяная
9. Плитка
10. Палочка стеклянная
11. Фильтровальная бумага
12. Уголь активированный
СХЕМЫ ПРИБОРОВ
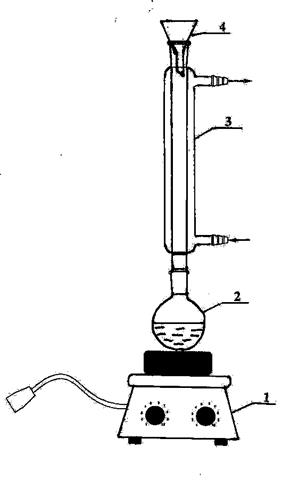
I – плитка; 2 – круглодонная колба; 2- обратный водяной холодильник; 4 – коническая воронка
Рисунок 1 - Прибор для перекристаллизации
I- воронка для горячего фильтрования; 2 - химическая воронка;
3 – фильтр; 4 - стакан
Рисунок 2 - Прибор для горячего фильтрования
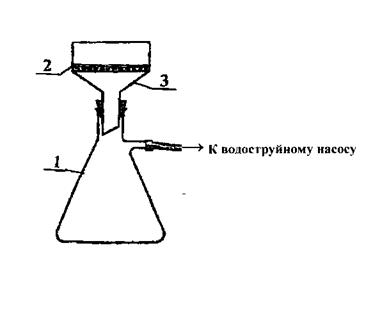
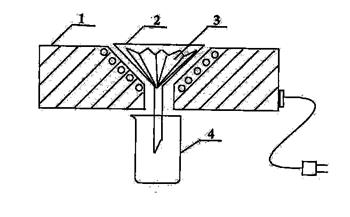
I - колба Бунзена; 2 - двухслойный фильтр размером, равным внутреннему диаметру воронки Бюхнера; 3 - воронка Бюхнера;
Рисунок 3 - Прибор для отделения осадка (нутч-фильтр)
Таблица 2 - Описание работы
| Ход работы | Наблюдения, объяснения |
| Собираю прибор (рис.1), в качестве нагревателя использую водяную баню. В колбу помещаю бензанилид, добавляю такое количество этилового спирта, чтобы он смочил продукт. Довожу жидкость в колбе до кипения Добавляю 5 мл спирта через обратный холодильник, опять довожу раствор до кипения. Добавляю еще 5 мл спирта, довожу раствор до кипения. Убираю нагреватель, даю смеси немного остыть и осторожно (чтобы . не было вспенивания) добавляю активированный уголь в количестве 1/20 от массы взятого для кристаллизации вещества. Вновь нагреваю до кипения. Отставляю нагреватель, заворачиваю колбу в полотенце и под тягой фильтрую по горячему. Ставлю стаканчик в снег на 40 минут. Маточным раствором смачиваю фильтр, включаю насос. Осадок бензанилида помещаю на фильтр. После отсасывания осадок отжимаю стеклянной палочкой-шпателем. Отсоединяю насос, смачиваю осадок охлажденным в снегу этиловым спиртом. Подсоединяю насос, отсасываю растворитель досуха. Промытый осадок снимаю с фильтра (не вынимая фильтр из воронки), оставляю сушиться до следующего занятия. Определяю температуру плавления, используя прибор с глицерином. | Температура кипения растворителя ниже 100 оС. Спирт кипит, осадок уменьшился, но не растворился. Количество осадка уменьшилось. Количество осадка остается неизменным, следовательно, это нерастворимая примесь. В стакане сразу появляются кристаллы. Выпадает обильный осадок. Фильтр должен плотно прилегать ко дну воронки Бюхнера. Маточный раствор перестал капать. . Весь осадок равномерно смочен жидкостью Высушенный осадок белого цвета мелкокристаллический, сыпучий. |
Результата работы:
масса бензанилида 2 г (50% от исходного). Тпл 64 - 67 °С.
Работа окончена 20.02.03
ОБРАЗЕЦ ОФОРМЛЕНИЯ РАБОты
Работа № 3
ДИАЗОТИРОВАНИЕ
СИНТЕЗ ИОДБЕЗНЗОЛА ИЗ АНИЛИНА /5/
Работа начата 3.02.03
Реакции получения целевого продукта:
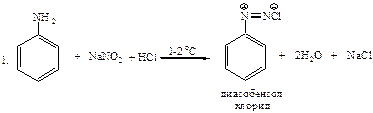
Механизм:

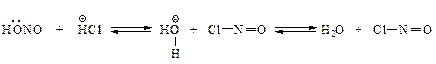
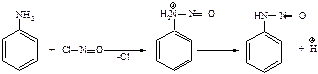
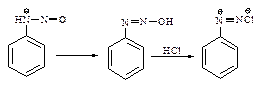
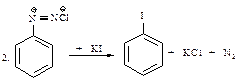
Побочные реакции:
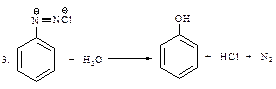
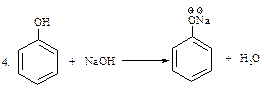
Количество реактивов по руководству:
Анилин 0,1 моль (9.3 г; 7,6 мл)
Соляная кислота ( 1,19) 25 мл
Натрий азотистокислый 0,11 моль (8 г)
Калий иодистый 0,12 моль (20 г)
Кальций хлористый
Натрия гидроксид
Эфир этиловый
Таблица 1 - Стехиометрический расчет
| Соотношения количеств реагентов и продукта в молях | С6Н5NH2 | NaNO2 | KI | C6H5I |
| по уравнению | ||||
| по руководству | 0,1 | 0,11 | 0,12 | 0.1 |
Теоретический выход продукта в молях эквивалентен количеству анилина - реагента, взятого в недостатке, - 0,1 моль, что составляет 204 х 0,1 = 20,4 г.
Таблица 2 - Константы исходных веществ
| Название и структурная формула соединения | Молекулярная масса | Тпл., оС | Ткип., оС | Плотность, г/см3 | Показатель преломления | Растворимость | Примечание (токсичность) | Ссылка на литературные источники |
| Анилин С6Н5NH2 | 93,2 | -6,2 | 184,4 | 1,022 | 1,5863 | в воде 3,618 сп., э., бз. | Отравление при вдыхании и попадании на кожу ПДК = 0,1 мг/л | 2, с.414 |
| Натрий азотистокислый NaNO2 | 69,00 | Разл. | 2,168 | 1,3611 | В воде 82,928 16068 | 2, с. 144 | ||
| Калий иодистый КI | 166,01 | 680-686 | 3,13 | В воде 127,80 206,4100 | 2, с. 144 | |||
| Кальций хлористый | 110,99 | 2,51225 | В воде 127,800 206,4100 | 2, с. 86 | ||||
| Эфир этиловый | 74,12 | -117,6 | 35,6 | 0,714 | 1,354217 | Сп., хл., бз., в воде 6,59 | наркотик ПДК = 0,3 мг/л взрывоопасен | 2, с. 480 |
Посуда и оборудование
1. Стакан фарфоровый вместимостью 250 мл
2. Термометр технический от 0 до 50 оС
3. Воронка капельная вместимостью 50 мл
4. Колба круглодонная вместимостью 1000 мл
5. Холодильник с водяной рубашкой
6. Приемник вместимостью 250 мл
7. Приемник вместимостью 100 мл(2 шт)
8. Воронка делительная вместимостью 250 мл
9. Воронка химическая
10. Колба перегонная вместимостью 100 мл
11. Термометр химический от 0 до 250 оС
12. Палочка стеклянная
13. Трубка для перегонки с парой
14. Баня водяная
15. Электроплитка
СХЕМЫ ОСНОВНЫХ ПРИБОРОВ
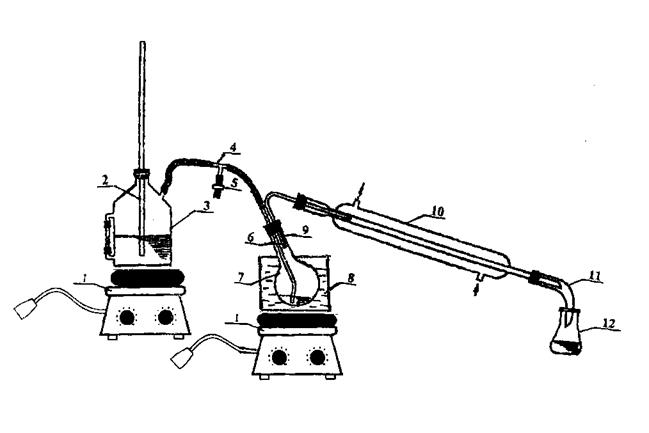
1 – плитка; 2 – предохранительная трубка; 3 - парообразователъ; 4 – тройник; 5 – винтовой зажим; 6 – трубка по которой поступает пар; 7 - перегонная колба; 8 – водяная баня; 9 – пароотводная трубка; 10 - холодильник; 11 – аллонж; 12 - приемник.
Рисунок 1- Прибор для перегонки с водяным паром
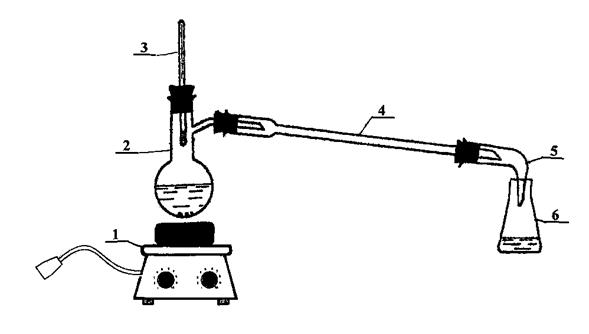
1 - плитка; 2 - перегонная колба; 3 - химический термометр; 4 - прямой воздушный холодильник; 5 - аллонж; 6 - приемник
Рисунок 2 - Прибор для перегонки иодбензола
Таблица 3 - Описание хода синтеза
| Ход синтеза | Наблюдения, объяснения |
| I этап: реакция диазотирования В фарфоровом стакане вме-стимостью 250 мл смешиваю 25 мл конц. соляной кислоты с 25 мл воды и к раствору прибавляю 7,6 мл анилина. Раствор охлаждаю до 1-2 °С добавляю из капельной воронки при непрерывном перемешивании раствор 8 г нитрита натрия в 20 мл воды. Добавление нитрита натрия следует вести с такой скоростью, чтобы температура не поднималась выше 8 °С. Через 10 мин после окончания добавления раствора азотистокислого натрия делаю пробу на присутствие свободной азотистой кислоты. II этап: превращение соли диазония в иодбензол. Раствор соли диазония смешиваю в круглодонной колбе вместимостью 500 мл с раствором 20 г йодистого калия в 30 мл воды и оставляю в ледяной бане. Ш этап: отгонка иодбензола с водяным паром. Раствор подщелачиваю конц. раствором гидроксида натрия до сильно-щелочной реакции (рН=10). Иодбензол отгоняю с водяным паром. IV этап: экстракция и осушка Иодбенол отделяю, водный раствор дважды экстрагирую эфиром порциями по 20 мл. Иодбензол соединяю с эфирными вытяжками, сушу хлористым кальцием. V этап: перегонка иодбензола Фильтрую под тягой осушенный эфирный раствор в перегонную колбу. Отгоняю на водяной бане с холодильником эфир, меняю холодильник на воздушный и на плитке отгоняю иодбензол (рис. 2). | Происходит реакция диазотирования 1. Никаких видимых изменений в реакционной смеси не наблюдаю. Иодкрахмальная бумажка не синеет, значит свободной азотистой кислоты в смеси нет. Диазотирование закончено. Раствор азотистокислого натрия прикапывал в течение 40 мин. Происходят реакции 2 и 3. Образуются темно-вишневые маслянистые капли. Смесь стояла в ледяной бане 1,5 часа. После этого работу прекращаю на неделю. Происходит реакция 4, фенолят (ионное соединение) с водяным паром не перегоняется. Тяжелые маслянистые капли собираются на дне приемника. Растворений в воде иодбензол переходит в эфир, эфирный слой окрашивается в желтый цвет. Раствор становится прозрачным. Иодбензол отгонялся в интервале 184-189 °С, продукт представляет собой темно-красную жидкость с резким неприятным запахом. |
Выход иодбензола – 12 г
Расчет выхода в процентах от теоретического:
| 20,4 г - 100% 12 г - X | 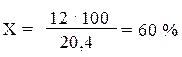 |
Расчет выхода от указанного в методике:
| 16 г - 100% 12 г - У | 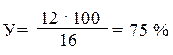 |
Таблица 4 - Константы иодбензола
| Название и структурная формула | Молекулярная масса | Константы | Плотность, г/см3 | Тпл., оС | Ткип., оС | Показатель преломления | Растворимость | Примечание (токсичность) | Ссылка на литературные источники |
Иодбензол 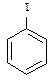 | 204,5 | Литературные | 1,83815 | 31,4 | 138,7 | 1,621318 | в воде, сп., э., хл. | Наркотик оказывает влияние на кроветворение, может вызвать экзему | 2, с. 433 |
| Полученные | - | - | 184-189 | 1,622920 |
Работа окончена 20.02.03
Список использованных иСТОЧников
1. Лабораторные работы по органической химии. / Под ред. С.Ф.Гинзбурга, А.А. Петрова. - М.: Высшая школа, 1967. - 295 с.
2. Гороновский, И.Т. Краткий справочник по химии / И.Т. Гороновский, Ю.П. Назаренко, Е.Ф. Некряч. - 4-е изд., испр. и доп. - Киев: Наукова думка, 1974. -992 с.
3. Свойства органических соединений. Справочник. / Под ред. А.А. Потехина.- .Л.: Химия, 1984. - 520-с.
4. Вредные вещества в промышленности. / Под ред. Н.В.Лазарева, Э. Н. Левиной. -Л.: Химия, 1976. -т .1-3.
5. Методические указания к лабораторному практикуму по органической химии для студентов химико-технологического факультета. Ч. I / Р.М. Басаев, И.С. Колпащикова, Е.Р. Кофанов, Т.А. Обухова - Ярославль: Яросл. гос. тех. ун-т, 1999. - 32 с.
ОПРЕДЕЛЕНИЕ ТЕМПЕРАТУРЫ ПЛАВЛЕНИЯ ТВЕРДОГО ВЕЩЕСТВА
Температура, выше которой кристаллическое органическое вещество превращается в жидкость, называется температурой плавления. Температура плавления является физической константой и используется в качестве критерия чистоты твердых веществ. Чистое вещество плавится резко при определенной температуре. Наличие в веществе примесей или влаги приводит к понижению температуры
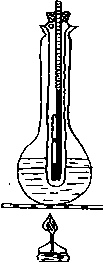 | плавления, Прибор для определения температуры плавления изображен на рисунке. Для веществ с температурой плавления выше 250 °С используется прибор, не содержащий жидкого теплоносителя. Вещество, температуру плавления которого надо определить, помещают в капилляр, запаянный с нижнего конца. Кусочки капилляров нужного диаметра запаивают с одного конца, осторожно внося их сбоку в пламя горелки. Капилляр наполняют веществом так, чтобы плотный слой его занимал около 0,5 см. Для этого небольшое количество вещества мелко измельчают на часовом стекле, собирают |
его в кучку и погружают в нее открытый конец капилляра. Сместить это вещество вниз к запаянному концу и утрамбовать его можно, бросая капилляр с веществом запаянным концом вниз в стеклянную трубку длиной 50-60 см. Заполненный капилляр прикрепляют посредством резинового кольца к термометру на уровне ртутного шарика так, чтобы было видно одновременно и шкалу термометра и содержимое капилляра на просвет. Прибор нагревают на спиртовке сначала быстро, а когда показания термометра достигнут величины на 10-15 °С ниже предполагаемой температуры плавления, нагрев уменьшают. За начало плавления принимают начало уменьшения высоты столбика вещества в капилляре, за конец плавления - момент полного расплавления вещества с превращением его в прозрачную жидкость. Интервал температур между началом плавления и его окончанием тем, меньше, чем чище вещество. Считается допустимым интервал плавления 1-2 °С.
