Общие закономерности реакционной способности важнейших классов органических соединений
Классификация реакций органических соединений
Для классификации органических реакций используют следующие принципы:
· характер изменения связей в реагирующих веществах (способ разрыва связи);
· направление реакции;
· число молекул, принимающих участие в стадии, определяющей скорость реакции.
Схема 3. Классификация химических реакций
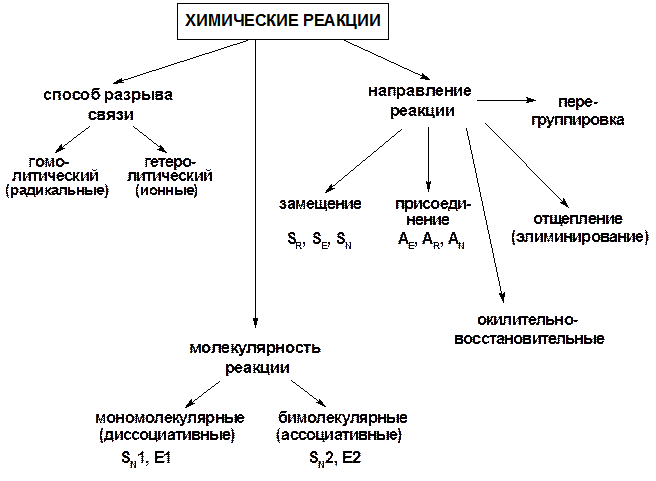


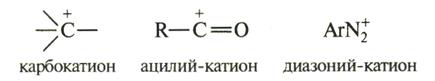
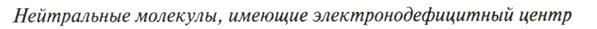
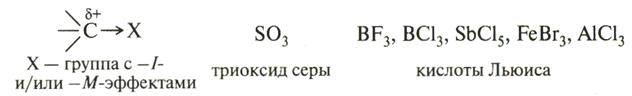


а) 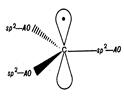 б)
б) 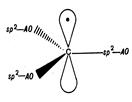 в)
в) 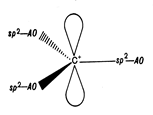
Рис. 10. Электронное и пространственное строение свободного
Радикала (а), карбоаниона (б) и карбокатиона (в).
Минимальное количество энергии, необходимое для осуществления реакции, называется энергией активации (Еа). Чем меньше энергия активации, тем выше скорость реакции и, наоборот, чем выше энергетический барьер, тем медленнее протекает реакция. Использование катализаторов существенно понижает энергию активации, направляя реакцию по другому пути через образование новых, более стабильных промежуточных соединений (рис. 11) .
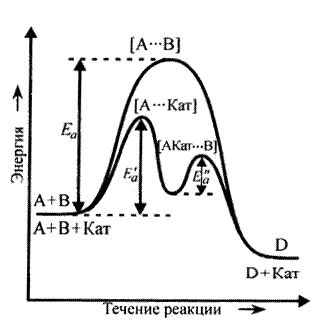 |
Рис. 11. Энергетические диаграммы реакции
Без катализатора и с катализатором
II. РЕАКЦИОННАЯ СПОСОБНОСТЬ ОСНОВНЫХ
КЛАССОВ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
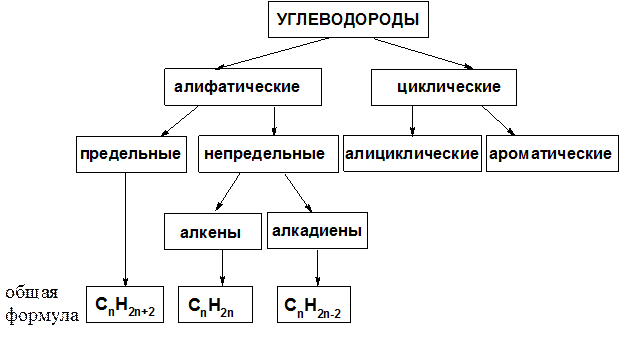
УГЛЕВОДОРОДЫ
Схема 4. Классификация углеводородов
| тип связи | одинарная | двойная | две двойные | делокализованное π-электронное облако | |
| длина связи, нм | 0,154 | 0,133 | σ – 0,146 π – 0,136 | ||
| энергия связи, кДЖ/моль | 150* | ||||
| вид гибридизации атомных орбиталей | sp3 | sp2 | sp2 | sp2 | |
| тип химических реакций | SR | AE | AE | SE |
* – энергия сопряжения
Таблица 8. Важнейшие насыщенные алифатические
Углеводороды (алканы)
| а) с неразветвлённой цепью | б) с разветвлённой цепью | ||
| Формула | Название | Формула | Название |
| СН4 | метан | 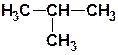 | 2-метил-пропан (изобутан) |
| С2Н6 | этан | ||
| С3Н8 | пропан | 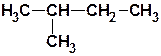 | 2-метилбутан (изопентан) |
| С4Н10 | бутан | ||
| С5Н12 | пентан | 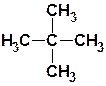 | 2,2-диметил-пропан (неопентан ) |
| С6Н14 | гексан | ||
| С7Н16 | гептан | ||
| С8Н18 | октан | 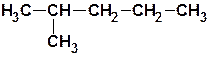 | 2-метил-пентан (изогексан) |
| С9Н20 | нонан | ||
| С10Н22 | декан | ||
| в) циклические | |||
| Формула | Название | ||
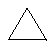 | 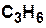 | циклопропан | |
 | 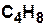 | циклобутан | |
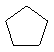 | 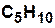 | циклопентан | |
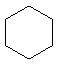 | 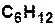 | циклогексан | |
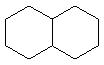 | 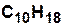 | декалин |
Реакционная способность алканов (SR)
Насыщенность, низкая полярность и слабая поляризуемость связей определяют высокую инертность углеводородов в химических реакциях. Для алканов характерны реакции радикального замещения (SR).
1. Механизм реакции радикального замещения:
а) инициирование
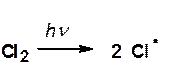
б) рост цепи
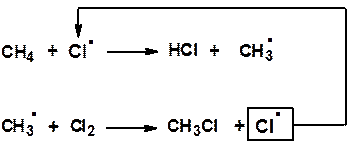
Такие процессы называют цепными, т.к. образовавшийся первоначально один радикал может инициировать хлорирование многих молекул метана.
в) обрыв цепи
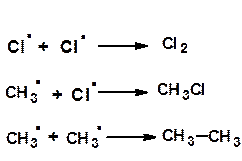
Региоселективность реакций радикального замещения
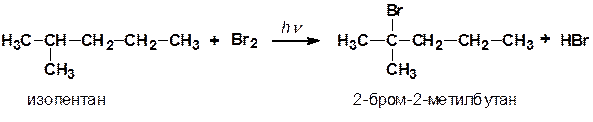
Реакция протекает по правилу Марковникова (в реакциях радикального замещения алканов c бромом легче идёт замещение у третичного, затем у вторичного и в последнюю очередь у первичного атома углерода).
