Определение концентрации хлорида железа (III)
Солянокислые растворы хлорида железа широко используются для химического травления различных металлов, сплавов и полупроводников, например, при производстве печатных плат для травления меди, в тонкопленочной технологии для растворения тонких пленок меди, алюминия, хрома, нихрома и других, в полупроводниковой технике для травления антимонида индия и т.д. Непрерывное определение концентрации хлорида железа в травильных растворах имеет большое практическое значение для корректировки состава этих растворов. Быстрое и надежное определение концентрации Fe3+ в присутствии ионов Cu2+, образующихся в процессе травления медных покрытий, можно приводить потенциометрическим титрованием.
Определение проводят титрованием слабого солянокислого испытуемого раствора (рН ~ 2) стандартным раствором аскорбиновой кислоты. За изменением потенциала индикаторного платинового электрода следят, измеряя ЭДС гальванического элемента и используя в качестве электрода сравнения насыщенный хлоридсеребряный электрод. Аскорбиновая кислота С6Н8О6,. стандартные растворы которой характеризуются высокой устойчивостью, является достаточно сильным восстановителем. В процессе титрования раствора железа аскорбиновой кислотой протекает химическая реакция, которая описывается уравнением:
2Fe3+ + C6H8O6 = 2Fe2+ + C6H6O6 + 2H+
В то же время медь (П) не восстанавливается аскорбиновой кислотой в условиях титрования железа (Ш). Титрование целесообразно проводить при нагревании, так как основная реакция характеризуется малой скоростью.
Электрохимическими реакциями при титровании являются следующие.
1) до точки эквивалентности:
Fe3+ + ē = Fe2+
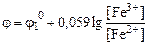 ;
;
2) после точки эквивалентности:
С6Н6О6 + 2Н+ + 2ē D С6Н8О6
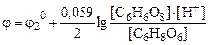 .
.
Из-за достаточной разности величин стандартных потенциалов (φ1º=+ 0.77 В и φ2º= + 0.18 В) в конечной точке титрования наблюдается довольно резкий скачок потенциала.
Оборудование и реактивы
Иономер.
Индикаторный электрод, платиновый.
Электрод сравнения хлоридсеребряный
Аскорбиновая кислота, 0,05000 М раствор.
Аммиак,10%-ный раствор.
Соляная кислота, раствор (1:1).

 Описание определения
Описание определения
В стакан емкостью 100-150 мл переносят 10,00 мл анализируемого раствора, прибавляют по каплям 10%-ный раствор аммиака до появления первой неисчезающей при перемешивании мути и затем 4-6 капель раствора соляной кислоты (1:1) разбавляют 50-100 мл дистиллированной воды.
В подготовленный таким образом раствор погружают два электрода: платиновый и хлоридсеребряный.
Бюретку заполняют титрантом – рабочим раствором аскорбиновой кислоты и подготавливают к работе.
Анализируемый раствор титруют при перемешивании ориентировочно по
1 мл стандартным раствором аскорбиновой кислоты. Затем титруют новую порцию анализируемого раствора, прибавляя раствор титранта в области скачка потенциала по 2-3 капли. Величины ЭДС цепи фиксируют при достижении их постоянного значения: изменение ЭДС в течение одной минуты не должно превышать ~5 мВ.
Результаты измерений и расчетов представляют в форме табл.15.2 и графически в координатах E – V и (ΔE/ΔV) – V. Вычисляют содержание железа (Ш) в граммах в исследуемом растворе по формуле:
m(Fe3+), г = (VN)аск.к.·Э(Fe3+)·n·10–3,.
где (VN)аск.к – объем и нормальная концентрация раствора аскорбиновой кислоты;
Э(Fe3+) – эквивалент железа (III), равный 55,85;
n – число аликвотных частей анализируемого раствора.
