Большое каноническое распределение
Рассматривается идеальный газ с 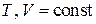 , обменивающийся энергией и частицами с термостатом. Распределение дает вероятность того, что система имеет N частиц и находится в элементе объема
, обменивающийся энергией и частицами с термостатом. Распределение дает вероятность того, что система имеет N частиц и находится в элементе объема 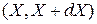 фазового пространства.
фазового пространства.
Распределение микросостояний по фазовому пространству
При 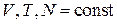 система описывается каноническим распределением (2.16)
система описывается каноническим распределением (2.16)
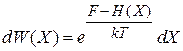 .
.
Свободная энергия F зависит от числа частиц. Выражаем ее через W-потенциал, не зависящий от N, используя (2.68)
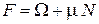 .
.
Получаем большое каноническое распределение –вероятность для системы иметь N частиц и находиться в элементе объема 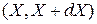 фазового пространства
фазового пространства
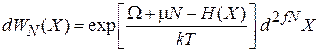 . (2.70)
. (2.70)
Интеграл состояния
В условие нормировки
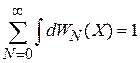
подставляем (2.70)
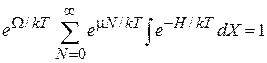 .
.
Определяем интеграл состояния большого распределения
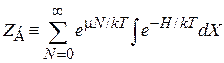 . (2.71)
. (2.71)
Условие нормировки дает
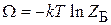 .(2.72)
.(2.72)
Используем статистический интеграл канонического распределения (2.17)
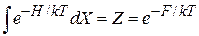 .
.
Из (2.71) получаем связь между Z и ZБ
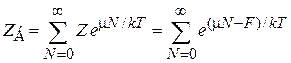 . (2.73)
. (2.73)
Для газа из N одинаковых частиц
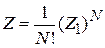 ,
,
тогда
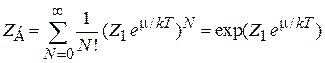 ,
,
где использовано разложение экспоненты в степенной ряд
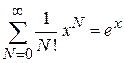 .
.
Учитывая активность (2.62б)
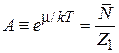 ,
,
получаем
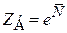 . (2.74)
. (2.74)
Статистический интеграл большого канонического распределения равен экспоненте от среднего числа частиц системы.
Из (2.69а), (2.72), и (2.74) получаем омега-потенциал и уравнение состояния
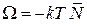 , (2.74а)
, (2.74а)
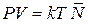 . (2.74б)
. (2.74б)
Уравнение (2.74б) является обобщением уравнения Менделеева–Клапейрона на идеальный газ с переменным числом частиц.
Большое каноническое распределение
Используем (2.70) и (2.72)
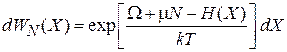 ,
,
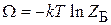 ,
,
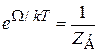 ,
,
получаем
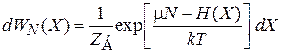 . (2.75)
. (2.75)
Вероятность появления N частиц в системе
Интегрируем (2.75) по фазовому пространству и находим вероятность N частиц в системе
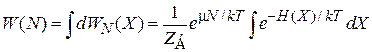 .
.
С учетом (2.17)
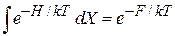
вероятность появления N частиц в системе
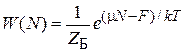 . (2.76)
. (2.76)
Согласно (2.73)
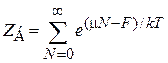
вероятность (2.76) удовлетворяет условию нормировки
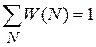 .
.
Термодинамические характеристики системы
Из определения омега-потенциала получены соотношения (2.69)
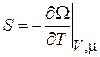 ,
,
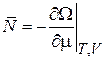 ,
,
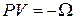 .
.
Подставляем (2.72) и (2.74)
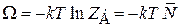 ,
,
находим
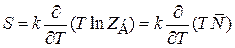 , (2.77)
, (2.77)
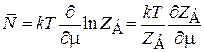 . (2.78)
. (2.78)
Физический смысл (2.78)
С учетом (2.73) и (2.76)
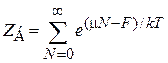 ,
,
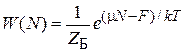 ,
,
выражение (2.78) сводится к определению среднего числа частиц
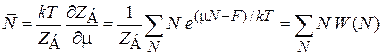 .
.
ПРИМЕРЫ
Вывод формулы Больцмана
Получим формулу Больцмана (2.76)
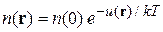
из условия термодинамического равновесия.
Используем химический потенциал (2.62а) идеального газа атомов, совершающих поступательные движения:
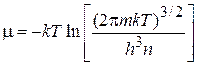 ,
,
и электрохимический потенциал (2.59)
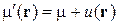 ,
,
где 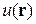 – потенциальная энергия частицы в точке
– потенциальная энергия частицы в точке 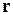 , тогда
, тогда
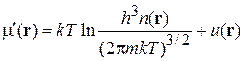 .
.
При 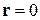 полагаем
полагаем 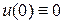 и получаем электрохимический потенциал в начале координат
и получаем электрохимический потенциал в начале координат
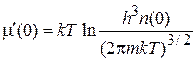 .
.
При термодинамическом равновесии химический потенциал одинаков во всех точках системы согласно (2.60)
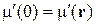 ,
,
тогда
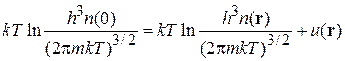 ,
,
получаем
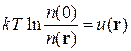 .
.
Откуда следует формула Больцмана
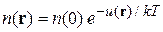 . (П.7.12)
. (П.7.12)
