История поиска биологически активных веществ. Формирование представлений о биологической активности веществ. 4 страница
Описаны также и другие виды конъюгации (например, фосфатная конъюгация, реакция ксенобиотиков с глицинтаурином и формилом).
Дегалогенирование. К хлорсодержащим ксенобиотикам относятся многие персистентные поллютанты, в том числе пестициды, а также ряд природных метаболитов низших растений.
Можно выделить следующие виды реакций дегалогенирования:
1гидролитическоедегалогенирование(хлорированных алифатических кислот, при деградации ароматических пестицидов). Например, гербицид 2,4-Д деградируется почвенными бактериями с участием реакции этого типа;
2восстановительное дегалогенированиеэто реакция замещения атома галоида на водород. Многие бактерии, грибы, водоросли таким образом трансформируют ДДТ в ДДД. Могут образоваться интермедиаты, токсичные для клеток.
3Окислительное дегалогенирование.Реакции этого типа подразделяются на: дегидрогалогенирование (при метаболизме ДДТ); окислительноедегалогенирование с образованием двойной связи; дегалогенирование - гидроксилирование с участием молекулярного кислорода.
24. Факторы, влияющие на метаболизм ксенобиотиков. Эти факторы могут быть:
-генетическими— относятся видовые различия и различия внутри одного вида.
-физиологическими,которые влияют на метаболизм — относятся возраст, пол, состояние питания, заболевания и т. д.
-факторы окружающей среды:стресс из-за неблагоприятных условий, облучение ионизирующей радиацией, окислительно-восстановительный потенциал (ОВП), наличие других ксенобиотиков.
-природа (структура)ксенобиотиков.
Так, неблагоприятные внешние условия приводят к увеличению микросомального окисления, а ионизирующая радиация вызывает угнетение гидроксилирования стероидов. Хорошо известно активирование метаболизма чужеродных соединений введением других ксенобиотиков - медикаментов, пестицидов и полициклических углеводородов (явление лекарственного синергизма и толерантности, индукция ферментов и канцерогенезу).Известен ряд лекарственных препаратов, которые подавляют микросомальный метаболизм ксенобиотиков, продлевая тем самым действие многих лекарств.
Имеется много данных по зависимости скорости метаболических превращений от природы вещества. Многие из ароматических углеводородов содержатся в сырой нефти и каменном дегте, некоторые известны как канцерогены. Основная реакция в их метаболических превращениях - это реакция гидроксилирования (сопровождается введением молекулы воды, образуются дигидролы). Даже для ряда близких по структуре многоядерных углеводородов скорость метаболизма изменяется более чем в двадцать раз.
У некоторых соединений (например, 1,1-дихлорэтан, 1,1-дихлорпропан и 1,1,2-трихлорпропан) дехлорирование протекает очень легко, тогда как другие вещества очень устойчивы к этому превращению. Скорость реакции дехлорирования повышается, если хлорированный атом связан с одним атомом водорода.Экспериментальные данные показывают, что родственные вещества метаболизируются оксидазой микросом печени крыс, обладающей смешанной функцией, с разной скоростью. Такие изменения активности обусловлены ограниченной доступностью активных мест на поверхности фермента и стериохимическими свойствами субстрата.
На скорость реакции могут влиять изменения плотности электронов в молекуле субстрата, вызываемые различными заместителями.
25. Механизмы детоксикацииксенобиотиков (общие положения). Вещества, связывающие металлы. В наиболее типичном варианте система защиты от самых разных ксенобиотиков представлена трехэтапным процессом, включающим фазы: 1) активации ксенобиотиков, 2) нейтрализации ксенобиотиков, 3) выведение ксенобиотиков из организма. Биотрансфармацияксенобиотиков играет ключевую роль в механизмах адаптации организма к факторам внешней среды. Она включает три последовательные и функционально сопряженные фазы, которые осуществляются за счет активности более 200 различных ферментов. Каждому индивидууму свойственна уникальная конфигурация генов, ответственных за синтез ферментов системы биотрансформации, и, соответственно, уникальную реакцию каждого человека на повреждающие действие, как факторов внешней среды, так и эндогенных факторов. Причиной фенотипических различий является полиморфизм соответствующих генов.
Сначала поступающие в организм чужеродные соединения (канцерогены, лекарства, промышленныя яды и пр.) активируются с помощью ферментов семейства цитохромов Р450 или микросомальныхэпоксид-гидролаз (тЕРОХ) , образуя короткоживущие промежуточные электро-фильные метаболиты, которые обладают генотоксическими свойствами. В процессе первой фазы нередко происходит активация гидрофобных ксенобиотиков с образованием активных промежуточных электрофильных метаболитов, являющихся основным субстратом детоксикации системы ферментов второй фазы.
Главным назначением второй фазы является нейтрализация дезактивация, детоксикация гидрофильных и зачастую токсичных продуктов первой фазы при помощи различных гидролаз и трансфераз . Промежуточные метаболиты с помощью ферментов семейств глутатионтрансферазы (GSTM) , УДФ-глюкуронсульфотрансфераз (UDF) , N-ацетилтрансфераз (NAT) превращаются в водорастворимые нетоксические продукты и выводятся из организма. Ферменты второй фазы присутствуют во всех клетках, т. е. функционируют при любых путях поступления ксенобиотиков, осуществляют или завершают детоксикапию, а иногда исправляют ошибки первой фазы. Большинство этих ферментов находятся в гиалоплазме, часть из них локализована в мембранах эндоплазматическогоретикулума и митохондрий.
Наиболее эффективно система детоксикации функционирует при сопряженном, гармоничном действии ферментов первой и второй фазы. Де-синхронизация этих процессов ведет к быстрому отравлению организма в результате накопления продуктов перекисного окисления, различных канцерогенов, мутагенов и тератогенов.
В третьей фазе биотрасформации происходит выведение из организма продуктов детоксикации через легкие, почки, кишечник. Важная роль в этих процессах принадлежит белку плазмы крови - альбумину, который связывает и транспортирует метаболиты экзогенных и эндогенных субстратов, в том числе продукты первой и второй фаз детоксикации.
26. Металлы в живой клетке и их биоцидные эффекты.Живые организмы нуждаются в катионах металлов, обеспечивающих протекание многих жизненно важных процессов. Более того, многие из этих металлов необходимы для всех форм жизни. К ним относятся: а) тяжелые металлы (кобальт, медь, железо, марганец, молибден, цинк и в меньших количествах хром, ванадий, никель и свинец); б) легкие металлы, обычно встречающиеся в большом количестве (кальций, магний, калий и натрий).Медь, железо, молибден, кобальт и иногда марганец принимают участие в окислительно-восстановительных процессах; действие цинка, магния и марганца связано с процессами гидролиза и переноса групп; кальций играет наиболее важную роль при создании гибких или жестких структур, а также может инициировать реакцию, вызывая по- видимому, структурные изменения (подобное действие иногда проявляет и магний), является вторичным мессенджером. Натрий и калий, благодаря их распространенности, служат переносчиками заряда; они очень слабо связываются и поэтому могут быстро обмениваться.Когда речь идет о тяжелых металлах, то многие из них необходимы в следовых количествах. Повышенные же их концентрации в организме вызывают токсические эффекты.Токсическое действие чужеродных металлов часто обусловлено антагонизмом катионов. Так, например, свинец - известный нейротоксин, вытесняет кальций из некоторых отделов нервной системы и тем самым препятствует выделению нейромедиаторов. В 1960 г. широко распространившееся загрязнение восточного побережья Японии кадмием в сочетании с низким уровнем поглощения кальция привело к развитию у людей мучительной болезни - одной из разновидностей остеомиелита. Выяснилось, что причина этого заболевания - антагонизм кадмия и кальция.С другой стороны, известны случаи синергического действия металлов. Например, показано, что внесение отдельных металлов в концентрациях, соответствующих предельно-допустимым (Канада, США), в культуру водорослей хлорелла, сценедесмус и других не влияло на рост клеток, тогда как их смесь сильно подавляла рост, даже при более низких концентрациях. Число таких примеров достаточно велико.
27. Двухфазная ответная реакция организма на действие тяжелых металлов. Антагонизм катионов. Относительно концентрационных эффектов металлов следует подчеркнуть, что реакция организма на тяжелые металлы является двухфазной.Если организм получает слишком мало металлов, ему наносится тяжелый ущерб. Это объясняется тем, что в организме содержится множество ферментов, которые могут функционировать только в присутствии тяжелых металлов, хотя бы в следовых количествах. Однако если организм получает слишком много металла, то наступает вторая фаза, связанная с токсическим действием избыточного количества.Примером такой двухфазной реакции может служить действие меди на овес: как избыточное, так и недостаточное количество этого металла наносит вред процессам его роста и развития.При содержании двух электронодонорных групп заряд катиона металла при образовании хелатного соединения не меняется (этилендиамин). Лиганды могут содержать также одну электронодонорную и одну анионную группы, как в глицине. В этом случае заряд металла уменьшается на единицу.
28. Химизм хелатообразования. Механизмы биологического действия хелактирующих агентов.В зависимости от количества вступивших во взаимодействие атомов металлов и лигандов могут образовываться комплексы 1:1, 1:2 и др.
А. Образование комплексов в стехиометрическом соотношении 1:1.
Три основных типа лигандов, образующих одно кольцо в комплексе 1:1:
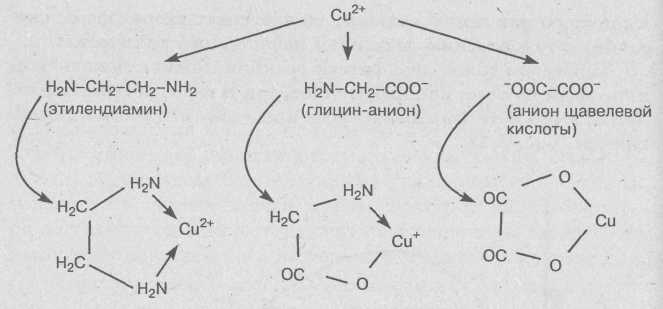
а) если лиганд содержит две электрондонорные группы, то заряд катиона металла при образовании хелатного соединения не меняется;
б) если лиганд содержит одну электронодонорную и одну анионную группу (глицин), то заряд металла уменьшается на единицу;
в) если, лиганд содержит две анионные группы (щавелевая кислота), то заряд металла уменьшается на две единицы.
Хелатные связи с атомами О и N возникают, обычно, в случае образования пяти- и шестичленных циклов. Однако при образовании хелатных связей через серу возникают устойчивые четырехчленные циклы.
Б.Образование комплексов в стехиометрическом соотношении 2:1. Такие комплексы могут образовываться в присутствии избытка лигандов.
-комплексы щавелевой кислоты 1:1 могут соединяться в дальнейшем с комплексом этилендиаминового типа, образуя смешанные комплексы;
-комплексы 1:1 глицинового типа способны соединяться с другими лигандами этого типа;
-комплекс 1:1, образованный лигандами, подобнымиэтилендиамину, может соединяться с любым из трех типов лигандов, образующих комплексы 1:1.
Для оценки прочности связей применяют константы устойчивости θ , характеризующие равновесие между одним или несколькими лигандами и одним ионом металла, подчиняющееся закону действия масс. Для комплекса в соотношении 1:1 константа устойчивости рассчитывается по формуле:
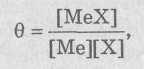
Факторы, влияющие на хелатообразование:
1)радиус иона.Повышение сродства к хелатирующим агентам является следствием уменьшения ионного радиуса. С увеличением заряда катиона металла так же происходит уменьшение его радиуса, поэтому Fe3+ имеет большее сродство, чем Fe2+.
2) степень ионизации хелатообразуншшх агентов. Вещество, обладающее меньшим сродством к металлу, может присоединить большее количество катионов металла, чем вещества, у которых это сродство больше. Это объясняется тем, что для хелатообразования необходимо не только наличие сродства между лигандом и металлом, но также быстрое образование анионов лиганда из агента (или молекул лиганда), т.е. зависит от значения константы ионизации.
3) химическая природа лиганда. Так, большинство металлов легче соединяются с лигандами, содержащими О, а не S. Однако Cu+, Ag+, Hg2+, As+ и Sb3+ отдают предпочтение сере;
у Cu2+, Ni2+ и Со2+ сродство к сере выше, чем к кислороду, если сера находится в неионизированном состоянии (органические сульфиды).
4) изменение окислительно-восстановительного потенциала металла, вызванное образованием хелатных соединений с металлами, имеющими переменную валентность. Вследствие хелатообразования такие металлы могут изменять первоначальную валентность. Металл может изменять избирательность органическоголиганда:
─ влияя на распределение электронов в лиганде;
─ повышая реакционную способность активного центра лиганда;
─ вызывая изменение конформациилиганда;
─ обеспечивая возможность присоединения или отрыва электрона;
─ увеличивая липофильностьлиганда и, следовательно, его способность проникать в живую клетку.
