Заттар қоспасының анализі.
Практика жүзінде ерітіндідегі екі немесе одан да көп компоненттерді анықтау қажет болады. Кейде компоненттерді алдын-ала бөліп алмайынша оларды бірге жүргенде анықтау мүмкін болмайды. Егер компоненттердің спектрлері бір-біріне қабаттасатын болса, онда аддитивтілік заңына сүйеніп анықтауға болады.
Хром мен марганецті бірге жүргенде анықтау аддитивтілік заңына және ерітіндідегі перманганат пен бихромат-иондарының жұту спектрлерінің айырмашылығына негізделген. Перманганат хромат жұтпайтын ұзындығы 550 нм жарық толқынын жұтады. Бихроматтың максимальды жұтатын жарық толқыны 430 нм. Перманганатта осы толқын ұзындығында жарықты жұтады. Сондықтан хромды анықтауға марганец кедергі жасайды.
Әртүрлі жарықсүзгілерін пайдаланып, бірге жүрген хром мен марганецті анықтауға болады. Ол үшін 550 нм жарық толқынының ұзындығын өткізетін жасыл жарықсүзгісін және 430 нм жарық толқынының ұзындығын өткізетін көк жарықсүзгіні қолданады. Алғашқыда марганецтің 550 нм және 430 нм толқын ұзындығындағы оптикалық тығыздығын өлшеп, калибрлі графигін түзеді (14.31-сурет). Содан кейін 430 нм-дегі хромның калибрлі қисығын алады.
|
|
Құрамында хромат пен перманганат ионы бар анықтайтын ерітіндінің оптикалық тығыздығын жасыл (550 нм) және көк (430 нм) жарықсүзгісін қолданып өлшейді. Калибрлі графиктен 550 нм-дегі оптикалық тығыздықтың мәнінен марганецтің мөлшерін тікелей анықтайды. Марганецтің 430 нм-дегі калибрлі графигінен анықталған мөлшеріне сәйкес оптикалық тығыздығын табады.
Хромның оптикалық тығыздығын табу үшін 430 нм-дегі жалпы оптикалық тығыздықтан осы толқын ұзындығындағы марганецтің оптикалық тығыздығын алып тастайды.
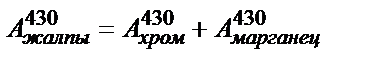
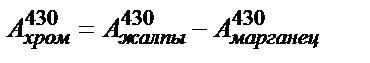
Хромның калибрлі графигін қолданып оның мөлшерін табады.
Көпкомпонентті жүйедегі 1 компонентті ғана анықтау қажет болса, одан басқаларын фон деп атайды. Анықталатын компоненттің концентрациясы аз да болуы мүмкін не көп те болуы мүмкін. Мысалы құрыштың құрамындағы никельді анықтау кезінде Ғе – негіз деп аталады. Көптеген әдістерде кедергі жасайтын компоненттерді немесе анықталатын компонентті алдын ала бөліп алады. Ал кейбір жағдайда оларды бір-бірінен бөлмей-ақ та анықтай береді. Мысалы, базисті сызық әдісін, Аллен әдісін және т.б. қолданып анықтау кезінде.
Базисті сызық әдісінде қиындыларды табады (14.32-сурет). АВ- қиындысы – анықталатын компоненттің оптикалық тығыздығын, ал ВС- қиындысы – фонның оптикалық тығыздығын көрсетеді. Анықталатын компоненттің концентрациясын Бугер-Ламберт-Бер заңына сәйкес: 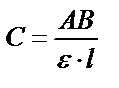 теңдігі арқылы анықтайды.
теңдігі арқылы анықтайды.
| А |
| λ |
| а) |
| А |
| В |
| С |
| А |
| λ |
| б) |
| λ2 |
| λ1 |
| λ3 |
14.32-сурет. Базисті сызық (а) және Аллен (б) әдістері
Аллен әдісі: анықталатын ерітіндінің оптикалық тығыздығын үш түрлі толқын ұзындығында λ1; λ2; λ3 өлшейді (14.32-сурет). λ1 мен λ2 және λ3 бір-бірінен бірдей қашықтықта болады. Анықталатын зат концентрациясын: 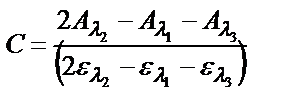 .теңдігі арқылы табады
.теңдігі арқылы табады
Комплекстің құрамын анықтау
Комплекстің құрамын өте кең тараған изомолярлы сериялар әдісімен анықтайды (14.33-сурет). Ол үшін изомолярлы ерітінділер сериясын дайындайды. Бұнда орталық ион мен лигандтың концентрациясы әртүрлі болатын ерітінділер сериясын дайындайды. Ескеретін бір нәрсе, бұнда орталық ион мен лигандтың қосынды концентрациясы барлық ерітіндіде бірдей болады. Белгілі толқын ұзындығында ерітіндінің оптикалық тығыздығын өлшейді. Содан соң төмендегідей график тұрғызады.
| DА |
| 0,4 |
| 0,2 |
| 0,6 |
| 0,8 |
| С2 |
| С1 |
| б) |
| DА |
| 0,4 |
| 0,2 |
| 0,6 |
| 0,8 |
| С2 |
| С1 |
| а) |
14.33-сурет. Комплекстің құрамын изомолярлы сериялар әдісімен анықтау. Компоненттер қатынасы: а) 1:1; б) 1:2
Компоненттердің массалық үлесінің комплекстегі стехиометриялық қатынасқа сәйкес мәндерінде максимум пайда болды. Оң және сол жақ қанаттарына түзу жанама жүргізіп, яғни экстраполяциялап екі түзудің қиылысқан нүктесін табады. Осы нүктедегі орталық ион мен лигандтың мольдік үлестерінің қатынасы комплекстің құрамын көрсетеді. Комплекс тұрақсыз болған сайын, оның максимумы ұшқыр болмайды. Бұл әдісте компоненттер қатынасы: 1:1; 1:2; 2:1 қатынасындай болғанда жақсы нәтиже береді.
14.2.10 Люминесценция
Люминесценция дегеніміз – атомдардың, молекулалардың жарық шығаруы болып табылады. Бұл құбылыс осы бөлшектердің қозған күйден қалыпты жағдайға қайта оралуы нәтижесінде, яғни электрондық ауысу нәтижесінде пайда болады.
Заттардың жарық шығаруы яғни люминесценттенуі олардың газ күйінде де, қатты және сұйық күйінде де байқалады.
Люминесценция құбылысы өте алуан түрлі.
1) Қоздыру тәсіліне байланысты люминесценцияны катодолюминесценция, хемилюменесценция, рентгенолюминесценция, триболюменесценция, термолюминесценция, фотолюминесценция деп бөледі.
а) катодолюминесценция – электрондар шоғымен атқылау нәтижесінде пайда болады;
б) хемилюминесценция – химиялық реакциялар жүру кезінде бөлінетін энергияның әсерінен пайда болады;
в) рентгенолюминесценция – рентген сәулелері әсерінен пайда болады;
г) триболюменесценция – кристалдарды бөлу, ұнтақтау, үгу, ысқылау нәтижесінде пайда болады;
д) термолюминесценция – температураны арттырып қоздыру әсерінен пайда болады;
ж) фотолюминесценция – УК немесе көрінетін сәулелердің әсерінен пайда болады.
Химиялық анализде көбінесе фотолюминесценция қолданылады.
2) Сәулеленуінің ұзақтығына байланысты люминесценция құбылысы флуоресценция және фосфоренция деп екіге бөлінеді.
а) флуоресценция кезінде қоздыру тоқталса, жарық шығару да тоқталады;
б) фосфоресценция кезінде қоздыру тоқталса да, жарық шығару тоқталмайды. Аналитикалық анықтауларда флуоресценция жиі қолданылады.
Люминесценция қоздыру тәсіліне тәуелсіз қашанда үш негізгі стадиядан тұрады:
1) затты қозған күйге көшіретін энергия жұту;
2) жұтылған энергияның заттың ішінде өзгеріске түсуі;
3) артық энергияның сәулеленуі (шығарылуы) және заттың қалыпты жағдайға қайта оралуы.
Флуоресценция – көзге көрінетін сәулеленуі болмайтын құбылыс, ұзақтығы 10-8 – 10–9 секунд.
Флуоресценция – көзге көрінетін сәулеленуі бар құбылыс. Ұзақтығы бірнеше сағатқа созылады, көбінесе қатты заттарға тән.
Люминесцентті анализ өсімдік және жануартекті тағам заттарын зерттеуде қолданылады. Люминесцентті анализ сапалық және сандық деп бөлінеді.
Капустаның, бұршақ тұқымдастарының, қиярдың шіри бастауын алғашқы стадияда флуоресценция қанықтығына байланысты байқауға болады. Осы люминесцентті анализ арқылы картоптың сапасын, астықтың (ұнның) сортын да анықтауға болады. Қоқыс көп болса жарықтың қанықтығы жоғары болады. Белокты анықтауда да люминесцентті анализ жиі қолданылады. Өйткені, белоктың құрамындағы ароматты аминқышқылдарының люминесценттену қабілеті жоғары болады. Люминесценция құбылысы күнделікті өмірде де жиі байқалады. Мысалы, микроороганизмдердің кейбір түрлері, насекомдардың, кейбір терең су балықтарының люминесценттену қабілеті болады. Наркотиктер, дәрі-дәрмектер, бензин, полициклді ароматты көмірсутектер күн сәулесі әсерінен люминесценттенеді. Кейбір минералды рудалар (уранды рудалар) жарық шығарады. Мысал ретінде теледидардың жарық шығаруын айтуға болады.
Люминесценция қанықтығына әсер ететін процестерді люминесценцияны сөндіру құбылысы деп атайды. Зат концентрациясының 10–3 – 10–4 моль/л аралығында ғана люминесценция қанықтығы жоғары болады, бұны люминесценцияны концентрациялық сөндіру деп атайды. Температура жоғарласа да люминесценция қанықтығы төмендейді. Ортаның әсеріне байланысты да люминесценция қанықтығы өзгереді, мысалы элементарлы J2, Fe3+, Cu2+ қосса люминесценция сөнеді. Бұларды сөндіргіштер деп атайды.
Фосфоренция құбылысын молекуланың синглетті және триплетті жағдайларын есімізге түсіріп, сол арқылы түсіндіруге болады.
Молекуланың мейлінше тұрақтырақ жағдайы синглетті жағдай болып табылады.
Синглетті жағдайда бір орбитадағы электрондардың және суммарлы спин саны 0-ге тең және антипараллельді болады.
Электронның синглетті өзгертпей ауысуы синглет-синглетті деп аталады. Мысалы:
S0 S1 S0 S2; S0 S1 .
Алғашқы 2-уі жарықты сіңіру нәтижесінде жүзеге асады. Ал үшіншісі флуоресценция кезінде жүзеге асады. Триплетті жағдайда, мыс: Т1 немесе Т2 қозған ē – ның спиндері параллельді болады және суммарлы спин 1-ге тең болады.
Синглетті жағдайдан триплетті жағдайға, яғни S1 T1 ауысуы көп таралмаған ауысуға жатады. Бұндай ауысулар тек күрделі атомдардың қатысында ғана мүмкін болады. Мысалы, галогендер қатысында және мұндай ауысуларды интеркомбинациялық конверсия деп атайды. Триплетті жағдайдың Т1 ұзақтығы 10– 3 – 10– 2 секундқа тең. Триплетті жағдайдағы молекула өзінің энергиясын жылу күйінде оңай бөліп шығарып, жояды. Мұндай дезактивациялану триплетті молекуланың жұптастаған ē – дары бар молекуламен соқтығысуынан болуы мүмкін. Мысалы: О2 – молекуласы. Сондықтан фосфоренцияға қарағанда флуоресценция жиі байқалады. Органикалық қосылыстар мұздатып, қатырылған күйінде интенсивті түрде фосфоресценттенеді.
