Для очистки бытовых стоковых вод больших жилищных массивов
Лабораторная работа №2.
Изучение фотосинтеза погруженных водных растений, которые используются
для очистки бытовых стоковых вод больших жилищных массивов.
В термодинамических условиях поверхности земли при активной деятельности живых организмов или продуктов их жизнедеятельности осуществляются многочисленные превращения веществ, которые систематически повторяются. Превращения веществ в значительной степени циклические, потому их называют кругообменами или циклами. В основе кругообмена лежит фотосинтез-реакция образования сложных веществ из простых неорганических соединений за счет энергии солнечного света, которая поглощается пигментом хлорофиллом. Эта реакция осуществляется в высших растениях, водорослях, фотосинтезирующих бактериях. Общий вид ее такой:
6С02 + 6Н20 = С6Н1206 + 602 (1)
Количество энергии, которая ежегодно связывается в продуктах фотосинтеза, на порядок более высокая всех энергетических потребностей человечества. В процессе фотосинтеза образуется органическое вещество и кислород. Вместе с углеводами в процессе фотосинтеза образуются аминокислоты, пигменты, сырьем для которых выступают сульфаты, фосфаты, нитраты. Из уравнения можно сделать вывод, что фотосинтез вместе с противоположным процессом окисления органического вещества обеспечивает ряд био- гео- химических циклов: водяной пары, углекислого газа, органического вещества, кислорода, а также превращения и аккумуляцию энергии. Масштабы этих циклов очень значительные: 100 млрд.т С02; 145 млрд.т 02. Считается, что весь кислород атмосферы плюс часть 02, которая связана с горными породами-оксидами, является продуктом фотосинтеза. С фотосинтезом в значительной степени связан углеродный био- гео- химический цикл. Он объединяется миграцией углерода, который в разных средах образует разные соединения. Этот цикл интересен механизмом саморегуляции и, экологически, очень важен. Углеродный цикл протекает в системе: земная кора (высвобождение С02 за счет вулканичных процессов и окисления органических остатков, депонирования углерода в карбонатах) - атмосфера (промежуточное звено цикла) - океан (химическая лаборатория, в которой образуется угольная кислота и свои соли, а также регулятор содержания С02 в системе: океаническое дно - донный ил - воды океана - атмосфера) - живые организмы (высвобождение С02 в процессе дыхания, аккумуляция фотосинтезирующими растениями) -человечество (высвобождение С02, СО за счет сгорания топлива). Основным регулятором в этом цикле является Мировой океан (при условии чистоты поверхности, в другом случае нарушается газообмен между ней и атмосферой). Важный экологический вывод заключается в потому, что углеродный цикл способен вбирать у себя избытки С02, что присутствует в атмосфере, емкость океана в этом случае безгранична. Но для этого необходимо время (система инерционная, связанная с изменением концентрации С02 во всей толще океана), единство цикла, чистота поверхности океана. Прогнозы климата, которые не учитывают цикл углерода, неверны.
В последнее время внимание геофизиков (авторы таких прогнозов) направлено на то, что нет прямой зависимости между ростом темпов сжигания топлива, повышением содержания С02 в атмосфере и парниковим эффектом.
В водных экосистемах кислотность воды зависит от содержания в них С02, потому что С02 в результате взаимодействия с водой образует угольную кислоту:
С02 + Н20 ========== Н2С03 (2)
Угольная кислота в очень разведенных водных растворах полностью разлетается на ионы:
н2со3 н++ нсо3-
НС03- Н+ + СОз-2
Критерием кислотности среды, которая определяется экспериментальным методом, есть рН(Ю9) - отрицательный логарифм концентрации ионов водорода:
(РН = -lg[Н+]) (3)
Основным фактором, который снижает содержание С02 в водных экосистемах, является фотосинтез углеводов в зеленом листе растений по уравнениям фотосинтеза. Таким образом, фотосинтез углеводов, если экспериментально определять рН водного раствора, с погруженной в него высшей водной растительностью, за определенный промежуток времени, можно легко оценить количество углекислоты, которая поглощается, и по уровню фотосинтеза рассчитать количество образованного кислорода (02) и углеводов (СбН1206 - прирост биомассы), то есть, оценить производительность (116) высшей водной растительности.
Цель работы. Изучение процесса фотосинтеза, который протекает в клетках погруженной водной ростительности методом измерения рН; расчет содержания поглощенного С02, образованного кислорода и углеводов.
Приборы и оборудование. Для выполнения работы необходим рН-метр, например рН-121.
Методика выполнения работы. В два сосуда, объемом 0,5л, налить по 0,5л водопроводной воды, из которой, отстаиванием удалить хлор (можно пользоваться водой из открытого водоема), подогретой до температуры 20-25°С. В один сосуд положить небольших розмсров водное растение, второй сосуд оставить без растения. Сосуды плотно закрыть крышками и расположить возле источника видимого света (например, на подоконнике, или под настольную лампу) и освещать в течение 30 минут. После этого взять пробы воды из обоих сосудов и провести измерение рН этих проб. Получены данные, занесите в таблицу 2.1.
Внимание! В нашем курсе Вам нужно взять не менее как два примера экспериментальных данных, которые приведены в таблице 2.
Таблица 2 Экспериментальные данные, полученные в процессе измерения рН
| Экспериментальный образец | Значение рН образца воды | |
| в контрольном опыте (без растения) | в рабочем опыте (с растением) | |
| 6.52 | 6,91 | |
| 6.45 | 6.87 | |
| 6,56 | 6,92 | |
| 6,75 | 7,02 | |
| 6,35 | 6,59 |
Таблица 2.1 - Экспериментальные данные, полученные в процессе измерения рН
| Экспериментальный образец | Значение рН образца воды | |
| в контрольном опыте (без растения) | в рабочем опыте (с растением) | |
По значению величины рН и использованием формулы (3) рассчитайте концентрацию ионов водорода Н~ в контрольном опыте (без растения) и в опыте с растением (используйте таблицу антилогарифмов). Потом пользуясь схемой (4):
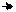
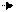

 2Н+ Н2С03 С02 02 1/6С6Н1206 (4) - рассчитайте количество ССЬ, который был употреблен в процессе фотосинтеза, и биомассы в виде углевода СбН1206, а также количество 02, который при этом высвободился.
2Н+ Н2С03 С02 02 1/6С6Н1206 (4) - рассчитайте количество ССЬ, который был употреблен в процессе фотосинтеза, и биомассы в виде углевода СбН1206, а также количество 02, который при этом высвободился.
2Н+ СО2
2МН+ МСО2
mН+ mСО2
Отсюда: МСО2 · mН+
 mСО2 =
mСО2 =
2МН+
где: mС02 - масса С02, который был употреблён, мг;
mН+ - масса ионов водорода в растворе, принимающих участие в реакции, мг;
МС02 - молекулярная масса С02; МН+ - атомная масса Н+.
mН+ = (ϭН+) · Мн + · V
где: V - объем воды в сосудах, мл;
(ϭН+) - разница в концентрации водородных ионов в опыте с растительностью и в контрольном опыте;
(ϭH+)· Mн+ · V · MCO2 (ϭH+)· V· MCO2

 mCO2 = =
mCO2 = =
2Mн+ 2
Точно такой же рассчитайте количество высвобожденного кислорода:
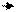 2(ϭН+) О2
2(ϭН+) О2
(ϭН+ ) · V · МО2
 mО2=
mО2=
и образованного углевода С6Н12О6
 1/6 · 2(ϭН+) С6Н12О6;
1/6 · 2(ϭН+) С6Н12О6;
(ϭН+) ·V ·M C6H12O6
 mC6H12O6=
mC6H12O6=
2 ·6
Полученные результаты расчётов запишите в таблицу 2.2.
Таблица 2.2 — Результаты расчёта количества веществ, которые принимали участие в реакции фотосинтеза, на основе данных эксперимента.
| № експер. | Опыт | рН | Н+ | ϭН+ | тсо2, мг | mCO2, мг | mуглевМГ |
| контр. | |||||||
| с растен. | |||||||
| контр. | |||||||
| с растен. | |||||||
Сделайте вывод на базе полученных расчетов об интенсивности фотосинтезной деятельности в зеленых частях, погруженных водных растений. Дайте рекомендации относительно использования тех или иных растений для очистки бытовых сточных вод.
Тест-контроль.
1.К каким реакциям можно отнести фотосинтез?
«А» - к реакциям окисления - обновления.
«Т» - к реакции соединения (синтеза).
«В» - к реакциям расщепления.
2. Какова роль Мирового океана в регуляции биохимического цикла углерода?
«А» - в поглощении углекислого газа из атмосферы.
«Б»-в высвобождении кислорода в атмосферу.
«В» - в снабжении паров волы для поддержки водообмену.
