В изолированных системах самопроизвольно могут совершаться только такие необратимые процессы, при которых энтропия системы возрастает (DS > 0).
Для неизолированных систем нужно учитывать не только изменение энтропии, но и изменение энергии. Поэтому необходимо рассматривать две тенденции, определяющие направление самопроизвольно протекающих процессов:
= стремление системы к достижению минимума энергии;
= стремление системы к максимуму энтропии, то есть к
неупорядоченности.
Процессы, при которых энергия в неизолированной системе уменьшается, а энтропия возрастает, протекают самопроизвольно. Самопроизвольность других процессов зависит от того, какая из этих двух тенденций – энергетическая или энтропийная – окажется более эффективной, какая из этих противоборствующих тенденций получит перевес над другой. В этом проявляется противоречивость материального мира.
Для однозначной формулировки условий протекания самопроизвольных процессов в любых системах введена ещё одна термодинамическая функция, которая характеризует одновременно и энергетику, и неупорядоченность систем. Впервые такую термодинамическую функцию ввёл Д. У. Гиббс, и в память об этом выдающемся американском учёном её назвали энергией Гиббса.
| Джозайя Уиллард Гиббс (11.11 1839=28. IV 1903). Американский физик и физико-химик, член Национальной АН США (с 1879). Родился 11 февраля в Нью-Хейвене. Окончил Йельский университет (1858; доктор философии, 1863). В 1863=1866 преподавал в Йельском колледже. Совершенствовал образование в Сорбонне и Коллеж де Франс в Париже (1866=1867), в Берлинском (1867) и Гейдельбергском (1868) университетах. С 1871 – профессор Йельского университета. Один из основоположников термодинамики. |  |
Предложил (1873) графические модели описания термодинамических свойств веществ. Разработал (1875=1878) теорию термодинамических потенциалов, изучил (1875) условия равновесия гетерогенных систем. Вывел (1875=1878) правило фаз, согласно которому в равновесной гетерогенной системе число фаз не может превышать числа компонентов системы, увеличенного на два. Предложил (1878) графическое изображение состояния трёхкомпонентной системы (треугольник Гиббса). Заложил основы термодинамики поверхностных явлений и электрохимических процессов; ввёл понятие адсорбции. Дал (1902) атомистическое истолкование развитым им термодинамическим методам. Осуществил исследования в области векторного анализа и алгебры кратных чисел, электромагнитной и механической теорий света.
Гиббс Член Американской академии искусств и наук (с 1880),и многих академий наук и научных обществ.
Биохимические процессы обычно происходят при изобарно-изотермических условиях. В этих условиях энергетическое состояние системы характеризуется энтальпией, а мера её неупорядоченности характеризуется произведением её энтропии и температуры. Функцией, учитывающей обе эти характеристики и противоположность в тенденции их изменения при самопроизвольных процессах, является энергия Гиббса:
G = Н -TS.
Энергия Гиббса является обобщённой термодинамической функцией состояния системы, учитывающей энергетику и неупорядоченность системы, при изобарно-изотермических условиях.
Энергию Гиббса называют также изобарно-изотермическим потенциаломили свободной энергией.
Подобно другим термодинамическим параметрам и функциям, характеризующим состояние системы, изменение энергии Гиббса в результате любого процесса определяется только конечным и начальным состоянием системы, независимо от пути процесса:
DG = Gкон - Gнач
Для энергетической характеристики веществ при стандартных условиях используют стандартные энергии Гиббса их образования DGо, значения которые даны в справочной литературе. Для простых веществ в термодинамически устойчивой форме стандартная энергия Гиббса их образования условно принимается равной нулю.
Изменение энергии Гиббса в результате химической реакции при стандартных условиях вычисляют по уравнению:
DGр = ∑vкон DGкон (Yкон) - ∑vисх DGисх (Xисх),
где DGкон(Yкон), DGисх(Xисх) - стандартные энергии Гиббса продуктов
реакции Yкон и исходных веществ Xисх.
vкон. и vнач - соответствующие стехиометрические коэффициенты в уравнении реакции.
Изменение энергии Гиббса для биохимических процессов при условиях, отличных от стандартных, рассчитывают на основе экспериментальных значений DН и DS для этих процессов по уравнению:
DG = DН - TDS,
где DН - характеризует полное изменение энергии системы при р,
Т = const и отражает стремление системы к минимуму энергии;
TDS - характеризует ту часть энергии, которую нельзя превратить в работу, и отражает стремление системы к максимуму неупорядоченности;
DG - характеризует ту часть энергии, которую можно превратить в работу, и является термодинамическим критерием возможности самопроизвольного протекания любых процессов при р, Т = const.
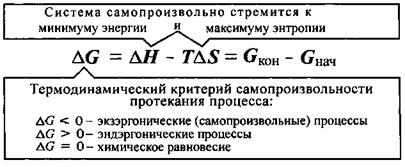
Соотношение между изменениями важнейших термоди-намических параметров и функций состояний системы, описывающими химические и биохимические процессы при р, Т = const, представлено в таблице и на следующей схеме.
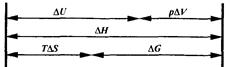
Второй закон термодинамики систем формулируется следующим образом: в системе при постоянных температуре и давлении самопроизвольно могут совершаться только такие процессы, в результате которых энергия Гиббса уменьшается (DGкон < DGнач или DG < 0).
Таким образом, согласно второму закону термодинамики самопроизвольно (DGр < 0) протекают экзотермические реакции (DНр < 0) при любой температуре, если они сопровождаются увеличением энтропии (DSp > 0). Эндотермические реакции (DНр > 0), сопровождающиеся уменьшением энтропии (DSp < 0), не могут протекать самопроизвольно ни при какой температуре, так как при этом DGр > 0.
Биохимические реакции
Биохимические реакции сопровождающиеся уменьшением энергии Гиббса (DGр < 0), называют экзэргоническими реакциями; они могут совершаться самопроизвольно. Если в течение экзэргонической реакции энергия Гиббса только понижается, как показано на рис. 1, то такая реакция протекает самопроизвольно и необратимо. Чем больше энергия Гиббса биохимической системы в начальном состоянии,чем в конечном состоянии, тем больше разница химического сродства между исходными веществами и продуктами реакции в то есть их реакционная способность.
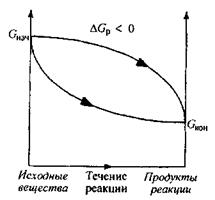
Рис. 1. Изменение энергии Гиббса в закрытой системе
в необратимых экзэргонических реакциях,
совершаемых самопроизвольно (р, Т = const)
Критерий DGp < 0 свидетельствует только о термодинамической возможности протекания данного процесса и ничего не говорит о его скорости и необходимых условиях для его начала.
Например, окисление (горение) графита:
С + O2 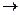 СО2
СО2
Согласно положениям термодинамики может происходить при стандартных условиях самопроизвольно, так как 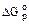 = -393,5 кДж/моль. однако графит при температуре 298 К с кислородом не реагирует, и чтобы реакция произошла, необходимо создать определённые условия (запал подвоз энергии, введение катализатора).
= -393,5 кДж/моль. однако графит при температуре 298 К с кислородом не реагирует, и чтобы реакция произошла, необходимо создать определённые условия (запал подвоз энергии, введение катализатора).
Биохимические реакции, сопровождающиеся увеличением энергии Гиббса (рис. 2), называются эндэргоническими (DGp > 0), и они не могут происходить без постоянного подвода энергии.
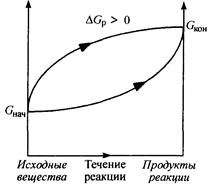
Рис. 2. Изменение энергии Гиббса в закрытой системе
в необратимых эндэргонических реакциях
(р, Т = const)
Например, процесс фотосинтеза в растениях идёт только под воздействием солнечной энергии:
6СО2 + 6Н2О 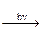 C6H12O6 + 6О2= DGp = 2870 кДж/моль.
C6H12O6 + 6О2= DGp = 2870 кДж/моль.
В живых системах эндэргонические реакции происходят за счёт их сопряжения с экзэргоническими реакциями.
Таблица
р, Т = const Взаимосвязь термодинамических величин 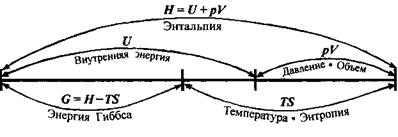 | ||
 | ||
Химическое равновесие
|
5. ПРИНЦИП ЭНЕРГЕТИЧЕСКОГО СОПРЯЖЕНИЯ
БИОХИМИЧЕСКИХ РЕАКЦИЙ
Живая клетка для своего существования нуждается в энергии. При этом некоторые (гетеротрофные) клетки получают необходимую энергию в основном за счёт окисления продуктов питания, а для некоторых (прототрофных клеток источником энергии часто является солнечный свет. Полученная энергия переводится клетками обоих типов с довольно хорошим КПД (~ 40 %) в химическую энергию за счёт синтеза в них аденозинтрифосфорной кислоты (АТФ):
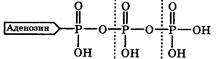
АТФ выполняет функцию аккумулятора энергии, так как при его гидролизе (расщеплении водой), образуются аденозиндифосфорная (АДФ) и ортофосфорная (Ф) кислоты и выделяется энергия. Поэтому АТФ называется макроэргическим соединением, а разрывающаяся при его гидролизе связь О–Р - макроэргической.
Макроэргической связью называется химическая связь, при гидролизе которой выделяется значительная энергия:
АТФ + Н2О ® АДФ+ Ф, DGр = -30,5 кДж/моль;
АДФ + Н2О ® АМФ= 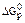 = -30,5 кДж/моль;
= -30,5 кДж/моль;
АТФ + 2Н2О ® АМФ + 2Ф, 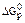 = -61,0 кДж/моль.
= -61,0 кДж/моль.
Разрыв любой химической связи (в том числе и макроэргической) требует затраты энергии. В случае же гидролиза АТФ, кроме разрыва связей между фосфатными группами, (DG > 0), происходят процессы гидратации (присоединение воды), изомеризации и нейтрализации кислотных продуктов, образующихся при гидролизе. В результате этих процессов суммарное изменение энергии Гиббса имеет отрицательное значение (∑∆G < 0). Следовательно, макроэргическим является не разрыв связей О-Р, а энергетический результат реакции гидролиза в целом.
АТФ функционирует в клетках как промежуточный продукт, обеспечивающий организм энергией, необходимой для протекания жизненно важных эндэргонических процессов: синтеза метаболитов (химическая работа), сокращения мышц (механическая работа), переноса вещества через мембраны против градиента концентрации (активный транспорт) и передачи информации (в частности, для передачи нервных импульсов).
Для протекания в живых системах эндэргонических реакций (DGp > 0), необходимо, чтобы они были сопряжены с экзэргоническими реакциями (DGp < 0). Такое сопряжение возможно, если обе реакции имеют какое-либо общее промежуточное химическое соединение и на всех стадиях сопряжённых реакций суммарный процесс характеризуется отрицательным значением изменения энергии Гиббса (Σ∆Gсопряж.р-ий 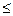 0).
0).
Например, синтез сахарозы из глюкозы и фруктозы является эндэргонической реакцией и самопроизвольно происходить не может:
Глюкоза + Фруктоза → Сахароза + Н2О, 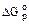 = 20,9 кДж/моль
= 20,9 кДж/моль
Однако сопряжение этой реакции с экзэргонической реакцией гидролиза АТФ, сопровождающееся образованием общего промежуточного соединения глюкозо-1-фосфата, приводит к тому, что суммарный процесс имеет ∑DGр < 0:
АТФ + Глюкоза + Фруктоза → Сахароза + АДФ + Ф,
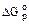 = -29,2 кДж/моль.
= -29,2 кДж/моль.
Наряду с АТФ в живых организмах имеются более эффективные макроэргические фосфорилированные соединения, гидролиз которых сопровождается выделением большей энергии. Так, стандартная энергия Гиббса для гидролиза креатинфосфата, 3-фосфоглицерилфосфата и фосфоенолпирувата равна соответственно -43,1, -49,4 и -61,9 кДж/моль. С помощью этих соединений происходит синтез АТФ из АДФ, а АДФ из АМФ.
Таким образом, внутренним источником энергии в живых системах являются фосфорилированные соединения, при взаимодействии которых с биосубстратами, включая воду, выделяется энергия. В результате сопряжения этих экзэргонических реакций с эндэргоническими реакциями обеспечивается протекание в клетке необходимых эндэргонических процессов.
6.ОСОБЕННОСТИ ТЕРМОДИНАМИКИ БИОХИМИЧЕСКИХ ПРОЦЕССОВ В РАВНОВЕСНЫХ СТАЦИОНАРНЫХ СОСТОЯНИЯХ.ПОНЯТИЯ О ГОМЕОСТАЗЕ
Отличительная особенность протекания обратимых биохимических реакций заключается в стремлении достичь динамического равновесия, так как это состояние возникает и поддерживается вследствие протекания реакций в двух противоположных направлениях с одинаковыми скоростями 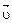 =
= 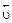 . Такое состояние называется химическим равновесием. В этом случае изменение энергии Гиббса в системе характеризуется наличием минимума, который соответствует состоянию химического равновесия (рис. 3, таблица). К равновесному состоянию возможен подход как со стороны исходных веществ (Δ
. Такое состояние называется химическим равновесием. В этом случае изменение энергии Гиббса в системе характеризуется наличием минимума, который соответствует состоянию химического равновесия (рис. 3, таблица). К равновесному состоянию возможен подход как со стороны исходных веществ (Δ 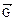 < 0), так и со стороны продуктов реакции (∆
< 0), так и со стороны продуктов реакции (∆ 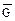 < 0).
< 0).
При протекании обратимых реакций система самопроизвольно приходит к состоянию химического равновесия, из которого она без внешнего воздействия выйти не может, поскольку это требует увеличения энергии Гиббса.
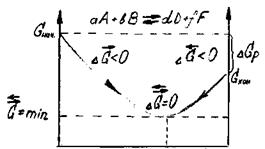
| Исходные вещества | Равновесный состав смеси исходных веществ и продуктов реакции | Продукты реакции |
Рис. 3. Изменение энергии Гиббса в закрытой системе
в обратимой химической реакции
(р, Т = const)
Химическое и биохимическое равновесное состояние системы характеризуется:
= равенством скоростей прямой и обратной реакций ( 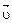 =
= 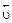 );
);
= энергетической выгодностью ( 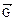 = min);
= min);
= отсутствием изменений величин параметров и функций состояния системы: концентрации реагентов, энтальпии, энтропии и энергии Гиббса [(Δ 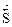 = О) (Δ
= О) (Δ 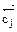 = 0) ( Δ
= 0) ( Δ 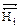 = 0) (ΔG =0)]
= 0) (ΔG =0)]
Поскольку в состоянии химического равновесия система достигает минимально возможной энергии Гиббса, то реакция, которая приводит в данных условиях к состоянию равновесия, всегда протекает самопроизвольно. Благодаря этой особенности обратимых процессов большинство биохимических реакций, протекающих в организме, обратимы.
Другая особенность биохимических процессов, протекающих в организме, заключается в их многостадийности, так как вероятность обратимого протекания отдельной стадии значительно выше, чем процесса в целом (рис. 4). Это объясняется тем, что разница между величинами (Gнач и Gкон для каждой отдельной стадии обычно невелика (| ΔGp | < 10 кДж/моль).
Обратимость отдельных стадий биохимических процессов позволяет живому организму легко регулировать синтез тех или иных химических соединений в зависимости от потребности и тем самым поддерживать стационарное состояние.
Стационарное состояние для живого организма характеризуется постоянством его термодинамических величин и неизменностью во времени скоростей поступления и удаления веществ и энергии. Несмотря на постоянство термодинамических величин, они не имеют равновесных значений в этом состоянии. Биологическое развитие организма возможно только в системе, находящейся в стационарном состоянии, но далёком от равновесия. Именно стационарное неравновесное состояние живой материи позволяет ей оптимизировать свои характеристики и эволюционировать во времени.
Термодинамическая особенность стационарного состояния открытых систем впервые сформулирована И. Р. Пригожиным (1946 )*.
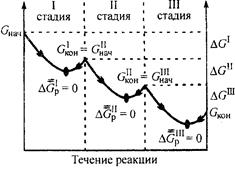
Рис. 4. Изменение энергии Гиббса в многостадийном
биохимическом процессе
(р, Т = const)
В открытой системе в стационарном состоянии прирост энтропии в единицу времени принимает минимальное положительное значение ( ΔS / Δτ → min).
Поскольку энтропия является мерой деградации, или рассеяния энергии, принцип Пригожина приводит к важнейшему заключению: при стационарном состоянии рассеяние энергии Гиббса открытой системой оказывается минимальным.
Термодинамические особенности открытых систем, характерные для живого организма, объясняют его устойчивость, позволяющую ему в течение многих лет сохранять определённый уровень работоспособности, а также относительное постоянство внутренней среды, называемое в биологии гомеостазом.
Гомеостаз – относительное (!) динамическое постоянство состава и свойств внутренней среды организма, обуславливающее устойчивость его физиологических функций.
В формировании и поддержании состояния гомеостаза большую роль играет обратимость большинства биохимических процессов. Эти процессы протекают самопроизвольно в направлении достижения равновесия, но, как правило, в организме они его не достигают, а только приводят к достижению необходимого соотношения между конечными и исходными веществами реакции, протекающей самопроизвольно при данных условиях. Это происходит или за счёт использования продуктов реакции, протекающей самопроизвольно в других процессах, или за счёт изменения условий в данной системе. Так, система, приближающаяся к химическому равновесию, переносится организмом в другие условия, при которых к состоянию химического равновесия приводит обратная реакция. Например, в лёгких, где концентрация кислорода большая, гемоглобин крови соединяется с ним, но, не достигнув состояния равновесия в насыщении кислородом, кровь переносится из лёгких к тканям, и там гемоглобин отдаёт О2, поскольку при переходе от лёгких к тканям в крови изменяются условия для процесса взаимодействия гемоглобина с кислородом. Другой пример: формирование и рост костной ткани происходит в одних клетках - остеобластах,* а её растворение - в других клетках - остеокластах,** в то же время работа клеток обоих типов регулируется организмом, что позволяет ему поддерживать содержание костной ткани на определённом уровне.
Организм, таким образом, использует в своей жизнедеятельности обратимые биохимические процессы и их стремление к состоянию химического равновесия, но не допускает наступления устойчивого во времени химического равновесия, так как это состояние приведёт к гибели организма. В то же время состояние гомеостаза поддерживается за счёт баланса, то есть необходимого соотношения между компонентами с противоположными (антагонистическими) свойствами. Так, в основе гомеостаза организма находятся следующие химические и физико-химические балансы: кислотно-основный, окислительно-восстановительный, металло-лигандный, гидрофильно-липофильный, водно-электролитный. В литературе понятия "баланс" и "гомеостаз" часто используются как синонимы.
Заключение
Основные положения, следующие из законов термодинамики:
= развитие системы происходит под влиянием двух тенденций =стремления к минимуму энергии и к максимуму энтропии;
= экзэргонические реакции в организме протекают самопроизвольно, так как ΔGр < 0;
= эндэргонические реакции требуют подвода энергии, так как DG > р0;
= состояние равновесия в обратимых процессах с позиции термодинамики характеризуется ∆ 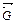 = 0 и является энергетически самым выгодным, так как
= 0 и является энергетически самым выгодным, так как 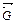 = min;
= min;
= биологические системы в стационарном состоянии характеризуются отношением DS/Δτ → min, а в соответствии с законом сохранения суммой S + I = const для живых систем должна быть справедлива закономерность Δ I/Δτ → max (в пределах соблюдения приведённого закона сохранения). При этом биологические системы далеки от состояния равновесия, что позволяет организмам оптимизировать свои характеристики и эволюционировать во времени.
Законы биохимической термодинамики дают экологу биологу, и врачу ключ к пониманию энергетической стороны биохимических реакций в организме, процессов эмбриогенеза,* регенерации** и старения тканей, аналогичных процессов, протекающих в биосфере, а также дают возможность регулировать эти процессы осуществлением профилактических или исправляющих (лечебных) мероприятий.
КОНТРОЛЬНЫЕ ЗАДАНИЯ
Вариант 1
1.При сгорании 1 л ацетилена C2H2 выделяется 58,0 кДж теплоты. Вычислите стандартную энтальпию реакции окисления (горения) ацетилена ?
2.При каком соотношении ∆H и T∆S системы находятся в равновесии ?
Вариант 2
1.Вычислите тепловой эффект реакции восстановления 1 моля оксида железа (III) алюминием.
2.Не производя вычислений, определите знак изменения энтропии для процесса:
а) CO2(к) 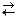 CO2(г)
CO2(г)
б) 2NH3(г) 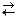 N2(г) + 3H2(г)
N2(г) + 3H2(г)
в) 2H2S(г) + 3O2(г) = 2SO2(г) + 2H2O(ж)
г) 2CH3OH(г) + 3O2(г) = 2CO2(г) + 4H2O(г)
Вариант 3
1.Пользуясь табличными значениями стандартных энтальпий образования реагирующих веществ, определите изменение стандартной энтальпии реакции
CaO + CO2 = CaCO3.
2.Почему при растворении в воде хлорида калия KCl энтропия увеличивается, а при растворении газообразного диоксида углерода CO2 – уменьшается ?
Вариант 4
- Что является термодинамическим критерием химического равновесия системы:
а) ∆Hо = 0 б) ∆Gо < 0 в) р = const г) ∆Gо = 0
- Определите теплоту образования оксида азота (I), исходя из уравнений реакций:
C + 2N2O 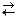 CO2 + 2N2, ∆Hо = -556,9 кДж;
CO2 + 2N2, ∆Hо = -556,9 кДж;
C + O2 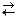 CO2, ∆Hо = -393,7 кДж.
CO2, ∆Hо = -393,7 кДж.
Вариант 5
- В каком случае возможно самопроизвольное протекание химической реакции при стандартных условиях, если ∆Hо >> T∆Sо?
а) ∆Hо > 0 , ∆Sо < 0 б) ∆Hо > 0 , ∆Sо < 0
в) ∆Hо < 0 , ∆Sо > 0 г) ∆Hо < 0 , ∆Sо < 0
Дайте подробный ответ.
- Чем отличаются термохимическая и термодинамическая системы знаков для тепловых эффектов процессов и почему ?
Вариант 6
- Исходя из теплот образования жидкой воды и водяного пара, определите теплоту испарения воды.
- Рассчитайте температуру, при которой равновероятны оба направления реакции
CuO(к) + C(графит) 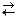 Cu(к) + CO(г)
Cu(к) + CO(г)
Вариант 7
- Вычислите стандартную энтальпию образования метилового спирта, исходя из следующих данных:
H2(г) + 1/2 O2(г) = H2O(ж), ∆H0 = -285,8 кДж;
C(гр) + O2(г) = CO2(г), ∆H0 = -393,7 кДж;
CH3OH(ж) + 3/2 O2(г) = CO2(г) + 2 H2O(ж) ∆H0 = -715,0 кДж.
- Может ли протекать реакция самопроизвольно при положительном изменении энтальпии и изменении энтропии ?
Вариант 8
- Теплота образования октана C8H18 равна 199,28 кДж/моль. Определите теплоту сгорания 1 кг октана.
(Образующуюся при сгорании воду считать жидкой).
- Какую информацию о веществе можно получить, используя значение энергии Гиббса ?
Вариант 9
- Рассчитайте термодинамические характеристики процесса термического разложения карбоната кальция СаСО3.
- Почему в уравнении для вычисления ∆G перед энтропийным фактором стоит знак минус ?
Почему этот фактор выражается произведением изменения энтропии на температуру ?
Вариант 10
1. При нейтрализации гидроксида натрия, какой массы хлороводородом по реакции
NaOH(к) + HCl(г) = NaCl(к) + H2O(ж)
выделяется 352,9 кДж теплоты ?
2. Рассчитайте температуру, при которой равновероятны оба направления реакции
2 SO2(г) + O2(г) 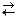 2 SO3(г).
2 SO3(г).
Вариант 11
- Рассчитайте, является ли реакция
Al2(SO4)3(к) = Al2O3(к) + 3SO3(г)
экзо- или эндотермической.
- Определите, рассчитав DS, возможность протекания реакции
2C(графит) + H2(г) = C2H2(г).
Вариант 12
- Определите знаки ∆Hо, ∆Sо и ∆Gо для реакции
AB(к) + B2(г) 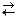 AB3(гр),
AB3(гр),
протекающей при температуре 298 К в прямом направлении.
Будет ли ∆Gо возрастать или убывать с ростом температуры ?
- Для реакций
Н2(г) + О (г) = Н2О(г) (1)
Н2(г) + 1/2О2(г) = Н2О(г) (2)
2Н(г) + О (г) = Н2О(г) (3)
укажите правильное соотношение стандартных изменений энтальпий:
а) 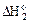 <
< 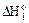 <
< 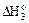 б)
б) 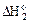 >
> 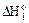 >
> 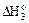
Вариант 13
- В каком из случаев:
а) ∆H < 0 , ∆S > 0; б) ∆H < 0 , ∆S < 0 или в) ∆H > 0 , ∆S > 0
реакция возможна при любых температурах ?
Ответ обоснуйте.
- Какой из оксидов – CuO или MgO – обладает наибольшим химическим сродством к серному ангидриду SO3 ?
Ответ подтвердите расчётом значений ∆Gо реакций.
Вариант 14
- Сколько теплоты выделится при сгорании 20 кг ацетилена C2H2 при стандартных условиях ?
- Если ∆H < 0 и ∆S < 0, то в каком из случаев:
а) ∆H > T ∆S или б) ∆H < T ∆S
реакция окисления (горение) ацетилена может протекать самопроизвольно ?
Вариант 15
- Исходя из теплот реакций окисления оксида мышьяка (III):
As2O3 + O2 = As2O5 (∆H0 = –271 кДж),
3As2O3 + 2O3 = 3As2O5 (∆H0 = –1096 кДж),
определите теплоту образования озона из молекулярного кислорода.
- В каком из случаев
а) ∆H > 0 , ∆S > 0, б) ∆H > 0 , ∆S < 0 или в) ∆H < 0 , ∆S < 0
реакция неосуществима при любых температурах ?
Ответ обоснуйте.
ТИПОВЫЕ ТЕСТОВЫЕ ЗАДАНИЯ
1. Теплосодержание энтальпия системы, в которой протекает экзотермическая реакция, в начальном состоянии … .
1) больше, чем в конечном
2) меньше, чем в конечном
3) одинаково с конечным
2. Для эндотермической реакции энтальпия в начальном состоянии … .
1) больше, чем в конечном
2) такая же, как конечном
3) меньше, чем в конечном
3. Реакция экзотермическая, если … .
1) ΔН = 0 2) ΔН < 0 3) ΔН > 0 4)
4. Экзотермическая реакция выражается термохимическим уравнением … .
1) А + В = С , ΔН > 0
2) А + В + Q = С
3) А + В = С , ΔН < 0
4) А + В = С – Q
5. Количество теплоты, поглощаемое при разложении 0,5 моль оксида углерода (IV) по термохимическому уравнению реакции
СО2 (г) = С (т) + О2 (г) – 393,4 кДж,
равно … кДж.
1) 98,35 2) 196,7 3) 786,8 4) 8,96
6. Теплота (энтальпия) образования сложного вещества равна … .
1) теплоте сгорания этого вещества
2) теплоте, которая выделяется или поглощается при образовании 1 моль вещества
3) теплоте разложения этого вещества
4) теплоте, которая выделяется или поглощается при образовании 1 моль этого вещества из простых веществ
7. Стандартная энтальпия образования оксида серы (IV) равна тепловому эффекту реакции … .
1) Сu2S (к) + О2 (г) = 2Сu (к) + SО2 (г)
2) S (к) + 2О (г) = SО2 (г)
3) Н2SО3 (ж) = Н2О (ж) + SО2 (г)
4) S (к) + О2 (г) = SО2 (г)
8. Понятие "теплота образования сложного вещества" относится к … .
1) 1 г вещества 2) любому количества вещества
3) 1 моль вещества 4) 100 г вещества
9. При стандартных условиях теплота образования … равна нулю.
1) О3 (г) 2) SО2 (г) 3) О2 (г) 4) СаО (т)
10. Тепловой эффект реакции
Аl2О3 + 3SО3 = Аl2(SО4)3
рассчитывают по уравнению … .
1) ΔН0 = ΔН0298, Аl2(SО4)3 + ΔН0298, Аl2О3 + 3ΔН0298, SО3
2) ΔН0 = ΔН0298, Аl2О3 + 3ΔН0298, SО3 – ΔН0298, Аl2(SО4)3
3) ΔН0 = ΔН0298, Аl2(SО4)3 – ΔН0298, Аl2О3 – ΔН0298, SО3
4) ΔН0 = ΔН0298, Аl2(SО4)3 – ΔН0298, Аl2О3 – 3ΔН0298, SО3
11. Тепловой эффект реакции
4NН3 (г) + 3О2 (г) = 2N2 (г) + 6Н2О (г)
(ΔН0298, кДж/моль: –46,2 0 0 –286)
равен … кДж.
1) –1531,2 2) –239,8 3) –1669,8 4) 1900,8
12. Изменение энтропии в химической реакции равно … .
1) сумме энтропий продуктов реакции
2) разности сумм энтропий исходных веществ и продуктов реакции
3) сумме энтропий исходных веществ
4) разности сумм энтропий продуктов реакции и исходных веществ
13. Энтропия идеально построенного кристалла при Т → 0 К стремится к … .
1) – ∞ 2) 0 3) + ∞ 4) – 273
14. Энтропия увеличивается в процессе … .
1) I2 (к) = I2 (г) 2) SО3 (г) + Н2О (ж) = Н2SО4 (ж)
3) Н2О (г) = Н2О (к) 4) N2 (г) + О2 (г) = 2NО (г)
15. Увеличение энтропии происходит в ряду превращений … .
1) Н2О (г) → Н2О (ж) → Н2О (т)
2) СО2 (г) → СО2 (т) → СО2 (г)
3) I2 (т) → I2 (ж) → I2 (г)
4) О2 (г) → О2 (ж) → О2 (г)
16. Для реакций
4Fе (к) + 3О2 (г) = 2Fе2О3 (к) ;
Н2 (г) + Сl2 (г) = 2НСl (г)
энтропия соответственно … .
1) увеличивается; практически не изменяется
2) уменьшается; увеличивается
3) увеличивается; увеличивается
4) уменьшается; практически не изменяется
17. Энергия Гиббса (изобарно-изотермический потенциал) определяется соотношением … .
1) G = Н + ТS 2) G = S + ТН
3) G = Н – ТS 4) G = S – ТН

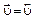
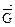 = 0
= 0