Степень окисления – это условный заряд атома в молекуле, вычисленный согласно предположению о том, что молекула состоит из ионов
Принято обозначать степень окисления римской цифрой с указанием: (+), (-).
Практическое значение окислительно – восстановительных реакций очень велико. Они лежат в основе многих таких важных промышленных процессов, как производство металлов, аммиака, серной и азотной кислот, широко используется в аналитической химии (во многих методах анализа).
1.Окислением называется процесс отдачи 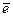 атомом, молекулой или ионом. (пи этом степень окисления повышается). Вещество, участвующее в окислении, называется восстановителем.
атомом, молекулой или ионом. (пи этом степень окисления повышается). Вещество, участвующее в окислении, называется восстановителем.
Al0 - 3 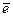 → Al3+ Fe2+ -
→ Al3+ Fe2+ - 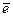 = Fe3+
= Fe3+
H2 - 2 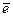 = 2H+ 2Cl- - 2
= 2H+ 2Cl- - 2 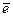 = Cl2
= Cl2
2. Восстановлением называется процесс присоединения 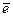 атомом, молекулой или ионом (С.О. при этом понижается). Вещество, участвующее в восстановлении, называется окислителем.
атомом, молекулой или ионом (С.О. при этом понижается). Вещество, участвующее в восстановлении, называется окислителем.
S0 + 2 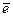 = S2-
= S2-
Cl2 + 2 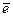 → 2Cl-
→ 2Cl-
Окисление и восстановление – взаимосвязанные процессы, так как вещества могут отдавать электроны только в том случае, если в реакции участвует другое вещество, способное электроны принимать, что определяет закон сохранения заряда в химических реакциях.
Окислителями являются:
1. Все атомы неметаллов. Окислительные свойства могут проявлять как простые, так и сложные вещества. К типичным (сильным) окислителям относятся галогены ( фтор, хлор и др. ), кислород, а также КС1О3, НС1О3, НNО3, Н2SО4 (конц.), МпО2, КMпО4, К2Сг2О7, РbО2 и др.
Восстановителями являются:
1. Атомы всех элементов, кроме He, Ne, Ar, F. Наиболее легко теряют электроны атомы тех элементов, которые на последнем слое имеют один, два, три электрона.
2. Положительно заряженные ионы металлов, находящиеся в низкой степени окисления, например:
Fe+2, Cr+3, Mn+2, Sn+2, Cu+1.
3. Отрицательно заряженные ионы, например Cl- , Br-, I-, S-2.
4. Слабые кислоты и их соли, например: H2SO3, K2SO3, HNO2 и KNO2
Составление уравнений окислительно – восстановительных реакций.
Составляя уравнение окислительно – восстановительной реакции следует сначала установить функции реагентов ( окислитель, восстановитель, среду ). Подбор коэффициентов в уравнении основан на том, что в результате реакции происходит перераспределение зарядов. Число электронов, отданных восстановителем, равно числу электронов, принятых окислителем.
Для подбора коэффициентов в уравнениях реакций окисления – восстановления используют метод электронного баланса.
Метод электронного баланса.
Последовательность составления окислительно-восстановительной реакции складываются из следующих этапов:
Записывают формулы реагентов и продукты реакции, находят элементы, повышающие и понижающие свои степени окисления и восстановления, и выписывают их отдельно, например:
МпСО3 + КС1О3 → МпО2 + КС1 + СО2
С1 5+ → С1-1
Мп+2 → Мп+4
С1+5… + 6е = С1-1 1
Мп+2 – 2е = Мп+4 3
По найденным множителям определяют стехиометрические коэффициенты для уравнения реакции ( коэффициент 1 опускается, но подразумевается ) :
3МпСО3 + КС1О3 = 3МпО2 + КС1 + СО2
Уравнивают числа атомов элементов, не изменивших своих степеней окисления. Получают уравнение окислительно-восстановительной реакции:
3МпСО3 + КС1О3 = 3 МпО2 + КС1 + 3 СО2
Рассмотрим этот же приём для реакции:
K+2Cr+62O72- + 7H2+S+6O2+4+ 3K+2S2-→ 4K+2S6-O2-4+ Cr23+(S6+O2-4)3+ 3S0+ 7H+2O2-
 Cr6+- 3
Cr6+- 3 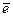 → Cr3+ 2 –
→ Cr3+ 2 –
S2- + 2 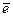 → S0 3 –
→ S0 3 –
10Fe2+S6+O2-4 +2K+Mn+7O4 +8H2SO4 → 5Fe+32(SO4)3 +2Mn+2SO4 +K2SO4 + 8H2O
 Mn+7 + 5
Mn+7 + 5 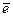 → Mn+2 2
→ Mn+2 2
2I- - 2 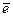 → I20 5
→ I20 5
Для того, чтобы определить степени окисления элементов в окислительно-восстановительной реакции, необходимо иметь ввиду:
Постоянную степень окисления имеют:
.1. Щелочные металлы - (+1 )
2. щелочно-земельные - (+2 )
3. галогены (ионы) - (-1 )
4. водород в соединениях - (+1 ), исключения : гидриды
металлов КН, СаН2 ( -1 )
5. кислород О (-2), исключения : перекисные соединения Н2О2N,а2О2 , - (-1),
ДОМАШНЕЕ ЗАДАНИЕ:
1. Контрольные вопросы :
1.1. Какие реакции относят к окислительно-восстановительным?
1.2. Что такое окисление? Привести примеры.
1.3 Что такое восстановление? Привести примеры.
1.4 Как изменяется степень окисления элементов при окислении и восстановлении? Привести примеры.
1.5 Что такое степень окисления ?
2. Определить степень окисления каждого элемента в соединениях :
К2Сг2О7; КмпО4; К2МпО4; А12 (SО4)3; Си SО4 К2 S
ЛИТЕРАТУРА
4. Ищенко А.А. Аналитическая химия.М.»Академия». 2008.
5. Барсукова З.А. Аналитическая химия.М.Иысш.шк.,1989.
6. Лурье Ю.Ю. Справочник по аналитической химии. М. Химия.1985.
