Полярность бокового радикала
.По этому признаку различают следующие 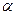 -аминокислоты:
-аминокислоты:
• с неполярными (гидрофобными) радикалами (предпочтительное связывание с неполярными молекулами).Это восемь 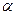 -аминокислот: аланин, валин, лейцин, изолейцин, пролин, фенилаланин, триптофан и метионин.
-аминокислот: аланин, валин, лейцин, изолейцин, пролин, фенилаланин, триптофан и метионин.
• с полярными (гидрофильными) радикалами (предпочтительное связывание с водой). По способности к ионизации в условиях организма полярные функциональные группы разделяют на ионогенные (фенольный гидроксил тирозина, тиольная группа цистеина; карбоксильная группа в глутаминовой и аспарагиновой кислотах способны образовывать анионы, а аминогруппа лизина, гуанидиновая группировка аргинина и пиридиновый атом азота имидазольного кольца гистидина — катионы) и неионогенные (ОН- серина и треонина, амидные группы аспарагина и глутамина).

3) Число кислотных и основных функциональных групп. В зависимости от этого 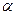 -аминокислоты разделяют на:
-аминокислоты разделяют на:
• нейтральные (одна аминогруппа и одна карбоксильная группа);
• кислые (одна аминогруппа и две карбоксильные группы);
• основные (две группы основного характера и одна карбоксильная). Такие аминокислоты различаются значениями изоэлектрической точки pI.

Нейтральные 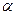 -аминокислоты. Аминокислоты, имеющие боковой радикал без дополнительных функциональных групп, характеризуются значениями pI, находящимися в слабокислой области около 6. Это обусловлено большей способностью карбоксильной группы к ионизации, чем аминогруппы к протонированию.
-аминокислоты. Аминокислоты, имеющие боковой радикал без дополнительных функциональных групп, характеризуются значениями pI, находящимися в слабокислой области около 6. Это обусловлено большей способностью карбоксильной группы к ионизации, чем аминогруппы к протонированию.
При наличии в радикале слабокислотных функциональных групп (гидроксильная, тиольная, амидная группы) значения pI сдвигаются в более кислую область от 5,0 до 5,7 (см. табл. ). В изоэлектрической точке наблюдается максимальное содержание диполярного иона, в сильнощелочных средах (рН >12) преобладают анионные формы, а в сильнокислых (рН 1—2) — катионные формы.
Катионная форма аминокислоты является двухосновной кислотой (по Брёнстеду), содержащей два кислотных центра: недиссоциированную карбоксильную группу и протонированную аминогруппу, характеризующиеся соответствующими значениями рКа. При изменении рН среды диссоциирует карбоксильная группа и образуется диполярный ион, являющийся слабой одноосновной кислотой с одним кислотным центром — протонированной аминогруппой.

Значение рН, при котором концентрация катионной формы будет равна концентрации диполярного иона, соответствует значению рКа карбоксильной группы.Для аланина это значение будет равно 2,3 (табл.). При дальнейшем увеличении рН среды уменьшается концентрация катионной формы и нарастает концентрация диполярного иона, которая максимальна в изоэлектрической точке. При изменении значений рН от изоэлектрической точки в щелочную область снижается концентрация диполярного иона и возрастает концентрация анионной формы.
Значение рН, при котором концентрация диполярного иона будет равна концентрации анионной формы, соответствует значению рКа протонированной аминогруппы.
Для аланина это значение составляет 9,7 (см. табл.).
Концентрация диполярного иона максимальна на «середине пути» между pKа1 и рКа2 (см. табл). Для вычисления изоэлектрической точки нейтральных аминокислот значения рКа1 и рКа2 суммируют и делят пополам. Таким образом, у аланина рI= 1/2 (2,3 + 9,7) = 6,0.
Поскольку суммарный заряд молекулы аминокислоты в изоэлектрической точке равен нулю, диполярные ионы в электрическом поле не перемещаются. При значениях рН среды ниже значения рI катионная форма аминокислоты движется к катоду, а при рН выше, чем рI, анионная форма аминокислоты перемешается к аноду. На этом основано разделение аминокислот методом электрофореза.

Рис. Зависимость ионного состояния аланина от рН среды
Кислые и основные 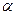 - аминокислоты
- аминокислоты



Таблица. Кислотно-основные свойства важнейших 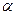 -аминокислот
-аминокислот


