Общие свойства металлов. Коррозия
Элементы с металлическими свойствами расположены вIA – VIA группах Периодической системы (табл. 7).
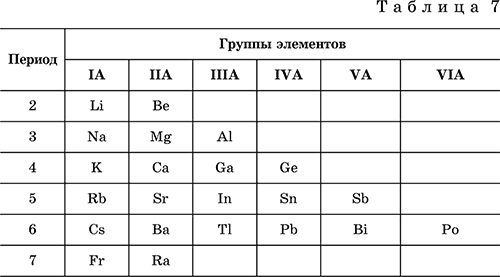
Металлами являются также все элементы, расположенные вIБ – VIIIБ‑группах (переходные металлы).
В настоящее время в Периодической системе 92 металла.
Типичными металлами являются s‑элементы (элементы IA‑группы от Li до Fr, элементы IIA‑группы от Mg до Ra). Общая электронная формула их атомов ns1–2. Для них характерны степени окисления +I и +II соответственно.
Небольшое число электронов (1–2) на внешнем энергетическом уровне атомов типичных металлов предполагает легкую потерю этих электронов и проявление сильных восстановительных свойств, что отражают низкие значения электроотрицательности. Отсюда вытекает ограниченность химических свойств и способов получения типичных металлов.
Характерной особенностью типичных металлов является стремление их атомов образовывать катионы и ионные химические связи с атомами неметаллов. Соединения типичных металлов с неметаллами – это ионные кристаллы «катион металлаанион неметалла», например К+Br‑, Са2+O2‑. Катионы типичных металлов входят также в состав соединений со сложными анионами – гидроксидов и солей, например Mg2+(OH‑)2, (Li+)2CO32‑.
Металлы А‑групп, образующие диагональ амфотерности в Периодической системе Be‑Al‑Ge‑Sb‑Po, а также примыкающие к ним металлы (Ga, In, Tl, Sn, Pb, Bi) не проявляют типично металлических свойств. Общая электронная формула их атомов ns2np0–4 предполагает большее разнообразие степеней окисления, большую способность удерживать собственные электроны, постепенное понижение их восстановительной способности и появление окислительной способности, особенно в высоких степенях окисления (характерные примеры – соединения ТlIII, PbIV, Biv). Подобное химическое поведение характерно и для большинства d‑элементов, т. е. элементов Б‑групп Периодической системы (типичные примеры – амфотерные элементы Cr и Zn).
Это проявление двойственности (амфотерности) свойств, одновременно металлических (основных) и неметаллических, обусловлено характером химической связи. В твердом состоянии соединения нетипичных металлов с неметаллами содержат преимущественно ковалентные связи (но менее прочные, чем связи между неметаллами). В растворе эти связи легко разрываются, а соединения диссоциируют на ионы (полностью или частично). Например, металл галлий состоит из молекул Ga2, в твердом состоянии хлориды алюминия и ртути(II) AlCl3 и HgCl2 содержат сильно ковалентные связи, но в растворе AlCl3 диссоциирует почти полностью, a HgCl2 – в очень малой степени (да и то на ионы HgCl+ и Cl‑).
В свободном виде все металлы – твердые вещества, кроме одного – ртути Hg, которая при обычных условиях жидкость. В кристаллах металлов преобладает особый вид связи (металлическая связь); валентные электроны слабо связаны с конкретным атомом в решетке, и внутри металла существует так называемый электронный газ. Все металлы обладают высокой электропроводимостью (наибольшая y Ag, Cu, Аи, Al, Mg) и теплопроводностью. Встречаются низкоплавкие металлы (цезий Cs с температурой плавления 28,7 °C плавится от тепла руки) и, наоборот, весьма тугоплавкие (вольфрам W плавится лишь при 3387 °C). Отличительным свойством металлов служит их пластичность (ковкость), вследствие чего они могут быть прокатаны в тонкие листы – фольгу (Sn, Al, Au) или вытянуты в проволоку (Cu, Al, Fe), однако встречаются и очень хрупкие металлы (Zn, Sb, Bi).
В промышленности часто используют не чистые металлы, а их смеси – сплавы, в которых полезные свойства одного металла дополняются полезными свойствами другого. Так, медь обладает невысокой твердостью и малопригодна для изготовления деталей машин, сплавы же меди с цинком (латунь) являются уже достаточно твердыми и широко используются в машиностроении. Алюминий обладает высокой пластичностью и достаточной легкостью (малой плотностью), но слишком мягок. На его основе готовят сплав с магнием, медью и марганцем – дуралюмин (дюраль), который, не теряя полезных свойств алюминия, приобретает высокую твердость и становится пригодным в авиастроении. Сплавы железа с углеродом (и добавками других металлов) – это широко известные чугун и сталь.
Металлы в свободном виде являются восстановителями. Однако реакционная способность некоторых металлов невелика из‑за того, что они покрыты поверхностной оксидной пленкой, в разной степени устойчивой к действию таких химических реактивов, как вода, растворы кислот и щелочей.
Например, свинец всегда покрыт оксидной пленкой, для его перехода в раствор требуется не только воздействие реактива (например, разбавленной азотной кислоты), но и нагревание. Оксидная пленка на алюминии препятствует его реакции с водой, но под действием кислот и щелочей разрушается. Рыхлая оксидная пленка {ржавчина), образующаяся на поверхности железа во влажном воздухе, не мешает дальнейшему окислению железа.
Под действием концентрированных кислот на металлах образуется устойчивая оксидная пленка. Это явление называется пассивацией. Так, в концентрированной серной кислоте пассивируются (и после этого не реагируют с кислотой) такие металлы, как Be, Bi, Со, Fe, Mg и Nb, а в концентрированной азотной кислоте – металлы Al, Be, Bi, Со, Cr, Fe, Nb, Ni, Pb, Th и U.
При взаимодействии с окислителями в кислых растворах большинство металлов переходит в катионы, заряд которых определяется устойчивой степенью окисления данного элемента в соединениях (Na+, Са2+, Al3+, Fe2+ и Fe3+).
Восстановительная активность металлов в кислом растворе передается рядом напряжений. Большинство металлов переводится в раствор соляной и разбавленной серной кислотами, но Cu, Ag и Hg – только серной (концентрированной) и азотной кислотами, a Pt и Аи – «царской водкой».
Нежелательным химическим свойством металлов является их коррозия, т. е. активное разрушение (окисление) при контакте с водой и под воздействием растворенного в ней кислорода (кислородная коррозия). Например, широко известна коррозия железных изделий в воде, в результате чего образуется ржавчина, и изделия рассыпаются в порошок.
Коррозия металлов протекает в воде также из‑за присутствия растворенных газов СO2 и SO2; создается кислотная среда, и катионы Н+ вытесняются активными металлами в виде водорода Н2 (водородная коррозия).
Особенно коррозионно‑опасным может быть место контакта двух разнородных металлов (контактная коррозия). Между одним металлом, например Fe, и другим металлом, например Sn или Cu, помещенными в воду, возникает гальваническая пара. Поток электронов идет от более активного металла, стоящего левее в ряду напряжений (Fe), к менее активному металлу (Sn, Cu), и более активный металл разрушается (корродирует).
Именно из‑за этого ржавеет луженая поверхность консервных банок (железо, покрытое оловом) при хранении во влажной атмосфере и небрежном обращении с ними (железо быстро разрушается после появления хотя бы небольшой царапины, допускающей контакт железа с влагой). Напротив, оцинкованная поверхность железного ведра долго не ржавеет, поскольку даже при наличии царапин корродирует не железо, а цинк (более активный металл, чем железо).
Сопротивление коррозии для данного металла усиливается при его покрытии более активным металлом или при их сплавлении; так, покрытие железа хромом или изготовление сплава железа с хромом устраняет коррозию железа. Хромированное железо и сталь, содержащая хром (нержавеющая сталь), имеют высокую коррозионную стойкость.
Общие способы получения металлов в промышленности:
• электрометаллургия, т. е. получение металлов электролизом расплавов (для наиболее активных металлов) или растворов солей;
• пирометаллургия, т. е. восстановление металлов из руд при высокой температуре (например, получение железа в доменном процессе);
• гидрометаллургия, т. е. выделение металлов из растворов их солей более активными металлами (например, получение меди из раствора CuSO4 действием цинка, железа или алюминия).
В природе иногда встречаются самородные металлы (характерные примеры – Ag, Au, Pt, Hg), но чаще металлы находятся в виде соединений (металлические руды). По распространенности в земной коре металлы различны: от наиболее распространенных – Al, Na, Са, Fe, Mg, К, Ti до самых редких – Bi, In, Ag, Au, Pt, Re.
Примеры заданий части A
1. В железосодержащих продуктах реакций между железом и разбавленными кислотами HCl, H2SO4 и HNO3 общая сумма числа атомов всех элементов равна
1) 14
2) 18
3) 22
4) 26
2. В уравнениях реакций
Fe + O2 → (FeIIFeIII2)O4
Fe + Cl2 → FeCl3
Fe + Н2O (пар) → (FeIIFeIII2)O4 + Н2
общая сумма коэффициентов равна
1) 6
2) 7
3) 12
4) 25
3. Соль NaCrO2 получают при взаимодействии между
1) CrO3 и Na2O
2) Cr2O3 и Na2CO3
3) CrО и NaOH
4) CrO2 и NaHCO3
4. Будет протекать реакция при внесении меди в разбавленные растворы
1) бромоводорода
2) нитрата ртути(II)
3) серной кислоты
4) азотной кислоты
5. Протекают реакции
1) H2SO4 + FeCO3 →…
2) AgNO3 + HI (p‑p) →…
3) K2Cr2O7 (p‑p) + PbO2 →…
4) AgNOg (p‑p) + Au →…
6–9. Масса тигля из
6. платины
7. меди
8. серебра
9. железа
при прокаливании на воздухе
1) уменьшается
2) увеличивается
3) не изменяется
4) не знаю
10–11. В молекулярных уравнениях реакций
10. Fe2O3 + HNOg →…, Fe(OH)2 + O2 → FeO(OH) +…
11. CuO + С → CO2 + Cu, Fe2O3 + CO → Fe +…
общая сумма коэффициентов равна
1) 12
2) 15
3) 16
4) 22
12. Сплав, оба компонента которого реагируют с концентрированной азотной кислотой, – это
1) Al + Cu
2) Pt + Аu
3) Hg + Ag
4) Fe + Cr
13. He протекает реакция замещения между реагентами
1) CuSO4 и Zn
2) Pb(NO3)2 и Cr
3) Fe и ZnSO4
4) Cd и Hg(NO3)2
14. Для удаления примеси NiSO4 из раствора FeSO4 надо добавить
1) хлорид бария
2) нитрат серебра(I)
3) гидроксид калия
4) железо
15. Пластинка металла окажется покрытой другим металлом, взятым в виде раствора соли, в наборах
1) Zn и Pb(NO3)2
2) Cu и Hg(NO3)2
3) Со и MnSO4
4) Pb и CrCl3
16–17. Коррозия стального изделия, склепанного с
16. хромом
17. никелем
во влажном воздухе
1) усиливается
2) ослабевает
3) не изменяется
4) не знаю
7. Неметаллы главных подгрупп IV–VII групп
Водород
Водород – первый элемент Периодической системы (1‑й период, порядковый номер 1). Не имеет полной аналогии с остальными химическими элементами и не принадлежит ни к какой группе (в таблицах условно помещается в IA– и/или в VIIA‑группу).
Атом водорода наименьший по размерам и самый легкий среди атомов всех элементов. Электронная формула атома 1s1, характерные степени окисления 0, +I и реже – I. Состояние HI считается устойчивым (соединения с H‑I – сильные восстановители).
Шкала степеней окисления водорода:
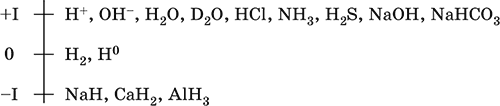
По электроотрицательности (2,10) водород занимает промежуточное положение между типичными металлами и типичными неметаллами. Проявляет амфотерные свойства – металлические и неметаллические. Входит в состав катионов (катионы оксония Н3O+ и аммония NH4+, аквакатионы металлов) и многочисленных анионов – кислых кислотных остатков (HS‑, HCO3‑ и др.).
Природный водород содержит изотоп 1Н – протий с примесью стабильного изотопа 2H(D) – дейтерия и следами радиоактивного изотопа 3Н(Т) – трития (на Земле всего 2 кг трития). В химии символом Н в формулах веществ обозначается содержащаяся в них природная смесь изотопов с преобладанием изотопа протий, а сами вещества рассматриваются как почти изотопночистые соединения протия.
Водород – наиболее распространенный элемент в космосе (Солнце, большие планеты Юпитер и Сатурн, звезды, межзвездная среда, туманности); в состав космической материи входит 63 % Н, 36 % Не и 1 % всех остальных элементов.
В природе – третий по химической распространенности элемент (после О и Si), основа гидросферы. Встречается в химически связанном виде (вода, живые организмы, нефть, природный уголь, минералы), содержится в верхних слоях атмосферы.
Водород Н2. Простое вещество. Бесцветный газ без запаха и вкуса. Молекула содержит ковалентную σ‑связь Н – Н. Очень легкий, термически устойчивый до 2000 °C. Весьма мало растворим в воде. Хемосорбируется металлами Fe, Ni, Pd, Pt, где находится в атомном состоянии.
Водород Н2 может проявлять в одних условиях восстановительные свойства (чаще), в других – окислительные свойства (реже):
восстановитель Н20 – 2е‑ = 2НI
окислитель Н20 + 2е‑ = 2Н‑I
Сильный восстановитель при высоких температурах, водород реагирует с неметаллами и оксидами малоактивных металлов, выполняет роль окислителя в реакциях с типичными металлами:
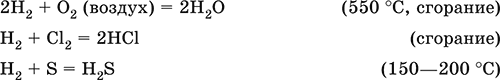

Очень высокой восстановительной способностью обладает атомарный водород Н0 (водород in statu nascendi, лат., – в момент возникновения), который получают непосредственно в зоне проводимой реакции (время жизни Н0 0,5 с); например, гранулы магния вносят в подкисленный раствор переманганата калия, протекают реакции:
а) образование атомарного водорода
Mg + 2Н+ = Mg2+ + 2Н0
б) восстановление перманганат‑иона атомарным водородом
5Н0 + 3H+ + MnO4‑ = Mn2+ + 4Н2O
Другой пример – восстановление нитробензола в анилин (реакция Зинина):
а) Fe + 2Н+ = Fe2+ + 2Н0
б) C6H5NO2 + 6Н0 = C6H5NH2 + 2Н2O
Получить атомарный водород можно также пропусканием водорода Н2 над никелевым катализатором.
Атомарный водород легко восстанавливает при комнатной температуре весьма устойчивые соединения, например KNO3 и O2:
2Н0 (Zn, разб. HCl) + KNO3 = KNO2 + H2O
2H0 (Zn, разб. HCl) + O2 = Н2O2
Аналогично протекают реакции при использовании амфигенов (Zn, Al) в щелочной среде:
а) Zn + 2OH‑ + 2H2O = [Zn(OH)4]2‑ + 2Н0
б) 8Н0 + KNO3 = NH3↑ + КОН + 2Н2O (кипячение)
Качественная реакция – сгорание собранного в пробирку водорода с «хлопком» («гремучая» смесь с воздухом при содержании Н2 4–74 % по объему).
Применяется водород как восстановитель и гидрирующий агент в синтезе технически важных продуктов (редкие металлы, NH3, НCl, органические вещества).
Вода Н2O. Бинарное соединение. Бесцветная жидкость (слой более 5 м толщиной окрашен в голубой цвет), без вкуса и запаха. Молекула имеет строение дважды незавершенного тетраэдра [:: ОН2] (sр3‑гибридизация). Летучее вещество, термически устойчивое до 1000 °C.
В обычных условиях полярные молекулы воды образуют между собой водородные связи. Это обусловливает аномалию температур плавления и кипения воды – они значительно выше, чем у ее химических аналогов (H2S и других). Затвердевание воды в лед сопровождается увеличением объема на 9 %, т. е. лед легче жидкой воды (вторая аномалия воды). Наибольшую плотность вода имеет не при 0 °C, а при 4 °C (третья аномалия воды). Твердая вода (лед) легко возгоняется.
Природная вода по изотопному составу водорода в основном 1Н2O с примесью 1Н2НО и 2Н2O, по изотопному составу кислорода в основном Н216O с примесью Н218O и Н217O. В малой степени подвергается диссоциации до Н+, или, точнее, до Н3O+, и ОН; очень слабый электролит. Катион оксония Н3O+ имеет строение незавершенного тетраэдра [: O(Н)3] (sр3‑гибридизация). Образует кристаллогидраты со многими солями, аквакомплексы – с катионами металлов. Реагирует с металлами, неметаллами, оксидами. Вызывает электролитическую диссоциацию кислот, оснований и солей, гидролизует многие бинарные соединения и соли. Подвергается электролизу в присутствии сильных электролитов. Почти универсальный жидкий растворитель неорганических веществ.
Для химических целей природную воду очищают перегонкой (дистиллированная вода), для промышленных целей умягчают, устраняя «временную» и «постоянную» жесткость, или полностью обессоливают, пропуская через иониты в кислотной Н+‑форме и щелочной ОН‑ – форме (ионы солей осаждаются на ионитах, а ионы Н+ и ОН‑ переходят в воду и взаимно нейтрализуются). Питьевую воду обеззараживают хлорированием (старый способ) или озонированием (современный, но дорогой способ; озон не только окисляет вредные примеси подобно хлору, но и увеличивает содержание растворенного кислорода).
Уравнения важнейших реакций:
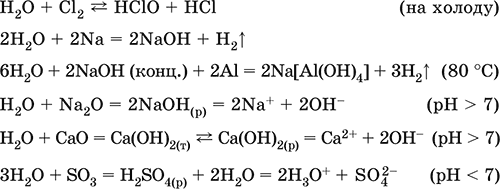
Примеры гидролиза бинарных соединений:
6H2O + Al2S3 = 2Al(ОН)3↓ + 3H2S↑
2H2O + SF4 = SO2↑ + 4HF↑ (40–60 °C)
6H2O + Mg3N2 = 3Mg(OH)2↓ + 2NH3↑ (кипячение)
2H2O + CaC2 = Ca(OH)2↓ + C2H2↑
Вода – окислитель за счет HI:
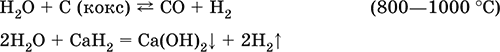
Электролиз воды:
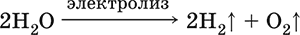
Электропроводность чистой (дистиллированной) воды весьма мала, поэтому электролиз проводят в присутствии сильных электролитов.
а) в нейтральном растворе (электролит Na2SO4)
катод 2H2O + 2е‑ = H2↑ + 2OH
анод 2Н2O – 4е‑ = O2↑ + 4H+
раствор ОН‑ + Н+ = Н2O
б) в кислом растворе (электролит H2SO4)
катод 2Н+ + 2е‑ = Н2↑
анод 2Н2O – 4е‑ = O2↑ + 4Н+
в) в щелочном растворе (электролит NaOH)
катод 2Н2O + 2е‑ = Н2↑ + 2OН‑
анод 4OН‑ – 4е‑ = O2↑ + 2Н2O
Один из методов обнаружения воды основан на переходе во влажной атмосфере белого сульфата меди(II) CuSO4 в голубой медный купорос CuSO4 5Н2O.
Известна изотопная разновидность воды – тяжелая вода D2O (2Н2O); в природных водах массовое отношение D2O: Н2O = 1: 6000.
Плотность, температуры плавления и кипения тяжелой воды выше, чем у обыкновенной. Растворимость большинства веществ в тяжелой воде значительно меньше, чем в обычной воде. Она ядовита, так как замедляет биологические процессы в живых организмах. Тяжелая вода накапливается в остатке электролита при многоразовом электролизе воды. Используется как теплоноситель и замедлитель нейтронов в ядерных реакторах.
Гидрид кальция СаН2. Бинарное соединение. Белый, имеет ионное строение Са2+(Н‑)2. При плавлении разлагается. Чувствителен к кислороду воздуха. Сильный восстановитель, реагирует с водой, кислотами. Применяется как твердый источник водорода (1 кг СаН2 дает 1000 л Н2), осушитель газов и жидкостей, аналитический реагент для количественного определения воды в кристаллогидратах.
Уравнения важнейших реакций:
СаН2 = Н2 + Са (особо чистый) (выше 1000 °C)
СаН2 + 2Н2O = Са(ОН)2 + 2Н2↑
СаН2 + 2НCl (разб.) = СаCl2 + 2Н2↑
СаН2 + O2 = Н2O + СаО (особо чистый) (300–400 °C)
ЗСаН2 + N2 = ЗН2 + Ca3N2 (выше 1000 °C)
ЗСаН2 + 2КClO3 = 2КCl + ЗСаО + ЗН2O (450–550 °C)
СаН2 + H2S = CaS + 2Н2 (500–600 °C)
Получение: обработка нагретого кальция водородом.
Галогены
Хлор. Хлороводород
Хлор – элемент 3‑го периода и VII А‑группы Периодической системы, порядковый номер 17. Электронная формула атома [10Ne]3s23p5, характерные степени окисления 0, ‑I, +I, +V и +VII. Наиболее устойчиво состояние Cl‑I. Шкала степеней окисления хлора:

Хлор обладает высокой электроотрицательностью (2,83), проявляет неметаллические свойства. Входит в состав многих веществ – оксидов, кислот, солей, бинарных соединений.
В природе – двенадцатый по химической распространенности элемент (пятый среди неметаллов). Встречается только в химически связанном виде. Третий по содержанию элемент в природных водах (после О и H), особенно много хлора в морской воде (до 2 % по массе). Жизненно важный элемент для всех организмов.
Хлор Cl2. Простое вещество. Желто‑зеленый газ с резким удушливым запахом. Молекула Cl2 неполярна, содержит σ‑связь CI–Cl. Термически устойчив, негорюч на воздухе; смесь с водородом взрывается на свету (водород сгорает в хлоре):
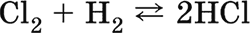
Хорошо растворим в воде, подвергается в ней дисмутации на 50 % и полностью – в щелочном растворе:
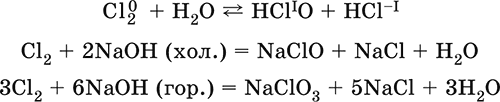
Раствор хлора в воде называют хлорной водой, на свету кислота НClO разлагается на НCl и атомарный кислород О0, поэтому «хлорную воду» надо хранить в темной склянке. Наличием в «хлорной воде» кислоты НСlO и образованием атомарного кислорода объясняются ее сильные окислительные свойства: например, во влажном хлоре обесцвечиваются многие красители.
Хлор очень сильный окислитель по отношению к металлам и неметаллам:
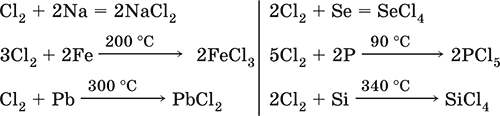
Реакции с соединениями других галогенов:
а) Cl2 + 2KBr(p) = 2КCl + Br2↑ (кипячение)
б) Cl2 (нед.) + 2KI(p) = 2КCl + I2↓
3Cl2 (изб.) + ЗН2O + KI = 6НCl + КIO3 (80 °C)
Качественная реакция – взаимодействие недостатка Cl2 с KI (см. выше) и обнаружение иода по синему окрашиванию после добавления раствора крахмала.
Получение хлора в промышленности:
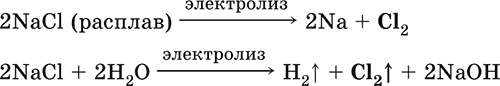
и в лаборатории:
4НCl (конц.) + MnO2 =Cl2↑ + MnCl2 + 2Н2O
(аналогично с участием других окислителей; подробнее см. реакции для НCl и NaCl).
Хлор относится к продуктам основного химического производства, используется для получения брома и иода, хлоридов и кислородсодержащих производных, для отбеливания бумаги, как дезинфицирующее средство для питьевой воды. Ядовит.
Хлороводород НCl. Бескислородная кислота. Бесцветный газ с резким запахом, тяжелее воздуха. Молекула содержит ковалентную σ‑связь Н – Cl. Термически устойчив. Очень хорошо растворим в воде; разбавленные растворы называются хлороводородной кислотой, а дымящий концентрированный раствор (35–38 %) – соляной кислотой (название дано еще алхимиками). Сильная кислота в растворе, нейтрализуется щелочами и гидратом аммиака. Сильный восстановитель в концентрированном растворе (за счет Cl‑I), слабый окислитель в разбавленном растворе (за счет НI). Составная часть «царской водки».
Качественная реакция на ион Cl‑ – образование белых осадков AgCl и Hg2Cl2, которые не переводятся в раствор действием разбавленной азотной кислоты.
Хлороводород служит сырьем в производстве хлоридов, хлорорганических продуктов, используется (в виде раствора) при травлении металлов, разложении минералов и руд.
Уравнения важнейших реакций:
НCl (разб.) + NaOH (разб.) = NaCl + Н2O
HCl (разб.) + NH3 H2O = NH4Cl + Н2O
4HCl (конц., гор.) + МО2 = МCl2 + Cl2↑ + 2H2O (М = Mn, Pb)
16HCl (конц., гор.) + 2КMnO4(т) = 2MnCl2 + 5Cl2↑ + 8H2O + 2КCl
14HCl (конц.) + К2Cr2O7(т) = 2CrCl3 + ЗCl2↑ + 7H2O + 2КCl
6HCl (конц.) + КClO3(т) = КCl + ЗCl2↑ + 3H2O (50–80 °C)
4HCl (конц.) + Са(ClO)2(т) = СаCl2 + 2Cl2| + 2Н2O
2HCl (разб.) + М = МCl2 + H2↑ (М = Fe, Zn)
2HCl (разб.) + МСO3 = МCl2 + СO2↑ + H2O (М = Са, Ва)
HCl (разб.) + AgNO3 = HNO3 + AgCl↓
Получение НCl в промышленности – сжигание Н2 в Cl2 (см.), в лаборатории – вытеснение из хлоридов серной кислотой:
NaCl(т) + H2SO4 (конц.) = NaHSO4 + НCl↑ (50 °C)
2NaCl(т) + H2SO4 (конц.) = Na2SO4 + 2НCl↑ (120 °C)
Хлориды
Хлорид натрия NaCl. Бескислородная соль. Бытовое название поваренная соль. Белый, слабогигроскопичный. Плавится и кипит без разложения. Умеренно растворим в воде, растворимость мало зависит от температуры, раствор имеет характерный соленый вкус. Гидролизу не подвергается. Слабый восстановитель. Вступает в реакции ионного обмена. Подвергается электролизу в расплаве и растворе.
Применяется для получения водорода, натрия и хлора, соды, едкого натра и хлороводорода, как компонент охлаждающих смесей, пищевой продукт и консервирующее средство.
В природе – основная часть залежей каменной соли, или галита, и сильвинита (вместе с КCl), рапы соляных озер, минеральных примесей морской воды (содержание NaCl = 2,7 %). В промышленности получают выпариванием природных рассолов.
Уравнения важнейших реакций:
2NaCl(т) + 2H2SO4 (конц.) + MnO2(т) = Cl2↑ + MnSO4 + 2Н2O + Na2SO4 (100 °C)
10NaCl(т) + 8H2SO4 (конц.) + 2КMnO4(т) = 5Cl2↑ + 2MnSO4 + 8Н2O + 5Na2SO4 + K2SO4 (100 °C)
6NaCl(т) + 7H2SO4 (конц.) + К2Cr2O7(т) = ЗCl2 + Cr2(SO4)3 + 7Н2O + 3Na2SO4 + K2SO4 (100 °C)
2NaCl(т) + 4H2SO4 (конц.) + РЬO2(т) = Cl2↑ + Pb(HSO4)2 + 2Н2O + 2NaHSO4 (50 °C)
NaCl (разб.) + AgNO3 = NaNO3 + AgCl↓
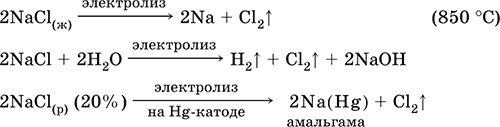
Хлорид калия KCl. Бескислородная соль. Белый, негигроскопичный. Плавится и кипит без разложения. Умеренно растворим в воде, раствор имеет горький вкус, гидролиза нет. Вступает в реакции ионного обмена. Применяется как калийное удобрение, для получения К, КОН и Cl2. В природе основная составная часть (наравне с NaCl) залежей сильвинита.
Уравнения важнейших реакций одинаковы с таковыми для NaCl.
Хлорид кальция СаCl2. Бескислородная соль. Белый, плавится без разложения. Расплывается на воздухе за счет энергичного поглощения влаги. Образует кристаллогидрат СаCl2 6Н2O с температурой обезвоживания 260 °C. Хорошо растворим в воде, гидролиза нет. Вступает в реакции ионного обмена. Применяется для осушения газов и жидкостей, приготовления охлаждающих смесей. Компонент природных вод, составная часть их «постоянной» жесткости.
Уравнения важнейших реакций:
СаCl2(т) + 2H2SO4 (конц.) = Ca(HSO4)2 + 2НCl↑ (50 °C)
СаCl2(т) + H2SO4 (конц.) = CaSO4↓ + 2НCl↑ (100 °C)
СаCl2 + 2NaOH (конц.) = Ca(OH)2↓ + 2NaCl↑
ЗСаCl2 + 2Na3PO4 = Са3(РO4)2↓ + 6NaCl
СаCl2 + К2СO3 = СаСO3↓ + 2КCl
СаCl2 + 2NaF = CaF2↓ + 2NaCl
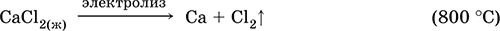
Получение:
СаСO3 + 2HCl = СаCl2 + СO3↑ + Н2O
Хлорид алюминия AlCl3. Бескислородная соль. Белый, легкоплавкий, сильнолетучий. В паре состоит из ковалентных мономеров AlCl3 (треугольное строение, sр2‑гибридизация, преобладают при 440–800 °C) и димеров Al2Cl6 (точнее, Cl2AlCl2AlCl2, строение – два тетраэдра с общим ребром, sр3‑гибридизация, преобладают при 183–440 °C). Гигроскопичен, на воздухе «дымит». Образует кристаллогидрат, разлагающийся при нагревании. Хорошо растворим в воде (с сильным экзо‑эффектом), полностью диссоциирует на ионы, создает в растворе сильнокислотную среду вследствие гидролиза. Реагирует со щелочами, гидратом аммиака. Восстанавливается при электролизе расплава. Вступает в реакции ионного обмена.
Качественная реакция на ион Al3+ – образование осадка AlРO4, который переводится в раствор концентрированной серной кислотой.
Применяется как сырье в производстве алюминия, катализатор в органическом синтезе и при крекинге нефти, переносчик хлора в органических реакциях. Уравнения важнейших реакций:
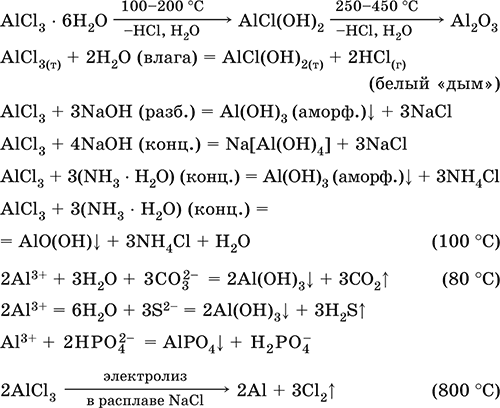
Получение AlCl3 в промышленности – хлорирование каолина, глинозёма или боксита в присутствии кокса:
Al2O3 + ЗС (кокс) + ЗCl2 = 2AlCl3 + ЗСО (900 °C)
Хлорид железа(Н) FeCl2. Бескислородная соль. Белый (гидрат голубовато‑зеленый), гигроскопичный. Плавится и кипит без разложения. При сильном нагревании летуч в потоке HCl. Связи Fe – Cl преимущественно ковалентные, пар состоит из мономеров FeCl2 (линейное строение, sp‑гибридизация) и димеров Fe2Cl4. Чувствителен к кислороду воздуха (темнеет). Хорошо растворим в воде (с сильным экзо‑эффектом), полностью диссоциирует на ионы, слабо гидролизуется по катиону. При кипячении раствора разлагается. Реагирует с кислотами, щелочами, гидратом аммиака. Типичный восстановитель. Вступает в реакции ионного обмена и комплексообразования.
Применяется для синтеза FeCl3 и Fe2O3, как катализатор в органическом синтезе, компонент лекарственных средств против анемии.
Уравнения важнейших реакций:
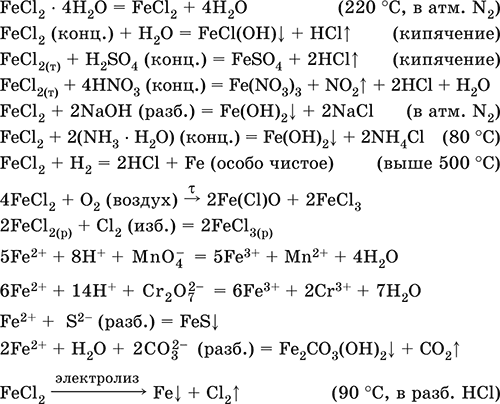
Получение: взаимодействие Fe с соляной кислотой:
Fe + 2НCl =FeCl2 + Н2↑
(в промышленности используют хлороводород и ведут процесс при 500 °C).
Хлорид железа(III) FeCl3. Бескислородная соль. Черно‑коричневый (темно‑красный в проходящем свете, зеленый в отраженном), гидрат темно‑желтый. При плавлении переходит в красную жидкость. Весьма летуч, при сильном нагревании разлагается. Связи Fe – Cl преимущественно ковалентные. Пар состоит из мономеров FeCl3 (треугольное строение, sр2‑гибридизация, преобладают выше 750 °C) и димеров Fe2Cl6 (точнее, Cl2FeCl2FeCl2, строение – два тетраэдра с общим ребром, sр3‑гибридизация, преобладают при 316–750 °C). Кристаллогидрат FeCl3 6Н2O имеет строение [Fe(H2O)4Cl2]Cl • 2Н2O. Хорошо растворим в воде, раствор окрашен в желтый цвет; сильно гидролизован по катиону. Разлагается в горячей воде, реагирует со щелочами. Слабый окислитель и восстановитель.
Применяется как хлорагент, катализатор в органическом синтезе, протрава при крашении тканей, коагулянт при очистке питьевой воды, травитель медных пластин в гальванопластике, компонент кровоостанавливающих препаратов.
Уравнения важнейших реакций:
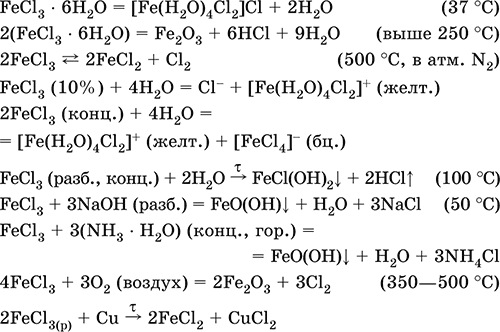
Хлорид аммония NH4Cl. Бескислородная соль, техническое название нашатырь. Белый, летучий, термически неустойчивый. Хорошо растворим в воде (с заметным эндо‑эффектом, Q = ‑16 кДж), гидролизуется по катиону. Разлагается щелочами при кипячении раствора, переводит в раствор магний и гидроксид магния. Вступает в реакцию конмутации с нитратами.
Качественная реакция на ион NH4+ – выделение NH3 при кипячении со щелочами или при нагревании с гашёной известью.
Применяется в неорганическом синтезе, в частности для создания слабокислотной среды, как компонент азотных удобрений, сухих гальванических элементов, при пайке медных и лужении стальных изделий.
Уравнения важнейших реакций:
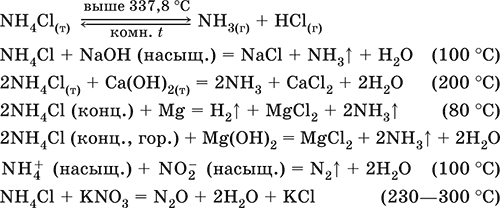
Получение: взаимодействие NH3 с HCl в газовой фазе или NH3 Н2O с HCl в растворе.
Гипохлориты. Хлораты
Гипохлорит кальция Са(СlO)2. Соль хлорноватистой кислоты HClO. Белый, при нагревании разлагается без плавления. Хорошо растворим в холодной воде (образуется бесцветный раствор), гидролизуется по аниону. Реакционноспособный, полностью разлагается горячей водой, кислотами. Сильный окислитель. При стоянии раствор поглощает углекислый газ из воздуха. Является активной составной частью хлорной (белильной) извести – смеси неопределенного состава с СаCl2 и Са(ОН)2. Уравнения важнейших реакций:
Са(ClO)2 = СаCl2 + O2 (180 °C)
Са(ClO)2(т) + 4НCl (конц.) = СаCl2 + 2Cl2↑ + 2Н2O (80 °C)
Са(ClO)2 + Н2O + СO2 = СаСO3↓ + 2НClO (на холоду)
Са(ClO)2 + 2Н2O2 (разб.) = СаCl2 + 2Н2O + 2O2↑
Получение:
2Са(ОН)2 (суспензия) + 2Cl2(г) = Са(ClO)2 + СаCl2 + 2Н2O
Хлорат калия КСlO3. Соль хлорноватой кислоты НСlO3, наиболее известная соль кислородсодержащих кислот хлора. Техническое название – бертоллетова соль (по имени ее первооткрывателя К.‑Л. Бертолле, 1786). Белый, плавится без разложения, при дальнейшем нагревании разлагается. Хорошо растворим в воде (образуется бесцветный раствор), гидролиза нет. Разлагается концентрированными кислотами. Сильный окислитель при сплавлении.
Применяется как компонент взрывчатых и пиротехнических смесей, головок спичек, в лаборатории – твердый источник кислорода.
Уравнения важнейших реакций:
4КClO3 = ЗКClO4 + КCl (400 °C)
2КClO3 = 2КCl + 3O2 (150–300 °C, кат. MnO2)
КClO3(т) + 6НCl (конц.) = КCl + ЗCl2| + ЗН2O (50–80 °C)
ЗКClO3(т) + 2H2SO4 (конц., гор.) = 2ClO2| + КClO4 + Н2O + 2KHSO4
(диоксид хлора на свету взрывается: 2ClO2(г) = Cl2 + 2O2)
2КClO3 + Е2(изб.) = 2КЕO3 + Cl2↑ (в разб. HNO3, Е = Br, I)
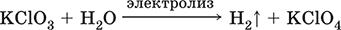
Получение КClO3 в промышленности – электролиз горячего раствора КCl (продукт КClO3 выделяется на аноде):
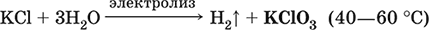
Бромиды. Иодиды
Бромид калия КBr. Бескислородная соль. Белый, негигроскопичный, плавится без разложения. Хорошо растворим в воде, гидролиза нет. Восстановитель (более слабый, чем KI).
Качественная реакция на ион Br – вытеснение брома из раствора КBr хлором и экстракция брома в органический растворитель, например СCl4 (в результате водный слой обесцвечивается, органический слой окрашивается в бурый цвет).
Применяется как компонент травителей при гравировке по металлам, составная часть фотоэмульсий, лекарственное средство.
Уравнения важнейших реакций:
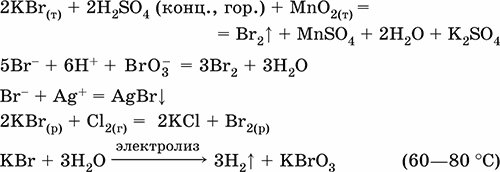
Получение:
K2CO3 + 2HBr = 2KBr + CO2↑ + H2O
Иодид калия KI. Бескислородная соль. Белый, негигроскопичный. При хранении на свету желтеет. Хорошо растворим в воде, гидролиза нет. Типичный восстановитель. Водный раствор KI хорошо растворяет I2 за счет комплексообразования.
Качественная реакция на ион I – вытеснение иода из раствора KI недостатком хлора и экстракция иода в органический растворитель, например СCl4 (в результате водный слой обесцвечивается, органический слой окрашивается в фиолетовый цвет).
Уравнения важнейших реакций:
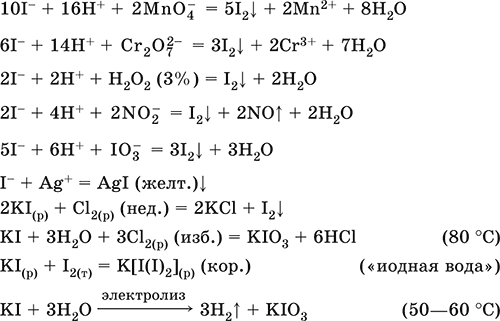
Получение:
K2CO3 + 2HI = 2KI+ СO2↑ + Н2O
Халькогены
Кислород
Кислород – элемент 2‑го периода и VIA‑группы Периодической системы, порядковый номер 8, относится к халькогенам (но чаще рассматривается отдельно). Электронная формула атома [2He]2s22p4, характерные степени окисления чаще 0 и – II, реже – I и +II, состояние ОII считается устойчивым.
Шкала степеней окисления кислорода:
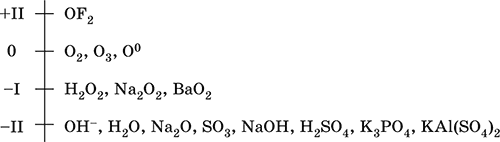
Кислород обладает высокой электроотрицательностью (3,50, второй элемент после фтора), проявляет типичные неметаллические свойства. Образует соединения со всеми элементами, кроме Не, Ne и Ar, входит в состав многочисленных оксидов, гидроксидов, солей кислородсодержащих кислот.
Природный кислород содержит изотоп 16O с примесью изотопов 17O и 18O. В химии большинство соединений природного кислорода рассматривается как изотопно‑чистые соединения кислорода‑16.
Кислород – самый распространенный элемент в земной коре (55 %) и природных водах, встречается в свободном и связанном виде. Жизненно важный элемент для всех организмов.
Кислород O2. Простое вещество. Состоит из неполярных молекул О2 (дикислород) с σπ‑связью O=O, устойчивая аллотропная форма существования элемента в свободном виде. Бесцветный газ, в жидком состоянии – светло‑голубой, в твердом – синий.
Составная часть воздуха: 20,94 % по объему, 23,13 % по массе. Из жидкого воздуха кислород выкипает после азота N2. Малорастворим в воде (31 мл/1 л Н2O при 20 °C), но несколько лучше, чем N2. При комнатной температуре обладает малой химической активностью из‑за прочности двойной связи в молекулах.
Кислород поддерживает горение многих веществ. Сильный окислитель при высоких температурах, реагирует с большинством металлов и неметаллов:

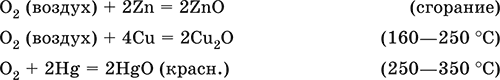
Кислород вызывает ржавление (медленное окисление) железа, уравнения реакций см. в 11.3. Особенно активен атомарный кислород О0 (активность выше, чем у озона O3), обычно получаемый непосредственно в зоне реакции при термическом разложении многих веществ.
Простейшая качественная реакция – яркое загорание тлеющей древесной лучинки в атмосфере кислорода.
Получение кислорода:
а) в промышленности – фракционная дистилляция жидкого воздуха, электролиз воды (уравнения реакций см. в разд. 12);
б) в лаборатории – нагревание легко разлагающихся кислородсодержащих веществ:
2HgO = 2Hg + O2 (450–500 °C)
2КMnO4 = К2MnO4 + MnO2 + O2 (200–240 °C)
2Na2O2 = 2Na2O + O2 (400–675 °C, вакуум)
2КClO3 = 2КCl + 3O2 (150–300 °C, кат. MnO2)
2KNO3 = 2KNO2 + O2 (400–520 °C)
Кислород является важнейшим продуктом основного химического производства. Применяется как реагент в химической технологии (обжиг сульфидных руд, синтез оксидов), металлургии (производство чугуна и стали) и газификации природного угля, при сварке и резке металлов; жидкий кислород – окислитель топлива в ракетной технике.
Убыль кислорода в атмосфере в результате процессов горения, гниения и дыхания возмещается растениями при фотосинтезе. При вдыхании человеком и животными воздуха в легкие кислород связывается с гемоглобином крови и переносится в клетки, где органические вещества (в первую очередь глюкоза) с его помощью окисляются и обеспечивают жизненную энергию организмов.
Озон O3. Простое вещество (трикислород), неустойчивая аллотропная форма существования элемента. Светло‑синий газ с характерным («озоновым») запахом, тяжелее воздуха. Молекула имеет строение незавершенного треугольника [: O(O)2] (sр2‑гибридизация, валентный угол 117°), содержит ковалентные σπ‑связи O=O. Разлагается под действием ультрафиолетового излучения, катализаторов и оксидов азота (разрушение озонового слоя атмосферы Земли). Устойчив в смеси с O2 (озонированный кислород). Малорастворим в воде (285 мл/1 л Н2O), но значительно лучше, чем O2. Сильный окислитель (более сильный, чем O2, но более слабый, чем атомарный кислород O0). Окисляет при комнатной температуре многие металлы и неметаллы до высоких степеней окисления. С надпероксидами щелочных металлов (К, Rb, Cs) образует оранжево‑красные озониды. Не реагирует с Au, Cu, Ni, Pt, Sn. Генерируется из кислорода O2 в специальном приборе – озонаторе.
Качественная реакция – выделение иода из раствора KI при комнатной температуре (O2 в реакцию не вступает). Уравнения важнейших реакций:
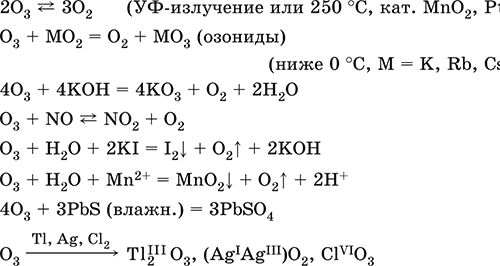
Получение: под действием электрического разряда в озонаторе:
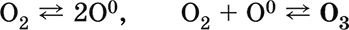
Применяется для дезинфекции питьевой воды, при отбеливании тканей и минеральных масел, как реагент в
неорганическом и органическом синтезе. В атмосфере Земли озоновый слой (на высоте =25 км) защищает живой мир от воздействия космического ультрафиолетового излучения.
Атомарный кислород О0. Третья аллотропная форма кислорода. Более сильный окислитель по сравнению с O2 и O3. Образуется при распаде молекул O2 и O3 под действием ультрафиолетового излучения. Возникает при термическом разложении кислородсодержащих веществ (см. выше, получение O2); при отсутствии восстановителей тут же переходит снова в O2 и O3, в присутствии восстановителей окисляет их:
KNO3 = KNO2 + O0
О0 + С (графит) = СO2
Поэтому вещества, легко отщепляющие кислород при нагревании, проявляют сильные окислительные свойства.
Пероксид водорода Н2O2. Бинарное соединение. Молекула Н2O2 неплоская, имеет строение с σ‑связью О – О на ребре и связями Н – О на плоскостях двугранного угла. Степень окисления кислорода равна – I. Группа – О – О– называется пероксогруппой.
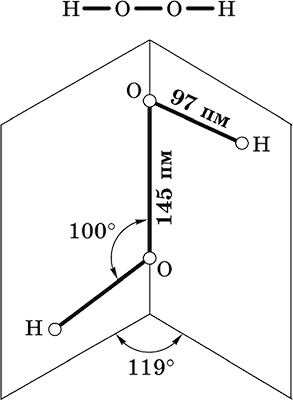
Бесцветная жидкость, вязкая, тяжелее воды, чувствительна к свету и примесям (стабилизатор Н3РO4). Разлагается со взрывом при слабом нагревании, на катализаторе – при комнатной температуре. Неограниченно смешивается с водой. Разбавленными щелочами нейтрализуется не полностью. Сильный окислитель, слабый восстановитель.
Пероксид водорода применяется как отбеливатель текстиля, бумаги, кож, жиров и минеральных масел, окислитель ракетного топлива, реагент в органическом синтезе, при осветлении картин старых мастеров (потемневший красочный слой из‑за перехода белил – гидроксокарбонатов свинца – в черный PbS осветляют переводом в белый PbSO4). В промышленности обычно используют взрывобезопасный 30 %‑ный раствор Н2O2 (пергидроль), в медицине – 3 %‑ный раствор.
Уравнения важнейших реакций:
2Н2O2 = 2Н2O + O2 (выше 150 °C или на кат. MnO2)
Н2O2 (разб.) + NaOH (разб.) = NaHO2 + Н2O
Н2O2 (конц.) + 2NaOH(т) = Na2O2↓ + 2H2O (0 °C)
Н2O2 (3 %) + 2H+ + 2I‑ = I2↓ + 2Н2O
5Н2O2 (30 %) + I2(т) = 2НIO3 + 4Н2O
Н2O2 (10 %) + SO32‑ = SO32‑ + H2O
4Н2O2 (30 %) + PbS (черн.) = 4H2O + PbSO4 (бел.)↓
3H2O2 + 2[Cr(OH)6]3‑ = 2CrO42‑ + 8H2O + 2OH‑
2Н2O2 (конц.) + Са(ClO)2 = СаCl2 + 2Н2O + 2O2↑
5H2O2 + 6H+ + 2MnO4‑ = 2Mn2+ + 5O2↑ + 8Н2O
Получение: в лаборатории вначале синтезируют пероксид бария ВаO2:
2ВаО + O2 (изб.) = 2ВаO2 (до 500 °C),
а затем его обрабатывают серной кислотой:
ВаO2 + H2SO4 = BaSO4↓ + Н2O2 (на холоду)
В промышленности (старый метод) – электролиз водного раствора H2SO4 или (NH4)2SO4 в специальных условиях; при этом кислота или соль не расходуются, а протекает электролиз воды с образованием на аноде Н2O2:
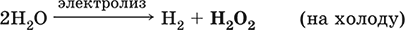
Современный промышленный способ (8O% мирового производства) – окисление сложного органического соединения 2‑этилантрагидрохинон кислородом воздуха на холоду.
