Коррозионное разрушение химического оборудования
Под коррозией понимают разрушение поверхности металла
вследствие протекания химических или электрохимических про-
цессов. По характеру распространения коррозия бывает сплош-
ной и локальной (местной) (рис. 10).
а
б
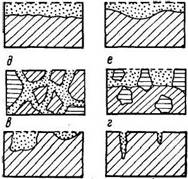
Рис. 10. Виды коррозии:
а – сплошная равномерная; б – сплошная неравномерная; в –
язвенная; г – точечная; д – межкристаллитная; е – структурно-
избирательная
При сплошной коррозии поверхность аппарата изнашивает-
ся равномерно. Это наименее опасный с точки зрения контроля
|
вид коррозии. При местной коррозии разрушение распространя-
ется только на отдельные участки и локализуется на них. Разно-
видностями местной коррозии являются язвенная и точечная.
Местной коррозии подвергаются металлы с инородными включе-
ниями, места сварки или повышенной механической нагрузки,
сплавы крупнозернистой структуры, когда защитная пленка име-
ет неодинаковую прочность и химическую стойкость на различ-
ных участках из-за образования гальванических микро- и макро-
элементов (пар).
Межкристаллитная коррозия – разрушение металлов по гра-
ницам зерен (кристаллов), при этом внешний вид детали не изме-
няется. Этот вид коррозии является более опасным, чем точечная
коррозия. Ей подвержены хромсодержащие стали, медьалюми-
ниевые сплавы и др. Межкристаллитная коррозия может быть
обусловлена рекристаллизацией сплава, образованием в нем но-
вой фазы: новых зерен и кристаллов, образующих между собой
гальванические пары. Склонность сплава к межкристаллитной
коррозии можно предотвратить специальной термической обра-
боткой и введением некоторых легирующих добавок (Ti, Та, V и
др.). Опасность возникновения межкристаллитной коррозии осо-
бенно велика около сварных швов.
Избирательная (селективная) коррозия представляет собой
разрушение одной или одновременно нескольких структурных
составляющих сплавов. Такой коррозии подвержены, главным
образом, серые чугуны и латуни, в которых в первую очередь
происходит растворение электрохимически более активных кри-
сталлов железа и цинка (процесс графитизации чугунов и обес-
цинкование латуней).
По механизму действия различают химическую и электро-
химическую коррозию.
Химическая коррозия – результат взаимодействия металла с
химически активными веществами. Частным случаем хими-
ческой коррозии является газовая (водородная, карбониль-
ная, кислородная, сероводородная и некоторые случаи атмосфер-
ной коррозии).
Особого внимания заслуживает водородная и карбонильная
коррозия, которая имеет место в производствах аммиака и неко-
торых других веществ. Молекулы и особенно атомы водорода
обладают малыми размерами и большой подвижностью, легко
диффундируют в металл, вызывая внутренние напряжения и хи-
мические реакции. Водород реагирует с цементитом стали по ре-
акции
Fe3C + 2Н2 = 3Fe + CH4.
Выделившийся при обезуглероживания стали метан вызывает по-
явление в ней микротрещин по границам зерен.
Оксид углерода (II) способен соединяться с некоторыми ме-
таллами и образовывать легколетучие карбонилы [например,
Fe(CO)8 и Ni(CO)4], которые в свою очередь при определенных
условиях разлагаются на металл и оксид углерода. При атмо-
сферном давлении действие СО на металл обнаруживается толь-
ко с повышением температуры до 500–600 ÉС. При давлении 20–
30 МПа карбонильная коррозия протекает при 150–200 ÉС.
Электрохимическая коррозия заключается в переходе в
электролит ионов металла под действием разности потенциалов,
обусловленной химической и структурной неоднородностью от-
дельных участков поверхности металла и градиента температуры.
Электрохимическая коррозия основного металла (например, же-
леза) возникает при наличии более электроположительных ино-
родных включений (углерод, никель, медь), гетерофазности спла-
ва, наличии защитных пленок на поверхности металла с микро-
порами, неравномерности концентрации электролита и темпера-
туры на различных участках корродирующей поверхности и т. д.
Частным случаем электрохимической коррозии являются
некоторые виды влажной атмосферной и почвенной коррозии,
протекающей под действием блуждающих токов, а также кон-
тактная коррозия (в зоне контакта различных металлов, при со-
прикосновении их с электролитом).
На скорость коррозионных процессов влияют многие фак-
торы: природа металлов и сплавов, состояние и качество обра-
ботки поверхности металла, характер агрессивной среды, темпе-
ратура, давление и др.
Обычно скорость растворения металлов при равномерной
коррозии выражают потерей массы с единицы поверхности в
единицу времени – К, г/(м2∙ч). При конструировании аппаратуры
удобнее оценивать возможную коррозию по глубинному показа-
телю (проницаемости П, мм/год), который связан с массовым по-
казателем зависимостью
П = 8,76К/ρ,
где ρ – плотность металла, г/см3.
Материал, из которого изготавливают химическую аппара-
туру, должен обладать высокой химической стойкостью не толь-
ко для обеспечения необходимой долговечности аппарата, но и
для безопасности условий работы и сохранения чистоты продук-
та. Разрушившийся материал загрязняет продукт, снижает его ка-
чество и может проявить каталитические свойства в побочных
процессах или, наоборот, может быть каталитическим ядом, на-
пример в процессе окисления аммиака.
Коррозионную стойкость металлов и сплавов в соответствии
с ГОСТ 13819-68 определяют по десятибалльной шкале.
Таблица 4
Группа стойкости
Совершенно стойкие
Весьма стойкие
Стойкие
Пониженно стойкие
Малостойкие
Нестойкие
Скорость
коррозии, мм/год
менее 0,001
0,001–0,005
0,005–0,010
0,01–0,05
0,05–0,10
0,1–0,5
0,5–1,0
1,0–5,0
5,0–10,0
более 10,0
Балл
Разрушение неметаллических материалов представляет со-
бой химическое их разрушение, происходящее в результате воз-
действия внешней среды (жидких и газообразных реагентов, на-
грева и охлаждения), метеорологических условий и микробиоло-
гического процесса.
Воздействие водных растворов веществ на неметаллические 
| |
| |
| |
| |
| |
| |
| |
















материалы неорганического происхождения можно свести к двум
видам процессов: растворению и выщелачиванию. Под растворе-
нием понимают переход всех компонентов материала в жидкую
фазу, а под выщелачиванием – процесс избирательного растворе-
ния отдельных компонентов. Так как многие неорганические не-
металлические конструкционные материалы (неорганические по-
лимеры) представляют собой в основном силикаты и алюмосили-
каты щелочных и щелочноземельных металлов, то растворяющее
действие на них оказывают щелочные растворы, плавиковая и
кремнийфтористоводородная кислоты. Вода, растворы солей и
кислот (кроме плавиковой) могут выщелачивать из силикатов ок-
сиды щелочных и щелочноземельных металлов.
Нагревание неорганических неметаллических материалов
может вызвать их термическую деструкцию, в результате чего
снижаются механическая и химическая стойкость. Деструкция
вызывается процессами структурной и собирательной рекристал-
лизации, приводящей к нарушению прочности материала, изме-
нению его объема, пористости и т. д.
Органические конструкционные материалы – органические
полимеры (пластмассы) – обладают высокой химической стой-
костью ко многим агрессивным средам, но подвержены термиче-
ской и фотохимической деструкции, биологической коррозии в
результате действия жидких и газообразных агрессивных сред.
В результате воздействия излучений происходит фотохими-
ческая деструкция полимеров. При этом в материале протекают
те же процессы, что и при термической деструкции.
Для уменьшения окисления в полимеры вводят антиокси-
данты, пигменты или создают из пластмасс композиционные ма-
териалы за счет введения в них порошковых и волокнистых ма-
териалов, в основном неорганического происхождения (углерод,
оксиды, карбиды и другие вещества).
Высокой стойкостью в кислотах, щелочах и солях обладают
полимеры, у которых макромолекулы состоят из углеводородных
цепей. При введении в эти цепи заместителей снижается химиче-
ская стойкость полимера, за исключением замены водорода фто-
ром (политетрафторэтилен) или хлором. Наличие в полимерах
двойной связи также снижает их устойчивость к действию окис-
лителей.
Сопротивляемость действию растворителей определяется
полярностью полимера и растворителей. Неполярные полимеры
набухают и растворяются в неполярных растворителях, а поляр-
ные – в полярных растворителях.
Все конструкционные материалы под действием рабочей и
окружающей среды претерпевают постепенное изменение, теря-
ют свою механическую прочность и претерпевают химические
изменения. Однако материалы, отвечающие требованиям корро-
зионной стойкости к определенной среде и пригодные для дан-
ных условий работы, всегда имеются. Конструкционные мате-
риалы выбирают, руководствуясь многими описанными выше ус-
ловиями, но в первую очередь – экономическими.