Электрохимические процессы
1. Электрохимические системы. Механизм возникновения электродного потенциала и его измерение. Устройство водородного электрода. Стандартные и равновесные значения электродных потенциалов. Уравнение Нернста.
2. Гальванический элемент: обозначение, электродные процессы, расчет напряжения гальванического элемента в стандартных и равновесных условиях. Типы гальванических элементов.
3. Электролизер. Последовательность процессов на электродах (катоде и аноде) в электролизере. Законы Фарадея.
4. Химическая коррозия металлов. Электрохимическая коррозия, коррозионный гальванический элемент, зависимость коррозионных процессов от кислотности среды. Методы зашиты от коррозии (легирование, покрытия – неметаллические, металлические: катодные, анодные; электронная защита – протекторная, защита внешним потенциалом).
Примерные задачи и вопросы к разделу «Электрохимические системы».
1. Составьте схемы двух гальванических элементов, в одном из которых медь была бы катодом, а в другом - анодом. Напишите для каждого из этих элементов электронные уравнения реакций, протекающих на катоде и на аноде, посчитайте напряжение этих гальванических элементов в стандартных условиях.
2. Составьте схему гальванического элемента, в основе которого лежит реакция, протекающая по уравнению Ni + Pb(N03)2 = Ni(NO3)2+ Pb. Напишите электронные уравнения анодного и катодного процессов. Вычислите напряжение этого элемента, если [Ni2+] = 0,01 моль/л.
3. Дана суммарная реакция Zn + 2H+ ® Zn2+ + H2. Обозначьте гальванический элемент, напишите электродные процессы. Посчитайте напряжение составленного Вами гальванического элемента в стандартных условиях и при условии, что металлический электрод погружен в раствор с концентрацией СZn2+ = 0,01 моль/л.
4. При каком условии будет работать гальванический элемент, электроды которого сделаны из одного и того же металла? Составьте схему, напишите электронные уравнения электродных процессов и вычислите напряжение гальванического элемента, в котором один никелевый электрод находится в 0,001 М растворе, а другой такой же электрод - в 1 М растворе сульфата никеля.
5. Составьте схему, напишите электронные уравнения электродных процессов, и вычислите напряжение медно-кадмиевого гальванического элемента, в котором [Cd2+] = 0.8 моль/л, а [Cu2+ ] = 0.01моль/л.
6. Марганцевый электрод в растворе его соли имеет потенциал -1,23 В. Вычислите концентрацию (моль/дм3) ионов Mn2+.
7. Из каких полуэлементов следует составить гальванический элемент с целью получения максимальной э.д.с.: а) Cu2+/Cu и Pb2+/Pb; б) Cr3+/Cr и Fe2+/Fe; в) Ni2+/Ni и Pb2+/Pb?
8. Значения стандартных электродных потенциалов систем Zn/Zn2+ и Cd/Cd2+ соответственно равны -0,76 В и 0,40 В. Какая реакция протекает произвольно в кадмиево-цинковом гальваническом элементе:
а) Zn + Cd2+ ® Cd + Zn2+ б) Cd + Zn2+ ® Zn + Cd2+.
9. В гальваническом элементе самопроизвольно протекает реакция Fe + Cd2+ ® Cd + Fe2+. Какой из электродов служит анодом: а) железный; б) кадмиевый?
10. Какой гальванический элемент называется концентрационным? Составьте схему, напишите электронные уравнения электродных процессов и вычислите э.д.с. гальванического элемента, в котором серебряные электроды опущены в 0,01 н и 0,1 н растворы нитрата серебра.
11. Железная и серебряная пластины соединены внешним проводником и погружены в раствор серной кислоты. Составьте схему данного гальванического элемента и напишите электронные уравнения процессов, происходящих на электродах.
12. В какой последовательности будут восстанавливаться катионы при электролизе водного раствора, содержащего ионы Cr3+, Pb2+, Hg2+, Mn2+, если молярная концентрация соответствующих им солей одинакова, а напряжение на катодах достаточно для восстановления каждого из них?
13. В каких случаях при электролизе водных растворов солей: а) на катоде выделяется водород; б) на аноде выделяется кислород; в) состав электролита не изменяется?
14. При электролизе водных растворов каких солей на катоде происходит: а) восстановление только катионов металлов; б) одновременное восстановление катионов металла и воды; в) восстановление только воды?
15. В каких случаях при электролизе водных растворов солей на аноде наблюдается разрядка анионов, в каких случаях выделяется кислород, в каких случаях идет окисление самого анода?
16. Электролиз водного раствора иодида натрия проводили при токе силой 6 А в течение 2,5 ч. Составьте электронные уравнения процессов, происходящих на угольных электродах, вычислите массу веществ, выделяющихся на электродах.
17. В течение какого времени необходимо пропускать ток силой 1 А при электролизе водного раствора сульфата хрома(III), чтобы масса катода возросла на 10 г? Какой объем (н.у.) кислорода выделился на аноде?
18. Какими формулами выражаются количественные характеристики электролиза? Приведите пример электролиза и его количественного расчета.
19. Какие реакции протекают при электролизе с инертными электродами водного раствора КОН? Какие вещества и в каком объеме (при н.у.) можно получить при электролизе этого раствора, если пропустить ток силой 13,4 А в течение двух часов (выход по току равен 100 %)?
20. Какой продукт не получится при электролизе раствора KI?
а) Н2; б) КОН; в) К; г) I2.
21. Газообразные вещества будут выделяться и на катоде и на аноде при электролизе водного раствора соли:
а) AgNO3; б) KNO3; в) CuCl2; г) SnCl2.
22. При электролизе водного раствора нитрата серебра на катоде образуется:
а) Ag; б) NO2; в) NO; г) H2
23. Установите соответствие между формулой вещества и продуктами электролиза его водного раствора на инертных электродах.
формулы веществ продукты электролиза
1) CaCl2 а) Ca, O2 , Cl2
2) Fe(NO3)3 б) Fe, H2, Cl2
3) K2SO4 в) K, H2, SO3
4) FeCl3 г) Fe, H2, O2
д) H2, Cl2
е) H2, O2
24. Процессы, протекающие при электролизе раствора сульфата натрия на платиновом катоде:
а) Na+ + 1e ® Na0; б) 2 H2O + 2e ® H2 + 2 OH-;
в) Pt0 - 2e ® Pt2+; г)
25. Процессы, протекающие при электролизе раствора сульфата натрия на никелевом аноде:
а) 2 SO42- - 2e ® S4O82-; б) 2 H2O - 4e ® O2 + 4 H+;
в) Ni0 – 2e ® Ni2+; г)
26. Процессы, протекающие при электролизе раствора хлорида меди(II) на железном катоде:
а) Cu2+ + 2e ® Cu0; б) 2 H2O + 2e ® H2 + 2 OH-;
в) Fe0 – 2e ® Fe2+; г)
27. Процессы, протекающие при электролизе раствора хлорида меди(II) на платиновом аноде:
а) 2 Cl- - 2e ® Cl2; б) 2 H2O - 4e ® O2 + 4 H+;
в) Pt0 - 2e ® Pt2+; г)
28. Во время проведения электролиза водного раствора СаСl2 среда у катода становится:
а) кислая; б) щелочная; в) нейтральная; г) не изменяется.
29. Ток силой 2 А в течение 2 час пропускали через раствор CuBr2. Сколько меди выделилось на катоде? Запишите электрохимическую систему, уравнения электродных реакций, если анод сделан из графита.
30. Какие реакции происходят на катоде и аноде при электролизе KNO3, если оба электрода сделаны из платины? Сколько и каких веществ образовалось возле анода и катода, если пропускали ток силой 1А в течении 30 мин? Запишите электрохимическую систему, электродные реакции.
31. На какие виды подразделяется коррозия в зависимости от механизма процесса и формы коррозионных разрушений? На каждый вид коррозии приведите примеры. Какое значение имеет коррозия?
32. .Какая коррозия называется химической, а какая – электрохимической?
33. Электрик подключил к открытым алюминиевым проводам нагрузку медным кабелем. Через некоторое время медный кабель в месте контакта с алюминиевым проводом прокорродировал. Как объяснить этот факт?
34. Железное изделие покрыли никелем. Какое это покрытие - анодное или катодное? Почему? Составьте электронные уравнения анодного и катодного процессов коррозии этого изделия при нарушении покрытия во влажном воздухе. Укажите продукты коррозии.
35. Никелевое изделие покрыто серебром. Какое это покрытие? Какой из металлов будет окисляться при коррозии в случае разрушения покрытия? Дайте схему образующегося при этом гальванического элемента, помня, что коррозия протекает в кислой среде.
36. Как происходит атмосферная коррозия луженого железа и луженой меди при нарушении покрытия? Составьте электронные уравнения анодного и катодного процессов в обоих случаях.
37. Под рисунком подпишите способ защиты металла Fe от коррозии:
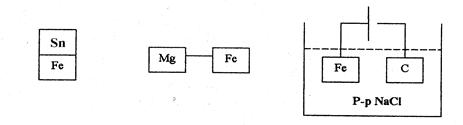 |
38. Определите возможность коррозии двух контактирующих металлов (Al – Cu) в кислой среде. Составьте схему коррозионного г.э., напишите уравнения электродных реакций. Предложите катодное покрытие.
39. Отверстия в медном самоваре и железном котелке запаяли оловом. Через некоторое время котелок прохудился, а самовар нет. Почему? Ответ иллюстрируйте схемами коррозионных процессов и уравнениями реакций.
40. Для придания красивого внешнего вида и защиты от коррозии железо обычно покрывают цинком, оловом, хромом, кадмием, никелем. Какое покрытие наиболее надежно защищает железо от коррозии? Расположите металлы в порядке убывания защитного эффекта.
41. Алюминий склепан с медью. Какой из металлов будет подвергаться коррозии, если эта пара попадет в кислотную среду? Составьте схему образующегося при этом гальванического элемента. Вычислите ЭДС и энергию Гиббса этого элемента при стандартных условиях.
42. Какому виду коррозии подвергается выхлопная труба автомобиля, работающего на бензине с примесью серы? Напишите уравнение реакции.
43. Две железные пластинки покрасили в серебристый цвет: одну краской с алюминиевой пудрой, а другую – с цинковой. При испытаниях на коррозионную устойчивость выяснилось, что краска с цинковой пудрой – лучше. Почему? Составьте схемы коррозионных гальванических элементов, которые образуются при нарушении покрытия.
44. Чем отличается защита от коррозии с помощью пассиваторов от защиты с помощью ингибиторов? Приведите примеры пассивирования поверхности и примеры ингибиторов коррозии.
45. Для защиты от коррозии используют протекторную и катодную защиту. Объясните, чем определяется выбор металла для протектора в первом случае и какова роль электрического тока от внешнего источника во втором случае.
