Задания для самостоятельного решения частей В, С. 1. Приготовили раствор 134,4 л (н.у.) диоксида серы и добавили 1,5 л 25 %‑ного раствора гидроксида натрия (плотность раствора 1,28 г/мл)
1. Приготовили раствор 134,4 л (н.у.) диоксида серы и добавили 1,5 л 25 %‑ного раствора гидроксида натрия (плотность раствора 1,28 г/мл). Определите массу (в граммах) образовавшейся соли.
2. Сульфид свинца (II) массой 95,6 г обрабатывают с помощью 300 мл 30 %‑ного раствора пероксида водорода (плотность раствора 1122,2 г/л). Рассчитайте массу (в граммах) продукта – сульфата свинца (II).
3. Смешали 100 г 5,64 %‑ного раствора фенола и 100 г 17,92 %‑ного раствора гидроксида калия. Найдите массовую долю (в %) избытка одного из реагентов в конечном растворе.
4. Установите массу (в граммах) железной пластинки после выдерживания в 110 мл 10 %‑го раствора CuSO4 (плотность раствора 1,1 г/мл), если до опыта ее масса составляла 11,5 г.
5. Вычислите объем (в литрах) 96 %‑ного водного спирта с плотностью 0,81 кг/л, полученного каталитической гидратацией 112 м3 (н.у.) этилена, содержащего 12,5 % (по объему) этана.
6. Газ, полученный сжиганием 44,8 л (н.у.) сероводорода в кислороде, поглощен с помощью 0,5 л 25 %‑ного раствора гидроксида натрия (плотность раствора 1,275 г/ мл). Определите массовую долю (в %) соли в конечном растворе.
7. Углекислый газ объемом 15 л (н.у.) пропущен через 560 г 5%‑ного раствора гидроксида калия. Найдите массу (в граммах) соли, полученной в этом процессе.
8. Железная пластинка массой 5 г опущена на некоторое время в 50 мл 15 %‑ного раствора сульфата меди (II) с плотностью 1,12 г/мл. Масса пластинки увеличилась на 0,16 г. Какова массовая доля (в %) сульфата меди (II) в оставшемся растворе?
9. По реакции Кучерова получен этаналь, который переведен в соответствующую кислоту в виде 100 г 6%‑ного водного раствора. Найдите объем (в литрах, н.у.) исходного органического соединения в получении этаналя.
10. Определите массовую долю (в %) избытка одного из реагентов в растворе после сливания 80 г 10 %‑ного раствора гидроксида натрия и 2O г 18,25 %‑ной хлороводородной кислоты.
11. Установите объем (в литрах, н.у.) газа, собранного после внесения 0,3 моль алюминия в 160 мл 20 %‑ного раствора гидроксида калия (плотность раствора 1,19 г/мл).
12. Найдите массу (в граммах) органического продукта, полученного при смешивании 250 г 94 % – ного водного раствора фенола и 2143 г 3,5 %‑ной бромной воды.
Нахождение молекулярной формулы органического соединения
При выведении формул веществ, особенно в органической химии, часто используют относительную плотность газа.
Относительная плотность газа X – отношение абсолютной плотности этого (неизвестного) газа к абсолютной плотности другого (известного) газа В при одинаковых условиях:
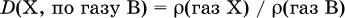
Для 1 моль газа его абсолютная плотность равна
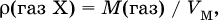
откуда
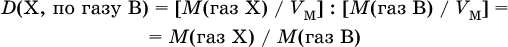
Если газ В задан, то
– плотность газа X по водороду Н2 (М = 2 г/моль)
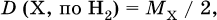
– плотность газа X по воздуху (М = 29 г/моль)
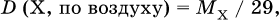
и аналогично для любого другого известного газа X.
Примеры решения задач
1. В результате сгорания кислородсодержащего органического соединения в избытке воздуха собрано 1,584 г СO2 и O,972 мл Н2O. Плотность пара этого соединения по воздуху равна 1,5865.
Выведите формулу соединения, если в его молекуле содержатся два одноименных радикала.
Элементы ответа.
1) Составлена схема реакции:
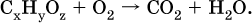
2) Определена масса С и Н в этом соединении:
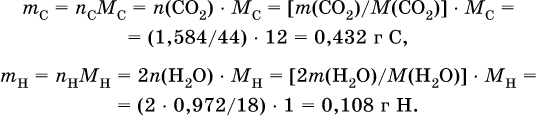
3) Определена формула соединения CxНyOz:
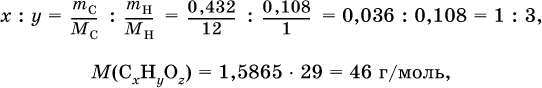
при х = 1 и у = 3: М(СН3) = 15, 46–15 = 31 г/моль на кислород – это не подходит,
при х = 2 и у = 6: 2М(СН3) = 30, М0 = 16, 30 + 16 = = 46 г/моль – это подходит, таким образом, искомая формула соединения С2Н6O, или с учетом условия (СН3)2O.
2. Некоторая масса неизвестного алкина с избытком хлора дает 21 г тетрахлор‑производного. Такая же масса того же алкина с избытком брома – 38,8 г тетрабром‑производного. Выведите формулу взятого алкина.
Элементы ответа.
1) Составлены уравнения реакций:
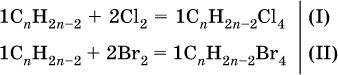
2) Составлены выражения для молярных масс производных:
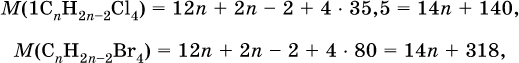
и для молярной массы алкина:
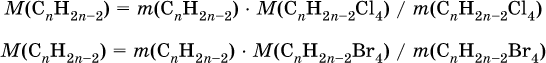
3) Выведена формула алкина: по условию масса алкина одинакова в реакциях (I) и (II), следовательно
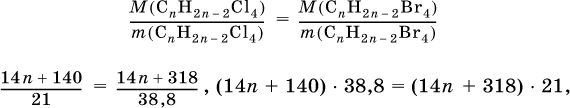
откуда n = 5 и формула алкина С5Н8.
