Ряд стандартных электродных потенциалов
Значения некоторых стандартных окислительно-восстановительных потенциалов гальванических элементов, расположенных в порядке возрастания их алгебраической величины, представлены в ряду стандартных электродных потенциалов – СЭП (ряду напряжения). В этот ряд всегда помещают, кроме металлов, также водород, что позволяет видеть, какие металлы способны вытеснять водород из водных растворов кислот.
Ионы металлов являются окислителями, а металлы в виде простых веществ – восстановителями.
Как говорилось ранее, на поверхности металла устанавливается равновесие:
 Me0 Me n+ ∙ + nē,
Me0 Me n+ ∙ + nē,
а на поверхности губчатой платины стандартного водородного электрода:
 Н20 2Н+ ∙ + 2ē.
Н20 2Н+ ∙ + 2ē.
Если металл проявляет более сильные восстановительные свойства, по сравнению с молекулярным водородом (равновесие на металле смещено вправо), то на поверхности металлической пластины при этом протекает процесс окисления, а на поверхности платины – процесс восстановления ионов водорода (равновесие водородного электрода смещено влево). Тогда стандартный электродный потенциал металла имеет отрицательное значение.
Если металл проявляет менее сильные восстановительные свойства (но зато его ионы проявляют более сильные окислительные свойства), по сравнению с молекулярным водородом (равновесие на металле смещено влево), то на поверхности металлической пластины при этом протекает процесс восстановления, а на поверхности платины – процесс окисления молекулярного водорода (равновесие водородного электрода смещено вправо). Тогда стандартный электродный потенциал металла имеет положительное значение.
Из вышесказанного можно сделать следующие выводы.
1 Чем дальше расположен металл в ряду напряжений, т. е. чем больше его стандартный потенциал, тем более сильным окислителем в водном растворе являются его ионы (и тем легче они принимают электроны), и наоборот, чем ближе металл к началу ряда, т. е. чем меньше значение Е0, тем более сильные восстановительные свойства проявляет простое вещество – металл (и тем легче он электроны отдает).
2 Потенциал электродного процесса:
Н2 = 2Н+ + 2ē
в нейтральной среде (рН = 7) равен Е = –0,059∙7 = –0,41 В .
Активные металлы начала ряда, имеющие потенциал, значительно более отрицательный, чем –0,41 В, вытесняют водород из воды (а). Магний вытесняет водород только из горячей воды (б). Металлы, расположенные между магнием и кадмием, обычно не вытесняют водород из воды. На поверхности этих металлов образуются оксидные пленки, обладающие защитным действием. В некоторых случаях возможно протекание процесса в случае нагревания (в) или разрушения защитной оксидной пленки (г). Например:
а) 2Na + 2H2O → 2NaOH + Н2↑;
t
б) Mg + 2H2O → 2Mg(OH)2 + Н2↑;
в) 3Fe + 4H2O → Fe3O4 + 4Н2↑;
г) Zn + 2H2O + 2KOH → K2[Zn(OH)4] + Н2↑.
Металлы, расположенные в ряду СЭП после водорода, с водой в отсутствии окислителей не взаимодействуют.
2 Водород из кислот неокислителей способны вытеснять только те металлы, которые имеют отрицательную величину стандартного водородного электрода и расположены в ряду СЭП до (выше) водорода. Металлы, расположенные в ряду СЭП после водорода, с растворами кислот не взаимодействуют. Например:
Мg + 2HCl → MgCl2 + H2↑ или в ионной форме Мg0 + 2H+ → Mg2+ + H20↑
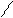 Ag + HCl →
Ag + HCl →
При этом на поверхности некоторых металлов образуются защитные пленки, тормозящие реакцию. Так, оксидная пленка на алюминии делает этот металл стойким не только в воде, но и в растворах некоторых кислот. Явление глубокого торможения окисления металла, обусловленное наличием на его поверхности защитных оксидных или солевых пленок, называется пассивностью, а состояние металла при этом – пассивным состоянием.
3 Металлы способны вытеснять друг друга из растворов солей. Рассматривая конкретные случаи таких реакций, следует помнить, что активные металлы вытесняют водород не только из воды, но и из любого водного раствора. Поэтому взаимное вытеснение металлов из растворов их солей практически происходит лишь в случае металлов, расположенных в ряду после магния. То есть, металл с более отрицательным значением стандартного электродного потенциала является восстановителем по отношению к электроду с более положительным значением E0.
Таким образом, металлы средней химической активности, стоящие в ряду СЭП выше, вытесняют нижестоящие из их солей. Например:
Мg + Ni(NO3)2 → Mg(NO3)2 + Ni
или в ионной форме: Мg0 + Ni2+ → Mg2+ + Ni0.
Гальванические элементы
В рассмотренных выше окислительно-восстановительных реакциях переход электронов от восстановителя – атома активного металла – к окислителю – ионам неактивного металла – происходит непосредственно, поскольку восстановитель соприкасается с окислителем. Обе стадии реакции – окисление активного металла и восстановление неактивного металла пространственно не разделены, т. е. протекают в одном месте – месте соприкосновения активного металла с раствором соли другого металла.
Так, при опускании цинковой пластинки в раствор сульфата меди происходит реакция:
Zn + CuSO4 → ZnSO4 + Cu
или в ионной форме: Zn0 + Cu2+ → Zn2+ + Cu0.
Здесь восстановитель – цинк – отдает электроны. Эта полуреакция выражается уравнением:
Zn0 – 2ē → Zn2+.
Окислитель – ион меди – принимает электроны. Уравнение этой полуреакции имеет вид:
Cu2+ + 2ē → Cu0.
Можно, однако, осуществить эту реакцию таким способом, что окислительная и восстановительная полуреакции окажутся пространственно разделенными, а электроны будут переходить от восстановителя к окислителю не непосредственно, а по проводнику электрического тока – по внешней цепи. Этот направленный поток электронов представляет собою электрический ток. Устройства, которые применяют для непосредственного преобразования энергии химической реакции в электрическую энергию, называются гальваническими элементами.Их называют также химическими источниками электрической энергии или химическими источниками тока(сокращенно ХИТ).
В простейшем случае гальванический элемент состоит из двух пластин или стержней (электродов первого рода), изготовленных из различных металлов (окислительно-восстановительных пар), погруженных в раствор электролита (чаще – это раствор соли металла). К электродам первого рода относятся электроды, в уравнение Нернста которых под знаком логарифма входят активности веществ, участвующих в электродной реакции. Потенциал таких электродов меняется с изменением концентрации реагентов. Электродами первого рода являются электроды, состоящие из элементарного вещества, находящегося в контакте с раствором, содержащим его собственные ионы. Например, металлический электрод – металл, погруженный в раствор своей соли Mе/Mеn+.
Электрод, на котором происходит процесс окисления (анодный процесс), называется анодом. Роль анода играет металл с меньшей алгебраической величиной электродного потенциала, т. е. более активный металл. Электрод, на котором осуществляется восстановление (катодный процесс), называется катодом (металл с большей алгебраической величиной электродного потенциала).
Такая система делает возможным пространственное разделение окислительно-восстановительной реакции: окисление протекает на одном металле, а восстановление – на другом. Таким образом, электроны передаются от восстановителя к окислителю по внешней цепи.
Рассмотрим в качестве примера медно-цинковый гальванический элемент (элемент Якоби-Даниэля), образованный двумя электродами первого рода и работающий за счет энергии приведенной выше реакции между цинком и раствором сульфатом меди.
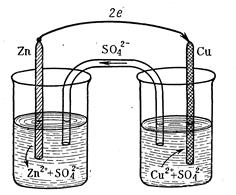
Этот элемент (рисунок 4) состоит из медной пластины, погруженной в раствор сульфата меди (медный электрод), и цинковой пластины, погруженной в раствор сульфата цинка (цинковый электрод). Оба раствора или соприкасаются друг с другом, но для предупреждения смешивания они разделены перегородкой, изготовленной из пористого материала (рисунок4, а), или не соприкасаются, но взаимосвязь между ними осуществляется посредством проводника второго рода (электролитного мостика (рисунок 4, б).
 а) б)
а) б)
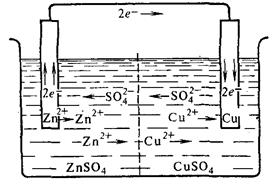
а) с растворами, соприкасающимися друг с другом;
б) с изолированными растворами
Рисунок 4 – Схема гальванического элемента Якоби-Даниэля.
Работа гальванического элемента при замыкании цепи начинается с того, что электрод, изготовленный из более активного металла, в данном случае из цинка, взаимодействует с полярными молекулами воды, находящимися в соприкасающемся с поверхностью электрода растворе, по уравнению:
Zn0 + п Н2О → Zn2+∙ п Н2О + 2ē
или в упрощенной форме Zn0 – 2ē → Zn2+.
Образовавшиеся гидратированные катионы цинка переходят в раствор, а электроны заряжают отрицательно поверхность электрода. Электрод, на котором этот процесс происходит, получил название анода.Как видно, в данном случае анод заряжается отрицательно. В этом заключается первая стадия работы гальванического элемента – возникновение источника отрицательного электричества.
Осуществляется отвод высвобождающихся при этом электронов по внешней цепи с анода на катод в результате соединения цинкового электрода проволокой с медным электродом. В этом заключается вторая стадия работы гальванического элемента – прохождение электрического тока по проводнику.
На медном электроде протекает восстановление ионов меди. Электроны, приходящие сюда от цинкового электрода, соединяются с выходящими из раствора дегидратирующимися катионами меди; образуются атомы меди, выделяющиеся в виде металла. Соответствующее электрохимическое уравнение имеет вид:
Cu 2+∙ п Н2О + 2ē → Cu0 + п Н2О
или в упрощенной форме Cu2+ + 2ē → Cu0.
Таким образом, на медном электроде идет процесс восстановления меди, в связи с чем электрод, на котором этот процесс происходит, получил название катода. В этом заключается третья стадия работы гальванического элемента – разрядка ионов на катоде. Все три стадии работы гальванического элемента сопряжены между собой и идут с одинаковой скоростью. Число электронов, посылаемых в единицу времени анодом, равно числу электронов, проходящих в единицу времени через сечение проводника, и числу электронов, разряжающих в единицу времени катионы на катоде.
Суммарное уравнение реакции, протекающей в элементе (токообразующей реакции), получится при сложении уравнений обеих полуреакций:
Zn0 + Cu2+ → Zn2+ + Cu0
или в молекулярной форме:
Zn + CuSO4 → ZnSO4 + Cu
Таким образом, при работе гальванического элемента электроны от восстановителя переходят к окислителю по внешней цепи (проводнику первого рода), на электродах идут электрохимические процессы, в растворе наблюдается направленное движение ионов.
У цинкового электрода катионы выходят в раствор, создавая в нем избыточный положительный заряд, а у медного электрода раствор, наоборот, все время обедняется катионами, так что здесь раствор заряжается отрицательно. В результате этого создается электрическое поле, в котором катионы, находящиеся в растворе (Сu2+ и Zn2+), движутся от цинкового электрода к медному, а анионы SO42– – в обратном направлении. Движение ионов SO42– в растворе замыкает электрическую цепь гальванического элемента (например, если убрать электролитный мостик (рисунок 4, б), то электрический ток по внешнему проводнику протекать не будет).
Таким образом при замыкании внешней цепи, т. е. при соединении цинка с медью металлическим проводником, возникают самопроизвольные процессы растворения цинка (как более активного металла) на аноде и выделения меди (как менее активного металла) из раствора на катоде. Данные процессы будут продолжаться до тех пор, пока не выровняются потенциалы электродов или не растворится весь цинк (или не восстановится на медном электроде вся медь).
При схематическом изображении гальванического элемента граница раздела фаз между металлом и раствором обозначается одной вертикальной чертой, граница между растворами электролитов – двойной вертикальной чертой, которая отделяет анодное пространство от катодного. Слева записывается анод Zn¦Zn2+, на котором возникает избыток электронов и происходит процесс окисления – отрицательный полюс (–). Справа – катод Cu2+¦Cu – электрод с недостатком электронов, положительный полюс (+). Стрелками показано направление движения электронов во внешней цепи гальванического элемента.
Например, схема гальванического элемента Якоби-Даниэля изображается следующим образом (молекулярная форма):
2ē
Zn ô ZnSO4 ôô CuSO4 ô Cu. |
Эта же схема может быть изображена в ионной форме:
2ē
Zn ô Zn2+ ôô Cu2+ ô Cu. |
Поскольку число электронов, которые за единицу времени отдает анод (цинк), равно числу электронов, принимаемых за это же время ионами катода (меди), скорость реакции, протекающей в гальваническом элементе, пропорциональна количеству электричества, перенесенного по цепи в единицу времени, т. е. силе тока в цепи.
Получаемая в процессе работы гальванического элемента энергия электрического тока равна произведению количества электричества, прошедшего от анода к катоду, на напряжение. Максимальное значение этого напряжения называется электродвижущей силой гальванического элемента.
Окислительно-восстановительная реакция, характеризующая работу гальванического элемента, протекает в направлении, в котором электродвижущая сила (ЭДС) элемента имеет положительное значение. В соответствии с принятой формой записи гальванического элемента его ЭДС равна электродному потенциалу правого электрода (окислителя) минус электродный потенциал левого электрода (восстановителя).
ЭДС гальванического элемента определяется как разность электродных потенциалов катода и анода:
ЭДС = ЕК – ЕА. .
В случае элемента Якоби-Даниэля (–)Zn¦Zn2+||Cu2+¦Cu(+) для стандартных условий:
ЭДС = Е0Cu – Е0Zn = 0, 34 – (–0, 76) = 1,1 В
Для нестандартных условий ЭДС элемента Якоби-Даниэля находится из разности электродных потенциалов, вычисленных по уравнению Нернста.


