Iii. периодический закон. химическая связь
СПЕЦИФИКАЦИЯ ТЕСТА
| № задания | Требование к уровню подготовки выпускников | Виды деятельности | ||
| Воспроизведение знаний | Применение знаний и умений | |||
| В знакомой ситуации | В измененной ситуации | |||
| Периодический закон и периодическая система химических элементов Д.И. Менделеева. | + | |||
| 2. | Группы и периоды периодической системы. | + | ||
| 3. | Строение атома. | + | ||
| 4. | Ядро (протоны, нейтроны) и электроны. | + | ||
| 5. | Изотопы. | + | ||
| 6. | Строение электронных оболочек атомов первых 20 элементов периодической системы Д.И. Менделеева. | + | ||
| 7. | Химическая связь. | + | ||
| 8. | Типы химических связей: ковалентная (полярная и неполярная), ионная, металлическая. | + | ||
| 9. | Понятие о валентности | + | ||
| 10. | Понятие о степени окисления | + | ||
| 11. | Кристаллическая решетка | + | ||
| 12. | Группы и периоды периодической системы. | + | ||
| 13. | Ионы | + | ||
| Ионы | + | |||
| Изотопы | + | |||
| 16. | Строение электронных оболочек + химическая связь | + |
ВАРИАНТ 1
1. Среди химических элементов Si, P, S, C1 более ярко свойства неметалла выражены у:
1) кремния 2) фосфора 3) серы 4) хлора
2. Атомы элементов, имеющие одинаковое число валентных электронов, расположены
| 1) в одной группе | 2) в одной подгруппе | 3) в одном периоде | 4) по диагонали |
3. В оксидах элементов третьего периода периодической системы Na2O, MgO, Al2O3, SiO2, P2O5, SO3, Cl2O7 в периоде слева направо
| 1) основные свойства возрастают | 3) кислотные свойства усиливаются |
| 2) основные свойства ослабевают | 4) кислотные свойства уменьшаются |
4. Число протонов в ядре атома 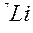 равно
равно
| 1) 3 | 2) 4 | 3) 6 | 4)7 |
5. Изотопы химического элемента отличаются числом
| 1) нейтронов | 2) заполненных электронных слоев | 3) валентных электронов | 4) протонов |
6. Химическому элементу, степень окисления которого в соединении равна -2, соответствует схема распределения электронов в атоме по слоям:
1)2,8,6 2) 2,8,2 3) 2,8,7 4) 2,2
7. Разрушение химической связи – это процесс, который .
1) сопровождается выделением энергии
2) происходит самопроизвольно в изолированных системах
3) требует затраты энергии
4) может происходить только под действием света
8. Вещества, формулы которых RbF, HF, F2, образованы химическими связями соответственно
1) ковалентной неполярной, ковалентной полярной, ионной
2) ионной, ковалентной неполярной, ковалентной полярной
3) ионной, ковалентной полярной, ковалентной неполярной
4) ковалентной полярной, ионной, ковалентной неполярной
9. Высшую и низшую валентность сера проявляет соответственно в соединениях
| 1) | SO3 и ZnS | 2) | SO2 и H2S | 3) | SO3 и SO2 | 4) | H2S и SO3 |
10. Азот имеет степень окисления +3 в ряду веществ:
1) N2О3, HNО3, KNО2
2) NН3, N2О3, НNO3
3) NaNО2, N2О3, HNO2
4) KNО3, HNО2, NH3
11. Ионную кристаллическую решетку имеет
1) фторид натрия
2) вода
3) алюминий
4) алмаз
12. Высший оксид состава Э2O3 образует химический элемент, имеющий
1) заряд атомного ядра +3
2) пять электронов на внешнем электронном слое
3) заряд атомного ядра +13
4) два электрона на внешнем электронном слое
13. Ион, имеющий в своем составе 18 электронов и 16 протонов, имеет заряд
| 1) +1 | 2) +2 | 3) – 1 | 4) –2 |
14. Атом щелочного металла, который образует ион, имеющий электронную конфигурацию 1s22s22p63s23p6 – это
| 1) рубидий | 2) калий | 3) натрий | 4) литий |
15. Ядро атома 13С состоит из
| 1) шести протонов и шести нейтронов | 3) шести протонов и семи нейтронов |
| 2) шести нейтронов и семи протонов | 4) семи нейтронов и семи протонов |
16. Химический элемент, в атоме которого электроны по слоям распределены так: 2, 8, 5, образует с водородом химическую связь
1) ковалентную полярную
2) ковалентную неполярную
3) ионную
4) металлическую
ВАРИАНТ 2
1. Наиболее ярко металлические свойства выражены у
1) лития
2) калия
3) натрия
4) рубидия
2. Атомы азота и фосфора имеют
1) одинаковое число электронных слоев
2) одинаковое число электронов внешнего электронного слоя
3) одинаковое число протонов в ядре
4) одинаковые радиусы
3. Четыре электрона на внешнем энергетическом уровне имеет атом
1) гелия
2) бериллия
3) углерода
4) кислорода
4. В состав ядра атома входят
1) протоны и электроны
2) электроны и нейтроны
3) нейтроны и протоны
4) только протоны
5. Изотопы химического элемента имеют разные массы, потому что в их атомах разное число
1) протонов 2) нейтронов 3) электронов 4) протонов и нейтронов
6. В ряду химических элементов С ® А1 ® Са число электронных слоев в их атомах
1) возрастает от 3 до 5
2) возрастает от 2 до 4
3) уменьшается от 4 до 2
4) уменьшается от 5 до 3
7. Образование химической связи – это процесс, который .
1) сопровождается выделением энергии
2) происходит самопроизвольно в изолированных системах
3) требует затраты энергии
4) может происходить только под действием света
8. Ковалентной неполярной связью образованы все молекулы веществ в ряду:
1) О3, N2, H2, O2
2) O2, О3, СО, NH3
3) NH3, СО, СO2, H2O
4) Н2O, O2, N2, H2
9. Валентности металлов в соединениях Al2O3, AgCl, FeCl2 соответственно равны
1) III, II, I 2) I, II, III 3) II, I, I 4) III, I, II
10. Степень окисления серы одинакова в ряду веществ:
1) CuSO4, Cu2S, H2SO4
2) SO2, (NH4)2SO4, H2SO4
3) SO3, Н2SO3, Na2SO3
4) K2SO3, SO2, Na2SО3
11. Кристаллическая решетка твердого оксида углерода (IV) CO2
1) ионная 2) атомная 3) молекулярная 4) металлическая
12. Химическому элементу со степенью окисления -3 соответствует распределение электронов в атоме по слоям
1) 2, 8, 7 2) 2, 3 3) 2, 5 4) 2, 8, 2
13. Ион, имеющий в своем составе 18 электронов и 17 протонов, имеет заряд
| 1) +2 | 2) +1 | 3) – 1 | 4) –2 |
14. Атом галогена, который образует ион, имеющий электронную конфигурацию 1s22s22p63s23p6, – это
| 1) фтор | 2) хлор | 3) бром | 4) йод |
15. Ядро атома 3Нe состоит из
| 1) трех протонов | 3) двух протонов и одного электрона |
| 2) двух протонов и одного нейтрона | 4) трех нейтронов и одного протона |
16. В соединении с фтором элемента, в атоме которого распределение электронов по слоям 2, 8, 8, 1, химическая связь
1) ионная
2) ковалентная полярная
3) ковалентная неполярная
4) металлическая
