Задача. Вычисление объема газа, вступившего в реакцию, если известна масса одного из продуктов реакции.
Пример:
2. Сколько литров водорода сгорело, если образовалось 72 г воды?
Решение:
1. M (H2O) = 1 • 2 + 16 = 18 г/моль
2. Находим количество вещества воды по условию задачи:
n = m / M = 72 г : 18 г/моль = 4 моль
3. Записываем над уравнением реакции имеющиеся данные, а под уравнением – число моль согласно уравнению (равно коэффициенту перед веществом):
x моль 4 моль
2H2 + O2 = 2H2O
2 моль 2 моль
4. Составляем пропорцию:
x моль – 4 моль
2 моль – 2 моль
Находим x:
x = 4 моль • 2 моль / 2 моль = 4 моль
5. Находим объем водорода:
v = 22,4 л/моль • 4 моль = 89,6 л
Ответ: 89,6 л.
Можно подставлять над и под уравнением непосредственно массу и объем веществ:
x л 72 г
2H2 + O2 = 2H2O
44,8 л 36 г
Билет № 24
1. Кислород: состав молекулы, физические и химические свойства.
Молекула кислорода O2 состоит из двух атомов кислорода, связанных ковалентной неполярной связью.
Представление о наличии в молекуле кислорода двух ковалентных связей не соответствует, в частности, её магнитным свойствам (жидкий кислород притягивается магнитом), поэтому лучше не останавливаться на этом моменте. В высшей школе изучается метод Молекулярных орбиталей о наличии в молекуле кислорода двух неспаренных электронов.
Кто скачивал билет №6 до 20 февраля 2011, пожалуйста, удалите примечание о строении молекулы кислорода.
Кислород – бесцветный прозрачный газ, без вкуса, без запаха. Немного тяжелее воздуха, сравнительно мало растворим в воде (в 1 литре воды при 20оC растворяется около 0,03 л кислорода).
Химические свойства:
Кислород активный окислитель. Многие вещества взаимодействуют с кислородом с выделением теплоты и света. Такие реакции называются горением:
1. S + O2 = SO2 (образуется оксид серы (IV), или сернúстый газ)
2. C + O2 = CO2 (образуется оксид углерода (IV), или углекислый газ)
Горение в чистом кислороде происходит гораздо энергичнее, чем в воздухе, так как выделяющаяся теплота не тратится на нагревание азота воздуха. Температура горения в чистом кислороде значительно выше.
Галогены, золото и платина не соединяются с кислородом напрямую, но можно получить их оксиды, в которых они проявляют положительную степень окисления, например, оксид хлора (VII) Cl2O7.
Фторид кислорода O+2F2-1 – соединение, в котором кислород проявляет положительную степень окисления.
3. Железо горит в кислороде с образованием железной окалины (представляет из себя смешанный оксид Fe+2O•Fe2+3O3):
3Fe + 2O2 = Fe3O4
4. При пропускании через воздух электрических разрядов, или во время грозы кислород превращается в озон – аллотропное видоизменение, состоящее из трех атомов кислорода:
3O2 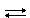 2O3
2O3
5. Пропитанные жидким кислородом угольный порошок, древесная мука и другие горючие материалы обладают взрывчатыми свойствами, используются при подрывных работах.
6. При участии кислорода в природе совершается важнейший процесс – дыхание. Транспорт кислорода из легких человека в ткани осуществляет гемоглобин крови, образующий комплекс с кислородом.
Кислород применяется
· в медицине при затрудненном дыхании,
· в металлургии,
· для газовой сварки и резки металлов и т.д.
