Определение концентрации приготовленного раствора титрованием
1. В 2 конические колбы пипеткой Мора отобрать аликвотные объемы приготовленного раствора 5 мл, добавить немного дистиллированной воды (до толщины слоя жидкости около 5 мм) и 2−3 капли индикатора – фенолфталеина.
2. Бюретку на 25 мл наполнить титрованным раствором едкого натра. Кончик бюретки должен быть заполнен раствором, а уровень жидкости доведен точно до нулевого деления. Затем медленно, по каплям, добавлять раствор щелочи из бюретки к аликвоте кислоты, непрерывно перемешивая раствор в конической колбе.
3. Эквивалентную точку определить по переходу окраски фенолфталеина от бесцветной к малиновой, сохраняющейся при перемешивании в течение 30 с.
4. Титрование повторить 2−3 раза, измеренные эквивалентные объемы щелочи усреднить.
Протокол лабораторной работы
1. Заданная преподавателем концентрация соляной кислоты 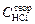 .
.
2. Расчет объема соляной кислоты, необходимого для приготовления 100 мл раствора кислоты заданной концентрации.
3. Объем аликвоты соляной кислоты, взятый для титрования, Va = ……., мл.
4. Концентрация раствора щелочи CNaOH = …….., экв/л.
5. Объем щелочи, пошедший на титрование пробы соляной кислоты:
VNaOH, 1 = …………., мл;
VNaOH,2 = …………., мл;
VNaOH,ср = …………, мл.
Обработка результатов эксперимента
Рассчитать концентрацию соляной кислоты по результатам титрования
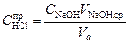
и определить отклонение от заданного значения концентрации соляной кислоты
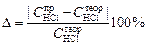 .
.
Содержание отчета по лабораторной работе
1. Название работы.
2. Цель работы.
3. Ход эксперимента.
4. Результаты эксперимента согласно протоколу лабораторной работы.
5. Обработка результатов эксперимента.
6. Выводы.
Лабораторная работа № 7. Исследование реакций в растворах электролитов
Цель работы: Ознакомиться с практическими выводами теории электролитической диссоциации, с реакциями в растворах электролитов и научиться составлять их уравнения.
Общие сведения
Электролитической диссоциацией называется процесс распада молекул электролитов на ионы под действием полярных молекул растворителя.
Количественно способность электролита распадаться на ионы характеризуют степенью диссоциации:
a = n/n0,
где n – число продиссоциированных молей; n0 – исходное число молей электролита.
Процесс диссоциации обратимый, он приводит к равновесию между недиссоциированными молекулами и ионами и, следовательно, должен подчиняться закону действующих масс. Вещество АВ при растворении в воде диссоциирует по уравнению:
АВ = А+ + В−
При постоянной температуре отношение произведения концентраций ионов и недиссоциированных молекул вещества постоянно и называется константой диссоциации:
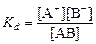 ,
,
где [А+], [В-], [АВ] – концентрации ионов и молекул электролита в растворе, моль/л или моль/кг.
По степени и величине константы диссоциации все электролиты принято условно делить на сильные и слабые. Сильные электролиты в растворе диссоциируют практически полностью, слабые - частично. Закон действующих масс справедлив лишь для слабых электролитов.
К сильным электролитам относят:
· Кислоты: азотную HNO3, серную H2SO4, соляную HCl, бромисто- и йодистоводородные HBr и HI, хлорную HClO4.
· Гидроксиды щелочных металлов, стронция и бария.
· Соли.
Остальные электролиты являются слабыми. Мало диссоциированными соединениями являются также комплексные ионы в растворе. Константы их диссоциации даны в справочниках.
Правила написания молекулярно-ионных уравнений реакций в растворах электролитов.
· Сильные электролиты записывают в диссоциированной форме, в виде отдельных составляющих их ионов.
· Слабые электролиты, сложные ионы, в том числе и комплексные, а также малорастворимые соединения и газы записывают в молекулярной, недиссоциированной форме.
· Одинаковые ионы в левой и правой частях уравнения сокращают, подобно правилам алгебры.
· Отсюда вытекают условия протекания реакций в растворах электролитов.
· Образование или растворение малорастворимого соединения, выпадающего в осадок. Растворимость соединений определяют по таблицам растворимости.
· Образование или разрушение мало диссоциированного соединения, иона или комплекса.
· Выделение или растворение газа.
Примеры написания уравнений реакций.
а) CaCl2 + 2AgNO3 = 2AgCl$ + Ca(NO3)2
Ag+ + Cl- = 2AgCl
б) 2NH4OH + H2SO4 = (NH4)2SO4 + 2H2O
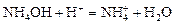
Выполнение работы
Опыт 1. Образование малорастворимых оснований.В одну пробирку налить 3−5 капель раствора соли железа (III), в другую – столько же раствора соли меди (II), в третью – раствора соли никеля (II). В каждую пробирку добавить по несколько капель раствора щелочи до выпадения осадков. Осадки сохранить до следующего опыта.
К какому классу относятся полученные осадки гидроксидов металлов? Будут ли эти осадки растворяться в избытке щелочи? Являются ли полученные гидроксиды сильными основаниями?
Опыт 2. Растворение малорастворимых оснований.К полученным в предыдущем опыте осадкам добавить по несколько капель раствора соляной кислоты концентрацией 15 % до их полного растворения.
Что происходит при растворении гидроксидов металлов в кислоте? Какое новое мало диссоциированное соединение при этом образуется?
Опыт 3. Образование малорастворимых солей. A. В две пробирки налить по 3−5 капель раствора нитрата свинца (II) и прибавить в одну пробирку несколько капель йодида калия, в другую – хлорида бария.
Ион какого металла образует осадки с ионами хлора и иода? Присутствие какого иона в составе соединения дает окраску иодида свинца? При помощи таблицы произведений растворимости определить, какой из образующихся осадков является менее растворимым.
Б. В одну пробирку налить 3−5 капель раствора сульфата натрия, в другую – столько же раствора сульфата хрома (III). В каждую пробирку добавить несколько капель раствора хлорида бария до выпадения осадков.
Какое вещество образуется в качестве осадка? Какой у него цвет? Будет ли протекать аналогичная реакция, например, с сульфатом железа (III)?
Опыт 4. Изучение свойств амфотерных гидроксидов. А.В две пробирки внести по 5 капель раствора соли цинка и несколько капель раствора едкого натра до образования осадка гидроксида цинка. Растворить полученные осадки в одной пробирке в растворе соляной кислоты, в другой – в избытке раствора едкого натра.
Б. В две пробирки внести по 5 капель раствора соли алюминия и несколько капель раствора едкого натра до образования осадка гидроксида алюминия. Растворить полученные осадки в одной пробирке в растворе соляной кислоты, в другой – в избытке раствора едкого натра.
В. В две пробирки внести по 5 капель раствора соли хрома (III) и несколько капель раствора едкого натра до образования осадка гидроксида хрома (III). Растворить полученные осадки в одной пробирке в растворе соляной кислоты, в другой – в избытке раствора едкого натра.
Какой из изученных гидроксидов металлов обладает более кислыми, а какой более основными свойствами? Расположить гидроксиды металлов в ряд по возрастанию их кислых свойств. Ответ обосновать строением атома элемента и его положением в периодической системе элементов.
Опыт 5. Образование малодиссоциированных соединений.В пробирку внести 3−5 капель раствора хлорида аммония и добавить несколько капель раствора едкого натра. Обратите внимание на запах, объясните его появление на основе уравнения реакции.
Опыт 6. Образование комплексов.В пробирку налить 5−7 капель раствора сульфата меди (II), затем по каплям добавить раствор аммиака до растворения образующегося осадка основной соли меди. Обратите внимание на окраску растворимого амминокомплекса меди.
Опыт 7. Образование газов. Внесите в одну пробирку 3−5 капель раствора карбоната натрия, в другую – столько же раствора сульфида натрия. В обе пробирки добавьте по несколько капель серной кислоты. Обратите внимание на выделение газов и их запах.
Опыт 8. Характер диссоциации гидроксидов. Пронумеровать 5 пробирок и внести по 4−5 капель растворов: в первую пробирку соли магния, во вторую соли алюминия, в третью силиката натрия, в четвертую соли никеля, в пятую соли цинка. Прибавить в пробирки 1, 2, 4, 5 по несколько капель (до начала выпадения осадков гидроксидов) раствор щелочи, в пробирку 3 − раствор соляной кислоты. Определить химический характер гидроксидов. Для этого половину суспензии гидроксида магния отлить в чистую пробирку и прибавить к ней 4−5 капель раствора НС1, к оставшейся части в первой пробирке добавить дополнительно 6−8 капель раствора щелочи.
В обоих ли случаях растворился осадок? Кислотными, основными или амфотерными свойствами обладает Mg(OH)2? Аналогичным образом исследовать свойства гидроксидов алюминия, кремния, никеля (II) и цинка. В чем они растворяются? Каковы их химические свойства?
