Периодические свойства химических элементов
Свойства химического элемента объединяют все без исключения его характеристики в состоянии свободных атомов или ионов, гидратированных или сольватированных, в состоянии простого вещества, а также формы и свойства образуемых им многочисленных соединений. Но обычно под свойствами химического элемента подразумевают, во-первых, свойства его свободных атомов и, во-вторых, свойства простого вещества. Большинство этих свойств проявляет явную периодическую зависимость от атомных номеров химических элементов. Среди этих свойств наиболее важными, имеющими особое значение при объяснении или предсказании химического поведения элементов и образуемых ими соединений являются:
энергия ионизации атомов;
энергия сродства атомов к электрону;
электроотрицательность;
атомные (и ионные) радиусы;
энергия атомизации простых веществ
степени окисления;
окислительные потенциалы простых веществ.
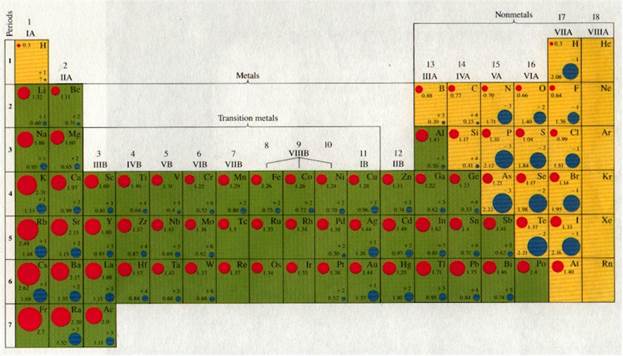
А́ТОМНЫЕ РА́ДИУСЫ, характеристики, позволяющие приближенно оценивать межатомные (межъядерные) расстояния в молекулах и кристаллах.
Под эффективным радиусом атома или иона понимается радиус сферы его действия, причем атом (ион) считается несжимаемым шаром. Используя планетарную модель атома, его представляют как ядро, вокруг которого по орбиталям вращаются электроны. Последовательность элементов в Периодической системе Менделеева соответствует последовательности заполнения электронных оболочек. Эффективный радиус иона зависит от заполненности электронных оболочек, но он не равен радиусу наружной орбиты. Для определения эффективного радиуса представляют атомы (ионы) в структуре кристалла как соприкасающиеся жесткие шары, так что расстояние между их центрами равно сумме радиусов. Атомные и ионные радиусы определены экспериментально по рентгеновским измерениям межатомных расстояний и вычислены теоретически на основе квантово-механических представлений.
Размеры ионных радиусов подчиняются следующим закономерностям:
1. Внутри одного вертикального ряда периодической системы радиусы ионов с одинаковым зарядом увеличиваются с возрастанием атомного номера, поскольку растет число электронных оболочек, а значит, и размер атома.
2. Для одного и того же элемента ионный радиус возрастает с увеличением отрицательного заряда и уменьшается с увеличением положительного заряда. Радиус аниона больше радиуса катиона, поскольку у аниона имеется избыток электронов, а у катиона – недостаток. Например, у Fe, Fe2+, Fe3+ эффективный радиус равен 0,126, 0,080 и 0,067 нм соответственно, у Si4-, Si, Si4+ эффективный радиус равен 0,198, 0,118 и 0,040 нм.
3. Размеры атомов и ионов следуют периодичности системы Менделеева; исключения составляют элементы от № 57 (лантан) до №71 (лютеций), где радиусы атомов не увеличиваются, а равномерно уменьшаются (так называемое лантаноидное сжатие), и элементы от № 89 (актиний) и дальше (так называемое актиноидное сжатие).
Атомный радиус химического элемента зависит от координационного числа. Увеличение координационного числа всегда сопровождается увеличением межатомных расстояний. При этом относительная разность значений атомных радиусов, соответствующих двум разным координационным числам, не зависит от типа химической связи (при условии, что тип связи в структурах со сравниваемыми координационными числами одинаков). Изменение атомных радиусов с изменением координационного числа существенно сказывается на величине объемных изменений при полиморфных превращениях. Например, при охлаждении железа, его превращение из модификации с гранецентрированной кубической решеткой в модификацию с объемно-центрированной кубической решеткой имеющее место при 906 оС, должно сопровождаться увеличением объема на 9%, в действительности увеличение объема составляет 0,8%. Это связано с тем, что за счет изменения координационного числа от 12 до 8 атомный радиус железа уменьшается на 3%. Т. е., изменение атомных радиусов при полиморфных превращениях в значительной степени компенсируют те объемные изменения, которые должны были бы произойти, если бы при этом не менялся атомный радиус. Атомные радиусы элементов можно сопоставлять только при одинаковом координационном числе.
Атомные (ионные) радиусы зависят также от типа химической связи.
В кристаллах с металлической связью атомный радиус определяется как половина межатомного расстояния между ближайшими атомами. В случае твердых растворов металлические атомные радиусы меняются сложным образом.
Под ковалентными радиусами элементов с ковалентной связью понимают половину межатомного расстояния между ближайшими атомами, соединенными единичной ковалентной связью. Особенностью ковалентных радиусов является их постоянство в разных ковалентных структурах с одинаковыми координационными числами. Так, расстояния в одинарных связях С-С в алмазе и насыщенных углеводородах одинаковы и равны 0,154 нм.
Ионные радиусы в веществах с ионной связью не могут быть определены как полусумма расстояний между ближайшими ионами. Как правило, размеры катионов и анионов резко различаются. Кроме того, симметрия ионов отличается от сферической. Существует несколько подходов к оценке величины ионных радиусов. На основании этих подходов оценивают ионные радиусы элементов, а затем из экспериментально определенных межатомных расстояний определяют ионные радиусы других элементов.
Ван-дер-ваальсовы радиусы определяют эффективные размеры атомов благородных газов. Кроме того, ван-дер-ваальсовыми атомными радиусами считают половину межъядерного расстояния между ближайшими одинаковыми атомами, не связанными между собой химической связью, т.е. принадлежащими разным молекулам (например, в молекулярных кристаллах).
При использовании в расчетах и построениях величин атомных (ионных) радиусов их значения следует брать из таблиц, построенных по одной системе
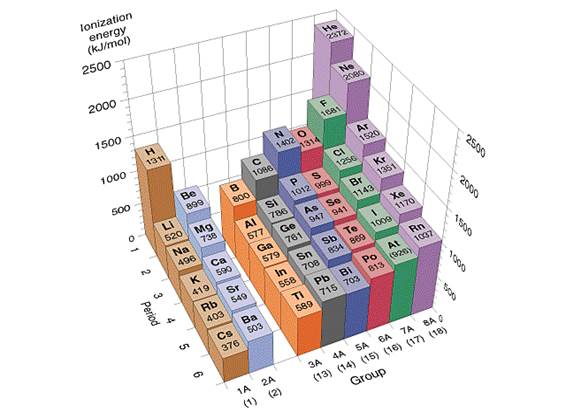
Проявления периодического закона в отношении энергии ионизации Энергия ионизации (Еи, I) - минимальная энергия, необходимая для отрыва наибольшее слабо связанного электрона от невозбужденного атома для процесса Эо + Eи → Э+ + ē
Выражается в кДж/моль. Определяется зарядом ядра, радиусом атома и конфигурацией внешних электронных оболочек.
По периоду слева направо с ростом заряда ядра и уменьшением атомного радиуса Eи увеличивается. В А-группах сверху вниз с увеличением атомного радиуса Eи уменьшается. Энергия ионизации (Eи) характеризует проявление металличности у атомов элементов. Чем меньше Eи, тем более выражена способность атома отдавать электроны, его восстановительные и металлические свойства.
Энергия ионизации — разновидность энергии связи или, как её иногда называют, первый ионизационный потенциал (I1), представляет собой наименьшую энергию, необходимую для удаления электрона от свободного атома в его низшем энергетическом (основном) состоянии на бесконечность.
Энергия ионизации является одной из главных характеристик атома, от которой в значительной степени зависят природа и прочность образуемых атомом химических связей. От энергии ионизации атома существенно зависят также восстановительные свойства соответствующего простого вещества.
Для многоэлектронного атома существуют также понятия второго, третьего и т. д. ионизационных потенциалов, представляющих собой энергию удаления электрона от его свободных невозбуждённых катионов с зарядами +1, +2 и т. д. Эти ионизационные потенциалы, как правило, менее важны для характеристики химического элемента.
Энергия ионизации всегда имеет эндоэнергетическое значение (это понятно, так как чтобы оторвать электрон от атома, требуется приложить энергию, самопроизвольно это произойти не может).
На энергию ионизации атома наиболее существенное влияние оказывают следующие факторы:
эффективный заряд ядра, являющийся функцией числа электронов в атоме, экранирующих ядро и расположенных на более глубоко лежащих внутренних орбиталях;
радиальное расстояние от ядра до максимума зарядовой плотности наружного, наиболее слабо связанного с атомом и покидающего его при ионизации, электрона;
мера проникающей способности этого электрона;
межэлектронное отталкивание среди наружных (валентных) электронов.
На энергию ионизации оказывают влияние также и менее значительные факторы, такие, как квантовомеханическое обменное взаимодействие, спиновая и зарядовая корреляция и др.
Энергии ионизации элементов измеряется в Электронвольт на 1 атом или в Джоуль на моль.
Энергии ионизации элементов.
Энергия последовательной ионизации In (кДж/моль) атомов элементов третьего периода Элемент I1 I2 I3 I4 I5 I6 I7
Na 495,8 4564 — — — — —
Mg 737,7 1451 7730 — — — —
Al 577,6 1817 2744 11600 — — —
Si 786,5 1577 3228 4350 16100 — —
P 1011,8 1904 2910 4950 6270 21200 —
S 999,6 2253 3380 4565 6950 8490 27000
Cl 1251,2 2296 3850 5160 6560 9360 11000
Ar 1520,6 2666 3946 5770 7230 8780 12000
Зависимость энергии ионизации атома от порядкового номера элемента носит отчетливо периодический характер. Легче всего удалить электрон из атомов щелочных металлов, включающих по одному валентному электрону, труднее всего — из атомов благородных газов, обладающих замкнутой электронной оболочкой. Поэтому периодичность изменения энергии ионизации атомов характеризуется минимумами, отвечающими щелочным металлам, и максимумами, приходящимися на благородные газы. Наряду с этими резко выраженными минимумами и максимумами на кривой энергии ионизации атомов наблюдаются слабо выраженные минимумы и максимумы, которые по-прежнему нетрудно объяснить с учетом упомянутых эффектов экранирования и проникновения, эффектов межэлектронных взаимодействий и т. д.