Индикаторы окислительно-восстановительного титрования
В ряде случаев ОВ титрования точку эквивалентности фиксируют по изменению окраски титруемого раствора, вызываемой избытком окрашенного стандартного раствора. Кроме того, могут быть использованы в методах окисления-восстановления так называемые red–ox-индикаторы, которые изменяют окраску в зависимости от величины Е. Наиболее широко для фиксирования точки эквивалентности применяют физико-химические методы.
В качестве стандартного раствора в перманганатометрии применяют раствор, KMnO4 который обладает наиболее высокой окислительной активностью в кислой среде E= 1,15В.
Здесь индикатор – сам реактив, который в кислой среде обесцвечивается. В случае применения сильно разбавленных растворов или титрования окрашенных растворов в качестве индикатора используется дифениламин – ОВ индикатор.
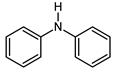
Обратимые ОВ индикаторы – органические соединения, имеющие в окисленной и восстановленной форме различную окраску:
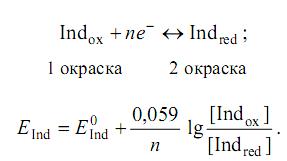
Изменение окраски индикатора зависит от соотношения концентрации Ind окисленной и восстановительной формы.
Как и для кислотно-основных индикаторов человеческий глаз воспринимает окраску раствора той формы индикатора, концентрация которой приблизительно в10 раз больше концентрации другой формы того же индикатора, т.е. при [IndOx]/[IndRed] = 10 раствор принимает окраску окисленной формы и наоборот.
При n=1и отношении 10:1 или 1:10 интервал перехода индикатора рассчитывают по формуле
EInd=E0Ind ±0,059 (20)
Другим примером обратимых red-ox-индикаторов является свежеприготовленный раствор крахмала, который окрашивается в синий цвет в присутствии йода.
Перманганатометрия
Титрант – 0,1; 0,05 н растворKMnO4, стандартизацию раствора которого проводят по стандартному раствору щавелевой кислотыH2С2O4·2H2Oна основе реакции:
2MnO4- + 5H2С2O4 + 6H+ = 2Mn2+ + 10CO2↑ + 8H2O
Водные растворыKMnO4неустойчивы вследствие протекания реакции
4MnO4- + 2H2O = 4MnO2 + 3O2 + 4OH-.
Эта реакция ускоряется при действии света, поэтому раствор KMnO4 хранят в склянках из тёмного стекла. Условия титрования: среда – сильно кислая (H2SO4), нагревание (60…80 °С), медленное титрование (особенно в начале), индикатор – титрантKMnO4.
Для определения восстановителей применяют прямое титрование. Используя обратное титрование, определяют содержание окислителей.
Перманганатометрия – один из самых распространённых методов ОВ титрования.
Достоинства метода: титрование проводится без индикатора, высокое значение ОВ потенциала в кислой среде (+1,51В) позволяет определять большое количество веществ с меньшим значением Е; доступность титранта.
Недостатки метода: невозможность приготовления стандартного раствора титранта по точной навеске, его нестабильность при хранении, необходимость строгого соблюдении условий проведении титрования, регламентируемых соответствующей методикой.
Окислительно-восстановительных методы широко используются для определения металлов и неметаллов в объектах металлургических производств.
Наиболее широко используются методы: перманганатометрии для определения V, Mo, W, U, Ti, Nb, Sn, Sb, Fe, Ca, Mg и др.; йодометрии - Cu, Sn; броматометрии -As, Fe, S, Sb, Sn и др.
Контрольные вопросы:
1. Каков основной принцип титриметрического анализа?
2. Что такое стандартный (рабочий, титрованный) раствор?
3. Какие методы используют при стандартизации растворов?
4. Что такое установочные вещества и какие требования к ним предъявляются?
5. Какие растворы называют приготовленными, а какие – установленными? Привести примеры.
6. В чем сущность титрований: прямого, обратного, по замещению? Привести примеры.
7. По каким формулам рассчитывают результаты прямого титрования, обратного титрования, титрования по замещению ?
8. В чем заключается сущность метода кислотно – основного титрования?
9. Какие первичные и вторичные стандартные вещества используют в ацидиметрии и алкалиметрии?
10. Что такое кривая титрования, скачок титрования, точка эквивалентность?
11. Какие требования предъявляются к окислительно-восстановительным реакциям в титриметрическом анализе?
12. Какими способами можно зафиксировать конечную точку титрования в методах окисления – восстановления?
13. Сущность методов перманганатометрии.
