Принципы заполнения атомных орбиталей электронами
Число электронов в атоме химического элемента определяется зарядом ядра, который равен порядковому номеру этого элемента в периодической системе Д.И.Менделеева. Распределение электронов в атомах подчиняется трём основным принципам.
1. Принцип минимума энергии.Электроны в невозбуждённом атоме распределяются по энергетическим уровням и подуровням так, чтобы их суммарная энергия была минимальна. Энергия электрона в атоме в основном определяется главным и орбитальным квантовыми числами, поэтому сначала заполняются те подуровни, для которых сумма (n+l) является наименьшей (правило В.М.Клечковского). В соответствии с этим в многоэлектронном атоме наблюдается следующая последовательность: 1s < 2s < 2p < 3s < 3p < 4s < 3d < 4p < 5s < 4d < 5p < 6s < 4f ≈ 5d < 6p < 7s < 5f ≈ 6d < 6p. Эту последовательность можно представить в краткой форме: Еns < E (n – 1)d ≈ E(n - 2)f < Enp
2. Принцип Паули. В атоме не может быть двух электронов с одинаковым набором всех четырёх квантовых чисел.
3. Правило Гунда. В невозбуждённых атомах электроны в пределах данного подуровня занимают максимальное число свободных орбиталей, при этом суммарный спин максимален.
Основные характеристики атомов элементов
1. Радиус атома. Размер атома не может быть определён точно, т.к. электронные орбитали атомов не имеют строго ограниченных контуров. Следовательно, речь может идти не об абсолютных размерах атомов, а только о размерах этих частиц в кристаллах и молекулах, т.е. об эффективных радиусах (rат). Эффективные радиусы атомов периодически изменяются в зависимости от заряда их ядра и числа электронов. В периоде с возрастанием заряда ядра атомные радиусы уменьшаются вследствие увеличения сил взаимодействия электронов и ядром. В группах атомные радиусы элементов, как правило. Возрастают сверху вниз, т.к. увеличивается число электронных слоёв в атомах элементов.
Орбитальный радиус несвязанного атома рассчитывается квантово-химическими методами как расстояние от его ядра до максимума электронной плотности, относящегося к последней занятой электронной орбитали.
В группах для однотипных элементов при движении сверху вниз наблюдается закономерный рост орбитальных радиусов, что связано с увеличением числа электронных оболочек. В периодах при движении слева направо прослеживается, как правило, уменьшение орбитальных радиусов.
Отклонение от такого закономерного уменьшения орбитальных радиусов наблюдается, например, при переходе от Mg к Al и объясняется тем, что последний электрон в атоме Al уже занимает 3p-орбиталь, а это способствует увеличению орбитального радиуса. Аналогичное возрастание орбитального радиуса атома по той же причине происходит и при переходе от Zn к Ga. Приводимые ниже радиусы связанных атомов (атомные, металлические) найдены путем деления пополам кратчайших межатомных расстояний в кристаллических структурах простых веществ с координационным числом 12. При других значениях координационные числа в соответствующие данные внесены необходимые поправки. Обратим внимание, что в кристалле радиус атома гелия намного больше аналогичного для атома водорода. Объяснить это можно, если принять во внимание запрет на перекрывание атомных орбиталей для атомов гелия и отсутствие такого запрета для атомов водорода.
На рисунке 1. сопоставлены орбитальные и атомные радиусы атомов.
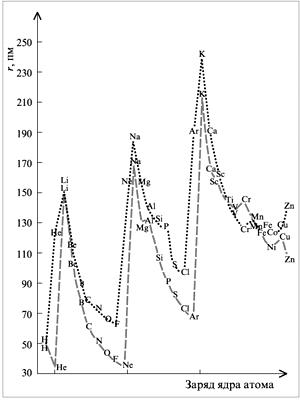 |
| Рис. 1. Графическое сравнение орбитальных (пунктир) и атомных (точки) радиусов атомов |
2. Энергия ионизации. Еи – это энергия отрыва электрона от атома элемента с образованием катиона: Э – ē → Э+ (кДж/моль). В периоде наибольшую Еи имеют элементы IA группы (щелочные металлы), т.к. в атомах этих элементов на внешнем энергетическом уровне находится 1 электрон, который значительно удалён от ядра. Поэтому характерной особенностью щелочных металлов является склонность к отдаче электронов (металлические свойства). В пределах каждой группы А энергия ионизации уменьшается сверху вниз, что свидетельствует о большем взаимодействии между ядром и электронами. В группах Б (d-элементы), за исключением IIIБ, изменение энергии ионизации носит обратный характер – она увеличивается сверху вниз.
Различают первую, вторую, третью и т. д. энергии ионизации атома. Первая энергия ионизации– это минимальная энергия, необходимая для удаления первого электрона из основного состояния атома. Вторая энергия ионизации – минимальная энергия, необходимая для удаления второго электрона из основного состояния однозарядного катиона. Аналогично определяются третья и последующие энергии ионизации атома. Очевидно, что для удаления второго электрона необходимо затратить больше энергии, чем для удаления первого электрона. Этот факт объясняется тем, что второй электрон приходится удалять уже из однозарядного катиона. Рассмотрим первые энергии ионизации для некоторых элементов периодической системы Д.И.Менделеева (таблица 3).
Таблица 3 Первые энергии ионизации некоторых атомов, МДж/моль
| Периоды | Группы элементов | |||||||
| I | II | III | IV | V | VI | VII | VIII | |
| Н 1,31 | He 2,37 | |||||||
| Li 0,52 | Be 0,90 | B 0,80 | C 1,09 | N 1,40 | O 1,31 | F 1,68 | Ne 2,08 | |
| Na 0,49 | Mg 0,74 | Al 0,58 | Si 0,79 | P 1,01 | S 1,00 | Cl 1,25 | Ar 1,52 | |
| K 0,42 | Ca 0,59 | Sc 0,63 | Ti 0,66 | V 0,65 | Cr 0,65 | Mn 0,72 | Fe 0,76 Co 0,76 Ni 0,74 | |
| Cu 0,74 Rb 0,40 | Zn 0,91 Sr 0,55 | Ga 0,58 | Ge 0,76 | As 0,94 | Se 0,94 | Br 1,14 | Kr 1,35 |
Анализ первых энергий ионизации атомов показывает, что в целом наблюдается закономерность роста этих величин в периодической таблице при движении слева направо и снизу вверх. Имеются и объяснимые исключения. Например, энергия ионизации атома Be (0,90) выше аналогичной характеристики атома B (0,80). Этот факт легко объяснить, если принять во внимание, что третий электрон во втором электронном слое атома В помещается уже на 2р-орбиталь. Здесь сказывается взаимное отталкивание этого электрона и находящихся в предыдущем электронном подслое. Аналогичное исключение наблюдается и при переходе от Mg к Al.
На рисунке 2 графически представлены первые энергии ионизации атомов первых 36 элементов периодической системы Д.И.Менделеева.
3. Энергия сродства к электрону. Еср – это энергия присоединения электрона к электронейтральному атому элемента с образованием аниона:
Э + ē → Э– (кДж/моль).
Она возрастает у элементов в пределах периода слева направо, достигая максимума у галогенов. У элементов группы А сверху вниз наблюдается уменьшение энергии сродства вследствие существенного увеличения радиуса. У элементов группы Б наобарот.
При анализе данных в таблицы 4 можно заметить как положительные, так и отрицательные значения сродства атомов к электрону. Отрицательные значения сродства показывают, что для присоединения еще одного электрона к атому энергию необходимо затратить.
Таблица 4 Сродство атомов к электрону, кДж/моль
| Периоды | Группы элементов | |||||||
| I | II | III | IV | V | VI | VII | VIII | |
| Н 73 | He < 0 | |||||||
| Li 16 | Be < 0 | B 27 | C 122 | N < 0 | O 141 | F 328 | Ne < 0 | |
| Na 53 | Mg < 0 | Al 43 | Si 134 | P 72 | S 200 | Cl 328 | Ar < 0 | |
| K 48 | Ca < 0 | Sc 18 | Ti 8 | V 51 | Cr 64 | Mn < 0 | Fe 16 Co 64 Ni 112 | |
| Cu 119 Rb 47 | Zn < 0 Sr < 0 | Ga 30 | Ge 107 | As 78 | Se 195 | Br 325 | Kr < 0 |
4. Относительная электроотрицательность (ОЭО). Это величина, характеризующая относительную способность атома элемента притягивать к себе общие электроны в молекуле. За единицу принята ЭО атома лития, у фтора этот показатель равен 4. у элементов в пределах периода с увеличение заряда ядра наблюдается увеличение ЭО. В соответствии с этим элементы становятся всё более слабыми восстановителями и всё более сильными окислителями. Внутри группы ЭО элементов уменьшается сверху вниз.
Химическая связь
Химическая связь – это взаимодействие, которое связывает отдельные атомы в молекулы, ионы, радикалы, кристаллы.
Основным условием образования химической связи является понижение общей энергии Е многоатомной системы по сравнению с энергией изолированных атомов, т.е.
А + В → АВ
атом атом молекула
ЕАВ < EA + EB
Различают 3 типа химической связи: ковалентная, ионная и металлическая.
Соединения с металлической связью имеют два важных отличия от ионно-ковалентных соединений:
1. Высокая электро- и теплопроводность,
2. Металлы – кристаллические вещества (исключение – ртуть).
Свойства химической связи
1. Энергия связи. Это та энергия, которая необходимая для её разрыва; она всегда больше нуля. Энергия разрыва равна по величине, но противоположна по знаку энергии образования. Наиболее прочная связь в молекулах N2 (945.3 кДж/моль) и СО (1070.0 кДж/моль). Самая слабая связь между атомами азота в N2O3 (40.6 кДж/моль).
Экспериментально энергия разрыва определяется по закону Гесса.
2. Длина связи. Это расстояние между ядрами атомов, соединенных связью. Её можно экспериментально измерить с помощью рентгеноструктурного метода. Обычно длина ковалентной связи составляет 0.1 – 0.2 нм. Самая короткая связь в молекуле дейтеро водорода НD (0.074нм). Рекорд в длине связи принадлежит атомам гелия Не…Не – 6.2нм.
3. Кратность (порядок) связи. В различных теориях строения химической связи кратность определяют по-разному. В теории электронных пар Льюиса порядок связи – это число электронных пар, осуществляющих химическую связь. Порядок может быть целым и дробным. Так порядок связи в О2 равен 2, в молекулярном ионе О2- = 2.5, а в ионе О2+ = 1.5. Чем выше кратность связи, тем большее число электронов обеспечивает связь, и тем труднее её разорвать. Так, энергия тройной связи НС ≡ СН 962 кДж/моль, двойной связи Н2С = СН2 712кДж/моль и одинарной Н3С – СН3 369кДж/моль.
4. Полярность связи. Она показывает, насколько электронная плотность смещена к одному из атомов. Способность атома смещать к себе электронную плотность химической связи называется электроотрицательностью. Самые электроотрицательные элементы – активные неметаллы: F, O, N, Cl; самые электроположительные – щелочные металлы. Чем больше разность электроотрицательностей атомов, участвующих в химической связи, тем более полярна связь. Предельный случай полярной связи – ионная. Количественно величина полярности определяется дипольным моментом (μ), который равен произведению эффективного заряда на расстояние между атомами. μ = q × l. Единица измерения - дебай [D = 3.3 × 10-30 Кл × м]. Чем больше дипольный момент, тем более полярна молекула.
HCl HBr HI
μ, D 3.24 2.87 1.14
Дипольный момент уменьшается, т.к. уменьшается разница электроотрицательностей между атомами.
5. Угол связи. Это угол между воображаемыми прямыми, соединяющими центры атомов.
Ковалентная связь
В 1927 году учёные Гейтлер и Лондон, рассматривая молекулу водорода сделали вывод о том, что связь образуется только в том случае, если спины электронов разнонаправлены. А связь, образованная за счёт общей пары электронов, получила название ковалентной.
Существует 2 метода описания связи:
1. МВС – метод валентных связей, предложен американскими учёными Слейтером и Полингом;
2. ММО – метод молекулярных орбиталей (Малликен).
Основные положения МВС:
1. Связь возникает между двумя атомами при обобществлении двух электронов с разными спинами или один из атомов предоставляет пару электронов с противоположными спинами, а другой – свободную орбиталь.
А↓ + В↑ → А↓↑В или А↑↓ + ٱВ → А↓↑В. Рассмотрим образование связи в молекуле СО
2. Связь возникает в том направлении, в котором перекрывание электронных облаков максимально.
3. Из двух орбиталей атома наиболее прочную связь образует та орбиталь, которая сильнее перекрывается орбиталью другого атома.
