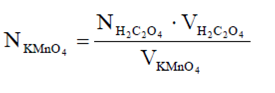Як готують та встановлюють концентрацію робочого розчину в перманганатометрії?
Нормальність. Переваги способу вираження концентрації розчинів через нормальність. Властивості нормальних розчинів.
Нормальна концентрація або нормальність, N - число, що показує, скільки еквівлентів (г/екв) речовини міститься в 1 літрі розчину. Розчин, в 1 л якого розчинений 1 еківалент речовини, називається однонормальним розчином.
В об’ємному аналізі найчастіше використовують нормальні концентрації розчинів. Це пов’язано з двома обставинами:
1) розчини з однаковими нормальностями реагують в однакових об’ємах;
2) нормальність розчину - це число, множенням на яке ми зводимо об’єм розчину будь-якої нормальності до об’єму точно однонормального розчину.
При титриметричних визначеннях розчин речовини невідомої нормальності Nx, взятий у певному об”ємі V1, титрують відповідним робочим розчином, нормальність якого Npp відома. Об’єм робочого розчину, витраченого на титрування (відрахованого за допомогою бюретки), - Vpp. Добуток VppNpp згідно з 2), дорівнює кількості мілілітрів точно однонормального робочого розчину визначуваної речовини. Однонормальні розчини реагують у рівних об’ємах. Тому
V1Nx= VppNpp
Чим характеризується точка еквівалентності в методі нейтралiзaцiї? індикатори, які використовуються в методі нейтралізації.
Точка эквивалентности в методе нейтрализации определяется по изменению окраски индикатора.
Залежно від способу застосування вони бувають внутрішніми і зовнішніми. Внутрішні індикатори вводять безпосередньо в розчин, який титрують. У більшості випадків користуються внутрішніми індикаторами. Зовнішні - це смужки паперу, змочені розчином індикатора.
Метиловий фіолетовий, тимоловий синій, метилоранж, метиловий червоний, бромфенол синій, фенолфталеїн, тимолфталеїн.
Хімічний еквівалент. Як обчислюють молярну масу еквіваленту сполуки в кислотно-основних реакціях? Наведіть приклади.
Хімічним еквівалентом сполуки називають таку її кількість, яка взаємодіє з 1 моль атомів (одним еквівалентом) водню або іншого одновалентного елементу. Еквівалент не є сталою величиною, а залежить від хімічної реакції, в якій бере участь речовина. Якщо порівняти дві хімічні реакції
Na2CO3 + HCl = NaCl + NaHCO3
Na2CO3 + 2HCl = H2O + 2NaCl + CO2
то в першій еквівалент соди дорівнює її молекулярній масі (заміщується один атом водню кислоти), тобто 106. У другу реакцію вступають 2 атоми водню (з двох молекул НСl). Тому еквівалент соди буде дорівнювати половині її молекулярної маси, тобто 53 г.
Як готують та встановлюють концентрацію робочого розчину в перманганатометрії?
Робочим титрованим розчином слугує перманганат калію. Перманганат калію не належить до вихідних речовин, тому що завжди містить домішки двооксиду марганцю, від якого дуже важко позбутись. Окрім цього, концентрація перманганату калію з часом змінюється під дією світла і внаслідок відновлення його невеликою кількістю органічних речовин, які попадають у розчин з пилом.
Тому розраховану кількість перманганату калію зважують на технічних терезах і готують розчин приблизної концнтрації, відміряючи дистильовану воду мірним циліндром. Точну концентрацію встановлюють через 10-12 днів за вихідною речовиною - щавлевою кислотою.
Методика
Бюретку наповнюють розчином перманганату калію. У колбу для титрування піпеткою переносять 20(25) мл вихідного розчину щавлевої кислоти, додають 15-20 мл розчину сірчаної кислоти (1:4) для створення кислотності середовиища. Нагрівають розчин до 70-80 оС (не можна доводити до кипіння, тому що в такому випадку розкладається щавлева кислота) і титрують розчином перманганату калію. На початку титрування до гарячого розчину щавлевої кислоти додають декілька краплин перманганату і чекають зникнення рожевого забарвлення. Кожну нову порцію розчину перманганату додають після зникнення забарвлення попередньої порції. Титрують до появи забарвлення, яке не зникає протягом 30 сек. Нормальність розчину визначають за формулою: