ОПЫТ 8. Определение порога коагуляции электролита для золя Fe(OH)3, полученного по реакции гидролиза
В 5 пробирок налейте по 9 мл раствора NaCl различной концентрации, в другие 5 пробирок налейте по 9 мл растворов MgSO4 таких же концентраций. В каждую пробирку добавьте по 1 мл золя Fe(OH)3 и перемешайте. Коагуляцию наблюдайте по появлению помутнения раствора в пробирке. Смотрите в пробирку сверху: если раствор остался прозрачным – коагуляции нет (-), если помутнел – коагуляция есть (+). Результаты наблюдений занесите в табл. 29. Для каждого электролита отметьте пороговую концентрацию.
Рассчитайте для каждого электролита порог коагуляции (Ск) и коагулирующее действие.
Таблица 29
| Электролит | Концентрация электролита, моль/л | Пороговая концентрация, моль/л | Cк, моль/л | D | Ион, вызывающий коагуляцию |
| 10-6 10-5 10-4 10-3 10-2 |
ВЫВОДЫ:
1. Покажите строение мицеллы золя Fe(OH)3, полученного по реакции гидролиза.
2. Сравните коагулирующее действие NaCl и MgSO4. Какие ионы вызывают коагуляцию?
3. Объясните различия в коагулирующем действии этих электролитов.
КОНТРОЛЬНЫЕ ВОПРОСЫ:
1. Факторы устойчивости различных ДС.
2. Агрегативная и кинетическая устойчивости.
3. Методы осаждения НМС, их механизм.
4. Высаливание ВМС из растворов. Механизм. Схема Кройта. Лиотропные ряды.
5. Денатурация белков. Виды денатурации. Механизм.
6. Коагуляция КДС. Механизм. Коагулирующее действие электролитов. Порог коагуляции. Правило Шульце-Гарди.
7. Осаждение ГДС. Разрушение эмульсий.
8. Сущность явления «коллоидной защиты».
9. Сравнительная характеристика устойчивости ДС,
ОБРАЗЕЦ ОТВЕТА НА ВОПРОС:
ВОПРОС: к 10 мл отрицательного золя СаСО3 для его коагуляции необходимо добавить 10 мл 10-4 М раствора КС1 или 10 мл 10-6 М раствора А1С13. Определите порог коагуляции и коагулирующее действие каждого электролита. Поясните механизм коагулирующего действия.
ОТВЕТ:
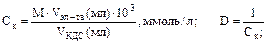
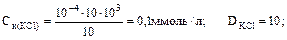
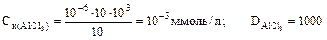
Запишем мицеллу золя СаСО3, взяв в качестве стабилизатора Na2CO3. Т.к. гранула имеет отрицательный заряд, коагуляцию вызывают К+ или А13+. Ион А13+ имеет меньший порог коагуляции, чем ион К+, что соответствует правилу Шульце-Гарди (Ск = А/Z6). Связано это с механизмом коагуляции. При добавлении электролита коагулирующие ионы (К+ или А13+) адсорбируются на грануле и нейтрализуют заряд. Ионы А13+ нейтрализуют частицу лучше, т.к. величина его заряда больше. Следовательно, для нейтрализации заряда гранулы достаточно меньшего количества ионов А13+, чем К+. При нейтрализации заряда гранулы происходит также сжатие диффузионного слоя, уменьшение ζ. Мицелла теряет свойство удерживать воду. Частицы коллоида теряют заряд (ζ → 0) и сольватную оболочку. Происходит осаждение золя.
ЛИТЕРАТУРА:
1. С. 510-523, 543-545; 3. С. 179-192; 5. С. 118-121, 126-127; 6. С. 718-727.
РАБОТА 27. РАСТВОРЫ ЭЛЕКТРОЛИТОВ.
