Задача 4. Коррозия металлов и защита от коррозии
Московский Энергетический Институт
(Технический университет)
Кафедра ХИЭЭ
Самостоятельная работа № 5
Тема: электрохимичекие процессы
Вариант № 16
Студент: Кобляков Антон
Группа Э-04-12
Преподаватель: Корнеева.Л.А
Задание 1
Вычислите потенциал серебряного электрода, помещенного в насыщенный раствор соли Ag2So4. Пр=1,2*10-5
Пр=1,2*10-5= 2с2*с=4с3
Сmax= 3√ ( Пр/4)=0,019 моль
С [ Ag+ ]=2Cmax=0.03 моль
ЕрAg+/Ag= E0Ag+/Ag=0.059/1*lg0.03 = 0.709 В
Задание 2
2.1 Составьте схему концентрационного ГЭ, одним из электролитов которого будет электрод задачи 1, а второй подберите сами. Рассчитайте ЭДС и Аmax этого гальванического элемента.
Ag|Ag2SO4 c=0.015 м|| AgNO3 c=1м|Ag
C = 1 моль/л С = 0,01 моль/л
E=Ek-Ea
а(Ме) = С=0,01 моль/л
EpAg+/Ag=E0Ag/Ag+ 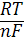 lna(Me) = 0,709 B
lna(Me) = 0,709 B
C = 1 моль/л
EpAg+/Ag=E0Ag+/Ag = 0,709 B
(K-) Ag|Ag2SO4|| Ag2SO4|Ag (A+)
Ep(2) = 0,799 B – (0,0591/1*lg1) B = 0,799 B
Ep=Ep(2)-Ep(1)
Cu0 + 2e—> Cu2+ |1
Ag+ + e —> Ag0 |2
Amax= n*F*E = 0 B
Cu0 + 2Ag+ —> Cu2+ + 2Ag0
2.2Схема гальванического элемента, катодом в котором будет электрод задачи 1, а анод подберите сами.
ГЭ: (К) Pd (А) Pb
2.2.1 Напишите электродные процессы и токообразующую реакцию E0Pb2+/Pb=-0.126 B
E0Pd2+/Pd= +0,987 В
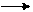 (K-) Pd2+ +2e Pd
(K-) Pd2+ +2e Pd
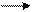 (A+) Pb Pb2+ + 2e
(A+) Pb Pb2+ + 2e
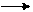 TOP : Pd2+ + Pb Pd + Pb2+
TOP : Pd2+ + Pb Pd + Pb2+
2.2.2 а)Термодинамический подход
E = -GTOP/(n*F)
∆GТОР=∆Gпрод-∆Gисх= -200,8 кДж
Е = 1,04 В
б)Электрохимический метод
E=Ek-Ea
E= 1,1 В
Небольшое различие в величинах ЭДС обусловлено наибольшей точностью термодинамического подхода в расчете ЭДС. Термодинамический подход имеет большую точность по причине того что в нем используются энергия Гиббса токообразующей реакции и число Фарадея.
2.2.3Температурная зависимость гальванического элемента.
EpPd2+/Pd=E0Pd2+/Pd+ 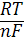 lna(Me)
lna(Me)
Температура влияет прямо пропорционально на ЭДС гальванического элемента. С увеличением температуры увеличивается разность потенциалов гальванического элемента.
2.2.4Ход поляризационных кривых
 Е, В
Е, В

 +0,987
+0,987
 Е
Е 
I, мА/см2
 -0.126
-0.126
2.2.5U=E-Ir-∆E
Для того, чтобы повысить U необходимо увеличить c Ag+ то есть заменить
Ag2SO4 на более растворимую соль серебра например AgNO3 или уменьшить концентрацию Сu2+ разбавив раствор или частично слив. Увеличить напряжение ГЭ можно, повысив ЭДС, уменьшив омические потери и поляризацию электродов.
Задача 3. Электролиз водных растворов.
Задание 1
Напишите уравнение возможных электродных процессов при электролизе водного раствора на электродах
 3.1 Fe | FeSO4 | Fe
3.1 Fe | FeSO4 | Fe
A: Fe2+ + 2e —> Fe0
2Н+ + 2е —> H2 | Электрохимическое родонирование K: Fe0 - 2e —> Fe2+ Способ очистки металлов
H2O – 2e —> 2H+ + ½ O2 |
2Fe2 + 3/2 O2 —> Fe2O3
3.1.1
Umin= E0
E0= E0 Fe2+/Fe0 ( 0.059/2 )*lg [ Fe+ ] – (E0* Fe2+/Fe0 + (0.059/2) lg [ Fe2+ ] ) + E0 O2/OH- - E0*H/H+ =1.23 В
EpH+/H2=-0.059pH, pH≈5, EpH+/H2=-0.295B
E0Cu2+/Cu=0.337
Разница меньше единицы, по-этому на катоде будут проходить 2 процесса одновременно.
A: 4OH-→O2+2H2O+4e
K: Cu2+ + 2e→ Cu
2H++2e→H2↑
3.1.2Изменятся ли электродные процессы, если заменить электроды на другие Рt ? В случае изменения показать ход поляризационных кривых.
3.1.3Pt | FeSO4 | Pt
K: Fe2+ + 2e —> Fe0
2H+ + 2e —> H2 |
А: Н2О – 2е —> ½ O2 + 2H+
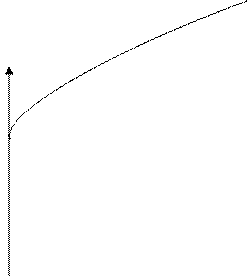
EpO2/OH-
Umin
 E0Fe2+/Fe
E0Fe2+/Fe

EpFe2+/Fe Fe,k
3.1.3При замене исходных электродов на графитовые электроды электродные процессы не изменяются, поскольку графитовые электроды являются инертными.
Задание 3.2
Определение время необходимое для электрохимической прошивке в заготовке из Ti отверстия диаметром d=0,5 см и глубиной h=2 см. Процесс проводят в растворе NaCl при силе тока I=50 A и анодном выходе металла по току равном Вi= 50% ,р. металла 4,5 г/см3 . Напишите уравнение электродных процессов.
Ti=m/M=V*p/m= ( П* r2*h*p)/ M=0.1476 моль
EpH+/H2 = -0,059 pH = -0,413 B
E0Na+/Na = -2,714 B
EpO2/OH- = 0,817 B
E0Cu2+/Cu = 0,337 B
E0Cl2/Cl- = 1,359 B
EpH+/H2 > E0Na+/Na
K: 2H+ + 2e → H2
A: 4OH- → O2 + 2H2O + 4e
Cu → Cu2+ + 2e
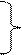 11.2л - 96500 А*с
11.2л - 96500 А*с
q=965 А*с
0.112л - х А*с
Q(Cu) = 0,95q = 916,75
m= 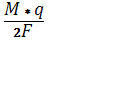 = 0,304 г
= 0,304 г
V = m/ 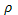 = 0,034 см3
= 0,034 см3
H = 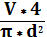 = 0,04 см
= 0,04 см
Задача 4. Коррозия металлов и защита от коррозии.
3.1 Определение возможности коррозии сплава Fe – Co в водном растворе CuSo4 c концентрацией 0,02 моль/л при 298 К и относительном парциальном давлении кислорода 0,48, считая относительное парциальное давление водорода равным 1. Рассчитатйте рН раствора
3.2 Уравнение процессов, протекающих при коррозии.
ZnCl2 → Zn2+ + 2Cl-
Соль образована слабым основанием Zn(OH)2 и сильной кислотой HСl
Гидролиз слабой части соли:
Zn2+ + HOH→ ZnOH+ + H+
ZnOH+ + HOH→ Zn(OH)2 + H+
Кд2(Zn(OH)2) = 1,5*10-9
Кг = Кw/ Кд2(Zn(OH)2) = 6,66*10-6
β = (Кг/С)1/2 = 0,01
СН+ = β*С = 4*10-4моль/л
рН = -lgCH+ = 3,39 среда кислая
EpH+/H2=-0.059*pH= -0.2 B
EpO2/OH-=1,23+0.0147lg(pпарц(О2)) = 1,22 В
E0Zn2+/Zn = -0,763 B
E0Sn2+/Sn = -0,136 B
E0Sn2+/Sn > E0Zn2+/Zn - окисление цинка
E0Zn2+/Zn < EpH+/H2 идет водородная диполяризация
EpO2/OH- > E0Zn2+/Zn кислородная деполяризация протекает
A: Zn→ Zn2++2e
K: O2+4H++4e→2H2O
2H++2e→ H2
4.3 Способы защиты от коррозии
а) Катодное металлическое покрытие:
E(катодного покрытия) > E(компонентов сплава)
E0Zn2+/Zn = -0,763 B
E0Sn2+/Sn = -0,136 B
Для защиты можно использовать медь E0Сu2+/Cu = 0,521 B
При повреждении покрытия возникает коррозионный гальванический элемент
Анодный участок - Zn→Zn2+ + 2e
Катодный участок – процессы в зависимости от среды
Анодное металлическое покрытие
Е (анодного покрытия) < Е (компонентов сплава)
E0Zn2+/Zn = -0,763 B
E0Sn2+/Sn = -0,136 B
Для защиты можно использовать алюминий E0Al3+/Al = -1,662 B
При повреждении покрытия сплав – катод коррозионного элемента не корродирует:
Анодный участок Al → Al3+ + 3e
Катодный участок – процессы в зависимости от среды
б) протекторная защита
Е (протектора) < Е (защищаемого металла)
E0Zn2+/Zn = -0,763 B
E0Sn2+/Sn = -0,136 B
E0Mn2+/Mn = -1,180 B
А: Mn→Mn2+ + 2e - корродирует протектор
К: процессы в зависимости от среды
