ЭЛЕКТРОЛИЗ. Электролизом называется совокупность процессов, протекающих при прохождении постоянного электрического тока через систему
Электролизом называется совокупность процессов, протекающих при прохождении постоянного электрического тока через систему, состоящую из двух электродов и расплава или раствора электролита. Эти процессы складываются из направленного движения ионов в растворе или расплаве электролита и реакций восстановления и окисления, происходящих на электродах.
При электролизе, как и в гальваническом элементе на аноде происходит окисление, а на катоде - восстановление. Однако при этом катод подключён к отрицательному полюсу внешнего источника тока, анод – к положительному полюсу.
При электролизе расплава электролита на электродах подвергаются восстановлению и окислению только ионы, на которые диссоциирует этот электролит. Например, при электролизе расплава хлорида натрия на катоде протекает восстановление катионов натрия (Na+):
Na+ +ē → Na;
на аноде окисление анионов хлора:
2Cl- → Cl2 + 2ē
Суммарная реакция: 2NaCl → 2Na + Cl2
Электролиз водных растворов осложняется возможностью протекания на электродах нескольких процессов. В водных растворах, кроме ионов электролита, находятся также вода, ионы Н+ и ОН-. Все эти вещества могут подвергаться электрохимическим превращениям.
Последовательность катодных реакций
При электролизе растворов солей на катоде возможны следующие реакции:
1. восстановление ионов металла
Men+ + nē → Me;
2. восстановление ионов водорода в кислой среде
2Н+ + 2ē → Н2 ( 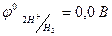 );
);
3. восстановление молекул воды
2Н2О + 2ē → Н2 + 2ОН- ( 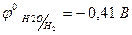 ).
).
Из возможных катодных процессов осуществляется тот, который характеризуется наибольшим значением электродного потенциала.
Из этого следует, что при электролизе растворов солей металлов, стоящих в ряду напряжения после водорода, например, медь, серебро, золото и другие, на электроде восстанавливаются только ионы металла и выделяется металл. В нейтральных и щелочных растворах с рН ≥ 7 возможно выделение и тех металлов, электродные потенциалы которых выше -0,41 В. (Объяснение следует дальше)
Из растворов, содержащих смесь таких катионов, происходит последовательное выделение металлов в порядке уменьшения величины их электродных потенциалов.
Если в растворе находятся ионы металлов, стоящие в ряду напряжения до алюминия включительно ( 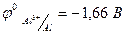 ), например, натрий, литий, кальций и другие, то на катоде восстанавливается только вода.
), например, натрий, литий, кальций и другие, то на катоде восстанавливается только вода.
Металлы, электродные потенциалы которых не сильно отличаются от водородного (находится в ряду напряжения металлов после алюминия), восстанавливаются на катоде одновременно с водой. При этом выделяется и металл, и водород. В зависимости от условий электролиза массовые соотношения металла и водорода могут быть различными, вплоть до выделения только одного металла или водорода.
Восстановление ионов металлов средней активности из растворов солей, становится возможным по двум причинам. Одна из них заключается в том, что растворы, подвергающиеся электролизу, имеют рН отличное от нуля, поэтому потенциал водородного электродного электрода становится величиной отрицательной, так, при рН = 7, 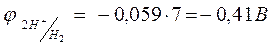 .
.
Реальные электрохимические реакции осложняются процессами диффузии ионов к поверхности электродов, адсорбции их, разрядки, десорбции и другими. Для их преодоления нужно приложить некоторое добавочное напряжение, которое получило название перенапряжения. Значительная величина перенапряжения процесса восстановления водорода, объясняет возможность восстановления на катоде достаточно активных металлов.
Последовательность анодных реакций
При электролизе растворов солей на аноде могут протекать реакции окисления:
1. анионов кислотных остатков: Ann- →An + nē
2. гидроксид - анионов
4ОН- - 4ē →2Н2О + О2 ( 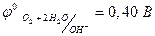 ).
).
3. молекул воды
2Н2О - 4ē → О2 + 4Н+ ( 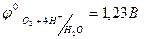 при рН = 7)
при рН = 7)
4. металла анода (растворимый анод)
Me →Men+ + nē
Из возможных анодных процессов осуществляется тот, который характеризуется наименьшим значением электродного потенциала.
Характер анодных процессов зависит от природы используемого анода. Различают инертные и растворимые аноды. Первые изготовлены из малоактивных металлов, например, из платины, а также используют графитовые, угольные электроды. Материалом растворимых анодов является металл с потенциалом меньшим, чем потенциалы конкурирующих процессов, например, медь, цинк и другие. При этом окислению подвергается материал анода. Так, при электролизе раствора сульфата меди (II) с медным анодом происходит растворение анода: Сu → Cu2+ + 2ē. Это объясняется тем, что потенциал меди ( 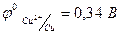 ) меньше потенциалов окисления воды и сульфат - иона. В процессе электролиза с использованием растворимого анода металла анода в виде ионов переходит в раствор, затем они могут восстанавливаться на катоде. На этом основаны методы очистки металлов от примесей (электрохимическое рафинирование металлов), методы нанесения покрытий и прочее.
) меньше потенциалов окисления воды и сульфат - иона. В процессе электролиза с использованием растворимого анода металла анода в виде ионов переходит в раствор, затем они могут восстанавливаться на катоде. На этом основаны методы очистки металлов от примесей (электрохимическое рафинирование металлов), методы нанесения покрытий и прочее.
На инертных анодах (графитовый, угольный, платиновый) могут окисляться молекулы воды, гидроксид – ионы или ионы кислотных остатков.
На аноде в растворах кислородосодержащих кислот или их солей разряжается вода. Это связано с тем, что электродные потенциалы анионов кислородосодержащих кислот имеют большие значения, чем потенциал окисления воды. Например, 2SO42- - 2ē → S2O82- (2,01 В). Аналогично ведут себя фторид-ионы ( 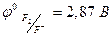 ).
).
Ионы Cl-, Br-, J-, S2- разряжаются из не очень сильно разбавленных растворов.
2Сl- → Cl2 + 2ē, 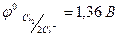 , 2Br- → Br2 - 2ē,
, 2Br- → Br2 - 2ē, 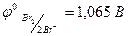
2J- → J2 - 2ē, 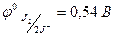 , S2- → S - 2ē,
, S2- → S - 2ē, 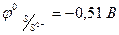
В связи с перенапряжением реакции выделения кислорода на аноде идёт окисление ионов хлора, хотя 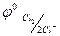 >
>  .
.
При электролизе растворов щелочей на аноде происходит окисление гидроксид-ионов, т.к. 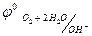 <
<  .
.
