Образование солей (реакция со щелочами)
Первичные и вторичные нитросоединения растворимы в щелочах с образованием солей. Т.е. проявляют свойства сопряженных С-Н кислот, что объясняется устойчивостью образующегося аниона:
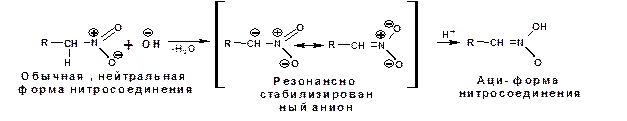
Если щелочной раствор нитросоединения обработать минеральной кислотой, то происходит образование аци-формы нитросоединения, которая изомеризуется в обычную форму. Поэтому нитросоединения относятся к псевдокислотам.
Реакция с карбонильными соединениями
Первичные и вторичные нитросоединения в присуствии щелочей нуклеофильно присоединяются по карбонильной группе альдегидов. При этом образуются нитроспирты:

Таким образом в нитрометане можно заместить три атома водорода с образованием три-(гидроксиметил)нитрометана О2N-С(СН2ОН)3.
Кислотность нитросоединений очень высокая. Поэтому в случае ароматических альдегидов гидроксипроизводное соединение выделить не удается. Реакция завершается на стадии ненасыщенного нитросоединения:
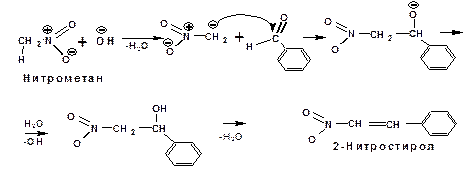
Реакция с азотистой кислотой
Первичные и вторичные нитросоединения реагируют с азотистой кислотой НNO2. В водном растворе азотистая кислота может распадаться следующим образом:
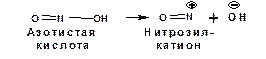
Образующийся ион гидроксила отщепляет протон от α-углеродного атома и образующийся анион присоединяется к атому азота нитрозил-катиона:

Из первичных нитросоединений образуются нитроловые кислоты. Вторичные нитросоединения образуют псевдонитролы.
Третичные нитросоединения не имеет атома водорода у α-углеродного атома. Поэтому не способны вступать реакции по типу альдольно-кротоновой конденсации.
Восстановление нитросоединений
Основной реакцией, характеризующей свойства нитросоединений, является реакция восстановления нитрогруппы до амино-группы. Реакция может протекать вкислой и щелочной средах. В качестве восстановителей могут быть использованы: железо или цинк в соляной кислоте, двухлористое олово в соляной кислоте, водород на катализаторах гидрирования, электрохимическое восстановление, сульфидом аммония. Классическая реакция Зинина – восстановления нитробензола осуществлена полисульфидом амммония (NH4)2Sn.
Механизм реакции восстановления нитробензола в кислой и нейтральной среде:
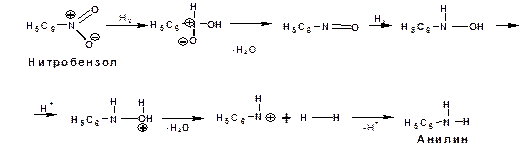
Механизм восстановления в щелочной среде:
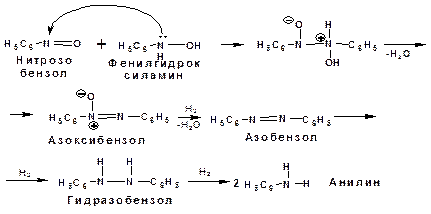
АМИНЫ
Производные аммиака, в которых атомы водорода замещены углеводородными группами, называются аминами.
