Многоядерные соединения. Гетероциклические соединения
Нуклеиновые кислоты.
1. Группа дифенила: получение, свойства, важнейшие природные.
2. Понятие о поворотной оптической изомерии.
3. Группа дифенилметана: получение, свойства, важнейшие природные.
4. Трифенилметан: получение, свойства.
5. Красители трифенилметанового ряда. Розанилины.
6. Красители трифенилметанового ряда. Аурины.
7. Группа дифенилэтана.
8. Гексафенилэтан. Понятие о свободных стабильных радикалах.
9. Нафталин и его свойства.
10. Способы получения нафталина.
11. Правила ориентации в нафталиновом ряду.
12. Антрацен. Особенности химических свойств.
13. Ализариновые красители.
14. Фенантрен. Особенности химических свойств.
15. Понятие о высших полициклических углеводородах. Канцерогены.
16. Ароматические углеводороды с конденсированными бензольными и пятичленными кольцами. Инден. Флуорен.
17. Небензоидные ароматические системы.
18. Пяти-членные гетероциклические системы с одним гетероатомом.
19. Фуран: получение, свойства.
20. Тиофен: получение, свойства.
21. Пиррол и его свойства.
22. Важнейшие производные пиррола.
23. Индол и его свойства.
24. Понятие о кубовых красителях.
25. Пиразол и его свойства.
26. Имидазол и тиазол.
27. Пиридин: получение, свойства.
28. Хинолин: получение, свойства.
29. Пиримидин: получение, свойства.
30. Важнейшие пиримидиновые основания.
31. Нуклеиновые кислоты: важнейшие составляющие.
32. Дезоксирибонуклеиновые кислоты: строение и биологическая роль в организме.
33. Рибонуклеиновые кислоты: строение и биологическая роль в организме.
Задачи
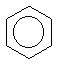 |
1. ® малахитовый зеленый.
 |
2. ® фенолфталеин.

3. ® конго красный.
4. Бензальдегид ® трифенилкарбинол.
5. Нафталин ® a– нафтол.
6. Нафталин ® b– нафтиламин.
7. Фталевый ангидрид ® антрахинон.
8. Нитрованием 2-метилнафталина было получено мононитросоединение, которое при окислении в жестких условиях дало 3 – нитробензол – 1,2,4 – трикарбоновую кислоту. Установить строение нитросоединения.
9. Антрацен легко реагирует с малеиновым ангидридом с образованием вещества С18Н12О3, которое при гидролизе дает дикарбоновую кислоту С18Н14О4. Какова наиболее вероятная структура полученных соединений?
10. Янтарный диальдегид ® фуран.
11. Фурфурол ® фурилакриловая кислота.
12. Пентоза ® фурфурол.
13. Заполнить схему превращения и назвать конечный продукт:
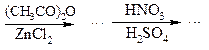 |
Тиофен
14. Расположите в порядке возрастания реакционной способности в условиях SE реакций: бензол, нафталин, тиофен, пиридин.
15. Следующие соединения расположите в порядке уменьшения основности:
а) пиридин;
б) пиперидины;
в) пиррол;
г) анилин;
д) аммиак;
е) метиламин.
Приведите объяснения.
16. Заполнить схемы превращений, назвать полученные соединения:
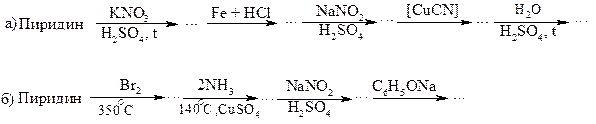 |
17. Глицерин ® хинолин.
18. Индол ® индиго синее.
19. Пиразол ® амидопирин.
20. Пиразол ® анальгин.
Гетероциклы не надо!!!!!!!!!!!!!!!!!!!
