Пример 2. Составьте тепловой баланс реактора синтеза этилового спирта, где протекает реакция
Составьте тепловой баланс реактора синтеза этилового спирта, где протекает реакция
СН2=СН2 +Н2О ↔С2Н5ОН + Qр (Qр=46090 кДж/кмоль),
Если исходный газ имеет состав: 40% Н2О и 60% С2Н4, скорость его подачи в реактор-гидрататор 2000м3/ч, температура на входе 614 К, конверсия за проход этилена 5%. Теплоемкость продуктов на входе и выходе одинакова и равна 27.1 кДж/кмоль. Побочные процессы и продукты не учитывать. Потери теплоты в окружающую среду принимаем 3% от прихода теплоты.
Решение.
Находим состав исходного газа:
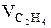 = 2000 · 0.6 = 1200 м3,
= 2000 · 0.6 = 1200 м3,
 = 2000 · 0.4 = 800 м3.
= 2000 · 0.4 = 800 м3.
Определяем состав газа на выходе из реактора:
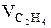 =1200 – 1200 · 0.05 = 1140 м3,
=1200 – 1200 · 0.05 = 1140 м3,
 = 800 – 1200 · 0.05 = 740 м3,
= 800 – 1200 · 0.05 = 740 м3,
 = 1200 · 0.05 = 60 м3.
= 1200 · 0.05 = 60 м3.
Находим суммарный объем газа (на выходе из реактора):
V = 1140 + 740 + 60 = 1940 м3.
Тепловой баланс:
Q1 + Q2 = Q3 + Q4
Рассчитываем приход теплоты. Физическая теплота газа:
Q1 = (2000/22.4) · 27.1 · 290 = 701396.5 кДж.
Теплота реакции:
Q2 = (2000/22.4) · 0.6 · 46090 · 0.05 = 123460 кДж
Всего: ΣQприх = 825156.5 кДж.
Определяем расход теплоты. Теплота, уносимая отходящими газами:
Q3 = (1940/22.4) · 27.1 · 341 = 800345.4 кДж
Q4 = 825156.5 · 0.03 = 24754.7 кДж
Всего: ΣQрасх= 825100.1 кДж
