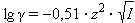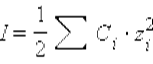Атомно-эмиссионный анализ. Атомно-адсорбционный анализ. Молекулярно-адсорбционный анализ. Основы данных методов, примеры, применение.
Атомно-эмиссионная спектроскопия (спектрометрия), АЭС или атомно-эмиссионный спектральный анализ — совокупность методов элементного анализа, основанных на изучении спектров испускания свободных атомов и ионов в газовой фазе. Обычно эмиссионные спектрырегистрируют в наиболее удобной оптической области длин волн от ~200 до ~1000 нм. АЭС — способ определения элементного состава вещества по оптическим линейчатым спектрам излучения атомов и ионов анализируемой пробы, возбуждаемым в источниках света. В качестве источников света для атомно-эмиссионного анализа используют пламя горелки или различные виды плазмы, включая плазму электрической искры или дуги, плазму лазерной искры, индуктивно-связанную плазму, тлеющий разряд и др.
АЭС — самый распространённый экспрессный высокочувствительный метод идентификации и количественного определения элементов примесей в газообразных, жидких и твердых веществах, в том числе и в высокочистых. Он широко применяется в различных областях науки и техники для контроля промышленного производства, поисках и переработке полезных ископаемых, в биологических, медицинских и экологических исследованиях и т.д. Важным достоинством АЭС по сравнению с другими оптическими спектральными, а также многими химическими и физико-химическими методами анализа, являются возможности бесконтактного, экспрессного, одновременного количественного определения большого числа элементов в широком интервале концентраций с приемлемой точностью при использовании малой массы пробы.
Процесс атомно-эмиссионного спектрального анализа состоит из следующих основных звеньев:
Пробоподготовка (подготовка образца)
Испарение анализируемой пробы (если она не газообразная);
Диссоциация — атомизация её молекул;
Возбуждение излучения атомов и ионов элементов пробы;
Разложение возбужденного излучения в спектр;
Регистрация спектра;
Идентификация спектральных линий — с целью установления элементного состава пробы (качественный анализ);
Измерение интенсивности аналитических линий элементов пробы, подлежащих количественному определению;
Нахождение количественного содержания элементов с помощью установленных предварительно градуировочных зависимостей.
Атомно-абсорбционная спектрометрия (ААС) — распространенный в аналитической химии инструментальный метод количественного элементного анализа(современные методики атомно-абсорбционного определения позволяют определить содержание почти 70 элементов Периодической системы ) по атомнымспектрам поглощения (абсорбции) для определения содержания металлов в растворах их солей: в природных и сточных водах, в растворах-минерализатах, технологических и прочих растворах[1][2][3].
Прибором для ААС служит атомно-абсорбционный спектрометр , основными элементами которого являются источник света, атомизатор, спектральный прибор и электронная система. Определение содержания элемента в пробе проводят с использованием экспериментально установленной функциональной зависимости между аналитическим сигналом и концентрацией элемента в градуировочном растворе .
Молекулярно-абсорбционный спектральный анализ включает в себя спектрофотометрический и фотоколориметрический виды анализа.
Спектрофотометрический анализ основан на определении спектра поглощения или измерении светопоглощения при строго определенной длине волны, которая соответствует максимуму кривой поглощения исследуемого вещества.
Фотоколориметрический анализ базируется на сравнении интенсивности окрасок исследуемого окрашенного и стандартного окрашенного растворов определенной концентрации.
37.Хроматография. Принципы метода, их классификация. Хроматограмма и методы её обработки. Высокоэффективная жидкостная хроматография. Ионная хроматография.Хроматография: сущность, классификация, основные характеристики элюентной колоночной хроматографии .Хроматография - это метод разделения и анализа смесей веществ, основанный на различном распределении компонентов смеси между двумя несмешивающимися фазами - одна из которых должна быть подвижной, а другая неподвижной (ПФ, НФ). Устанавливается динамическое равновесие, вследствие чего молекулы разделяемой смеси часть времени находятся в НФ, а часть - в ПФ. Для разделения разных молекул НФ должна обладать хотя бы одним из их основных свойств: 1) физически сорбировать вещества, находящиеся в ПФ; 2) химически сорбировать вещества, находящиеся в ПФ; 3) растворять разделяемые вещества; 4) иметь пористую структуру и поэтому удерживать одни вещества и не задерживать другие, в зависимости от их размеров или формы.
Хроматографический метод является универсальным для разделения и анализа смесей веществ самой различной природы. В зависимости от конкретных задач он видоизменялся, вследствие чего возникло много вариантов метода В настоящее время хроматографические методы классифицируют по следующим признакам: 1) агрегатному состоянию ПФ и НФ; 2) механизму взаимодействия веществ, анализируемой смеси и сорбента; 3) природе явлений, лежащих в процессе разделения; 4) способу оформления метода; 5) методу проведения анализа.
По агрегатному состоянию ПФ может быть жидкой (жидкостная хроматография) или газообразной (газовая хроматография).
НФ может быть твердым телом или жидкостью, нанесенной на материал-носитель. В соответствии с этим в жидкостной хроматографии различают жидкость-жидкостную хроматографию (НФ и ПФ - жидкие) и жидкотвердофазную (ПФ - жидкая, а НФ - твердая), а в газовой хроматографии газотвердофазную (ПФ-газ, НФ-твердая) и газожидкостную (ПФ-газ, НФ-жидкость). Высокоэффективная жидкостная хроматография — один из эффективных методов разделения сложных смесей веществ. Основой хроматографического разделения является участие компонентов разделяемой смеси в сложной системе Ван-дер-Ваальсовых взаимодействий (преимущественно межмолекулярных) на границе раздела фаз. Ионная хроматография. В ионообменной хроматографии разделение компонентов смеси достигается за счет обратимого взаимодействия ионизирующихся веществ с ионными группами сорбента. Сохранение электронейтральности сорбента обеспечивается наличием способных к ионному обмену противоионов, расположенных в непосредственной близости к поверхности. Ион введенного образца, взаимодействуя с фиксированным зарядом сорбента, обменивается с противоионом. вещества, имеющие разное сродство к фиксированным зарядам, разделяются на анионитах или на катеонитах.
38.Термодинамическая система. Классификация термодинамических систем. Параметры и функции состояния. Равновесные, стационарные и переходные состояния. Термодинамические процессы Термодинамическая система — выделяемая (реально или мысленно) для изучения макроскопическая физическая система, состоящая из большого числа частиц и не требующая для своего описания привлечения микроскопических характеристик отдельных частиц[1], «часть Вселенной, которую мы выделяем для исследования»[2]. Единицей измерения числа частиц в термодинамической системе обычно служит число Авогадро[3] (примерно 6·1023 частиц на моль вещества), дающее представление, о величинах какого порядка идёт речь.Классификация: По характеру взаимодействия с окружающей средой различают системы[8]:изолированные, не обменивающиеся с внешней средой ни энергией, ни веществом;адиабатически изолированные, не обменивающиеся с внешней средой веществом, но допускающие обмен энергией в виде работы[17];закрытые, обменивающиеся с внешней средой энергией, но не обменивающиеся веществом;открытые, обменивающиеся с внешней средой и энергией, и веществом;
частично открытые, обменивающиеся с внешней средой и энергией, и веществом, но у которых не все составляющие вещества принимают участие в материальном обмене (например, из-за наличия полупроницаемых перегородок).Параметры состояния –экстенсивные,и интенсивные. Термодинамические процессы разделяются на равновесные и неравновесные. Равновесные это такие процессы, при которых система переходит последовательно из одного состояния равновесия в другое. Термодинамическое равновесие — состояние системы, при котором остаются неизменными по времени макроскопические величины этой системы (температура, давление, объём, энтропия) в условиях изолированности от окружающей среды. В состоянии равновесия в системе отсутствуют потоки материи или энергии, неравновесные потенциалы (или движущие силы), изменения количества присутствующих фаз. Отличают тепловое, механическое, радиационное (лучистое) и химическое равновесия. На практике условие изолированности означает, что процессы установления равновесия протекают гораздо быстрее, чем происходят изменения на границах системы (то есть изменения внешних по отношению к системе условий), и осуществляется обмен системы с окружением веществом и энергией. Иными словами, термодинамическое равновесие достигается, если скорость релаксационных процессов достаточно велика (как правило, это характерно для высокотемпературных процессов) либо велико время для достижения равновесия (этот случай имеет место в геологических процессах).
Третье начало термодинамики может быть сформулировано так:Приращение энтропии при абсолютном нуле температуры стремится к конечному пределу, не зависящему от того, в каком равновесном состоянии находится система». Третье начало термодинамики относится только к равновесным состояниям.Поскольку на основе второго начала термодинамики энтропию можно определить только с точностью до произвольной аддитивной постоянной (то есть, определяется не сама энтропия, а только её изменение): Третье начало термодинамики позволяет находить абсолютное значение энтропии, что нельзя сделать в рамках классической термодинамики (на основе первого и второго начал термодинамики). В классической термодинамике энтропия может быть определена лишь с точностью до произвольной аддитивной постоянной , что не мешает термодинамическим исследованиям, так как реально измеряется разность энтропий в различных состояниях. Согласно третьему началу термодинамики, при значение . Энтропию, как и другие термодинамические функции, принято относить к стандартному состоянию вещества. Абсолютную величину энтропии в стандартном состоянии принято обозначать 5°2Э8-Использование 5°2Э8 значительно упрощает расчеты химического. Энтропия состоит из двух слагаемых энтропии смешения WjN катионов при температуре Т и давлении Р и энтропии стандартного состояния So, которая, в свою очередь, складывается из энтропии отдельных катионов в чистом состоянии.
39.Работа и теплота. Первое начало термодинамики для различных процессов в системе идеального газа. Закон Гесса и следствия из него.Первое начало термодинамики— это обобщение закона сохранения энергии с учётом тепловых процессов. Его формулировка: количество теплоты, сообщённое системе, расходуется на выполнение работы против внешних сил и изменение её внутренней энергии: dQ=dA+dU.Первому началу термодинамики можно дать другую формулировку, если учесть, что dA=dQ-dU, т.е. dAdQ. Применим первое начало термодинамики к различным изопроцессам.
1. Изохорный процесс (V=const). В этом процессе объём системы остаётся постоянным, поэтомуdA=PdV=0 и dQ=dU.В изохорном процессе теплота, подведенная к системе, полностью расходуется на изменение её внутренней энергии.2. Изобарный процесс (Р=сonst). Так как объём изменяется, то при подведении теплоты к системе она частично превращается в работу и поэтому первое начало термодинамики имеет вид:dQ=dA+dU. 3.Изотермический процесс (T=const). При постоянной температуре изменения внутренней энергии идеального газа не происходит: dU=0, поэтомуdQ=dA.В изотермическом процессе вся теплота, подведенная к газу, расходуется на совершение работы. Закон Гесса — основной закон термохимии, который формулируется следующим образом.Тепловой эффект химической реакции, проводимой в изобарно-изотермических или изохорно-изотермических условиях, зависит только от вида и состояния исходных веществ и продуктов реакции и не зависит от пути её протекания.Иными словами, количество теплоты, выделяющееся или поглощающееся при каком-либо процессе, всегда одно и то же, независимо от того, протекает ли данное химическое превращение в одну или в несколько стадий (при условии, что температура, давление и агрегатные состояния веществ одинаковы). Например, окисление глюкозы в организме осуществляется по очень сложному многостадийному механизму, однако суммарный тепловой эффект всех стадий данного процесса равен теплоте сгорания глюкозы.
40.Возможность рассчитать величину "свободной" энергии, т.е. той части внутренней энергии системы, которую можно превратить в работу, дает тепловая теорема Нернста, называемая также третьим началом термодинамики.
Основные положения тепловой теоремы заключаются в следующем:
1. При абсолютном нуле температуры свободная энергия X равна теплоте процесса.
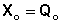
2. При температурах, близких к абсолютному нулю, теплоемкость системы равна нулю.
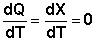
Одной из формулировок третьего начала термодинамики является также постулатПланка:
Энтропия идеального кристалла при абсолютном нуле температуры равна нулю.
Строго говоря, тепловая теорема Нернста и постулат Планка являются следствиями из второго начала термодинамики; но независимо от этого они имеют очень большое значение, позволяя рассчитывать абсолютную энтропию системы и, следовательно, величину свободной энергии системы.
Расчет абсолютной энтропии
Рассчитаем изменение энтропии некоторой системы при нагревании её от абсолютного нуля до температуры T при постоянном давлении. Из первого и второго начал термодинамики имеем:
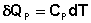
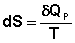
Отсюда:
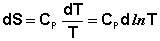
Учитывая, что ST=0 = 0, получим:
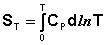
При T = 0 любое вещество может находиться только в твердом состоянии. При нагревании вещества возможен его переход в жидкое и затем в газообразное состояние; для фазовых переходов, происходящих в изобарно-изотермических условиях, изменение энтропии равно приведенной теплоте фазового перехода:
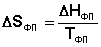
Таким образом, нагревание вещества без фазовых переходов сопровождается непрерывным ростом энтропии; при фазовом переходе происходит скачкообразное изменение энтропии. Графическая зависимость энтропии вещества от температуры приведена на рисунке 1.3.
Учитывая это, рассчитать абсолютную энтропию любого вещества при любой температуре можно следующим образом:
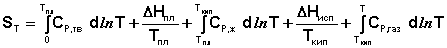
Поскольку энтропия есть функция состояния, изменение энтропии в ходе химического процесса определяется только видом и состоянием исходных веществ и продуктов реакции и не зависит от пути реакции; оно может быть рассчитано по уравнению (I.67):
 Для многих веществ величины абсолютной энтропии в стандартных условиях пРиведены в справочной литературе.
Для многих веществ величины абсолютной энтропии в стандартных условиях пРиведены в справочной литературе.
41.При протекании химической реакции через некоторое время устанавливается химическое равновесие. Существует два признака химического равновесия: кинетический, термодинамический. В кинетическом – ?пр = ?обр, в термодинамическом – характеризует химическую реакцию при условиях P, t – const (?G = 0); при условиях V, Т – const (?F = 0).
Химический потенциал – функция, которая характеризует состояние i-го компонента при определенных внешних условиях.где n1 – число молей i-го компонента.
Если к бесконечно большому количеству раствора прибавить определенное количество какого-нибудь компонента, то химический потенциал системы определяется изменением изобарного потенциала при изобарных условиях или изменением изохорного потенциала при изохорных условиях.
Химический потенциал зависит от концентрации данного компонента?i = ?0 + RTLnPi– (для идеального газа),
где Рi– парциальное давление – вклад каждого компонента в общее давление или давление, которое компонент имел бы, если бы находился в смеси.Парциальное давление – элементарная функция (можно складывать). Пример (O2, N2, H2) – их общее давление
?i= ?0+ RTLnCi – (для раствора),?0– значение химического потенциала при стандартных условиях.Химический потенциал характеризует способность данного компонента выходить из данной фазы путем испарения, растворения, кристаллизации и т. д. Переход этот происходит произвольно.В результате химического равновесия скорость прямой реакции уменьшается, а скорость обратной реакции увеличивается.Концентрации, которые соответствуют химическому равновесию, называются равновесными концентрациями. Связь между равновесными концентрациями устанавливается законом действующих масс (ЗДМ). Этот закон в 1867 г. вывели К. М. Гульберг и П. Вааге.
Принцип Ле Шателье — Брауна (1884 г.) — если на систему, находящуюся в устойчивом равновесии, воздействовать извне, изменяя какое-либо из условий равновесия (температура, давление, концентрация, внешнее электромагнитное поле), то в системе усиливаются процессы, направленные на компенсацию внешнего воздействия.Анри Ле Шателье (Франция) сформулировал этот термодинамический принцип подвижного равновесия, позже обобщённый Карлом Брауном[1].
Принцип применим к равновесию любой природы: механическому, тепловому, химическому, электрическому (эффект Ленца, явление Пельтье)[2].
Если внешние условия изменяются, это приводит к изменению равновесных концентраций веществ.В этом случае говорят о нарушении или смещении химического равновесия.
Химическое равновесие смещается в ту или иную сторону при изменении любого из следующих параметров:
1) температуры системы, т. е. при её нагревании или охлаждении
2) давления в системе, т. е. при её сжатии или расширении
3) концентрации одного из участников обратимой реакции
42. Растворы – термодинамически устойчивые системы переменного состава, состоят не менее чем из двух компонентов и продуктов их взаимодействия. Это дисперсные системы, состоящие из дисперсной фазы и дисперсионной среды. уществуют жидкие, газовые и твердые растворы. Растворы отличаются от химических соединений тем, что их состав может изменяться непрерывно. Как и любая химически равновесная в данных условиях система, растворы должны обладать минимумом свободной энергии Гиббса. По своему агрегатному состоянию дисперсные системы могут быть: газообразными, жидкими, твердыми; по степени дисперсности – взвесями, коллоидными и истинными растворами. В истинном растворе распределенное в среде вещество диспергировано до атомного или молекулярного уровня. Примеры многочисленны: газообразный раствор – воздух, состоящий из главного компонента азота – 78% N2; сплавы, представляющие собой твердые растворы, например, медные Cu – Zn, Cu – Cd, Cu – Ni и др.
Коллоидные растворы – микрогетерогенные системы, занимают промежуточное положение между истинными растворами и взвесями. Растворы состоят из растворенного вещества и растворителя. Растворителем считают тот компонент, который преобладает в растворе. Свойства растворов зависят от концентрации. Рассмотрим способы выражения концентрации растворов. Рассмотрим модель идеального раствора. Раствор называется идеальным, если в нем отсутствует взаимодействие между частицами (молекулами, атомами, ионами). Растворы неэлектролитов – частицы, плохо растворимые в воде, так как нет носителя электрического заряда. Закон Рауля справедлив только для разбавленных растворов неэлектролитов.
Пусть PBO – давление пара над чистым растворителем, при постоянной температуре T1; PB – давление пара растворителя при этой же температуре, но над раствором, состоящим из нелетучего компонента А (сахар), и чистым жидким растворителем В:
PB = f (T).
Разность PBO – PB равна понижению давления пара.
Величина (PBO – PB) /PBO – относительное понижение упругости пара = XA = ?P/PBO, где XA – мольная доля, PBO > PB, ?P = PBO – PB – абсолютное понижение упругости пара.
Закон Рауля. Относительное понижение упругости пара растворителя над раствором равно мольной доле растворенного нелетучего компонента.
барометрическая формула Больцмана.
Следствия из закона Рауля:
1. Растворение нелетучего компонента в растворителе приводит к расширению температурной области существования жидкой фазы.
2. Понижение температуры замерзания и повышение температуры кипения прямо пропорциональны моляльной концентрации растворенного вещества.
3. Растворы, содержащие одинаковое число молей растворенных веществ в одинаковых молях растворителя, обнаруживают одно и то же понижение температуры замерзания и одно и то же повышение температуры кипения.
tкип=Э x Смоляльн,
где Э – эбуллиоскопическая константа, +0,52.
tзам=К x Смоляльн,
где К – криоскопическая константа, равная –1,86.
Эбуллиоскопическая константа – разница между температурой кипения раствора и температурой чистого растворителя.
Криоскопическая константа – разница между температурой замерзания раствора и температурой чистого растворителя.
Для решения задач об этих константах необходимо знать массу растворенного вещества и массу раствора. Например, масса хлороформа (трихлорметан CHCl3) рассчитывается по формуле:где m1 – масса растворенного вещества;
m2 – масса растворителя;t – величина, показывающая на сколько градусов понизилась температура;К – криоскопическая константа.
43.Р-ры сильных электролитов.ионная сила раствора.теория дебая-хюккеля и её приближени. Равновесие диссоциации сильных электролитов полностью смещено вправо,поэтому константа равновесия оказывается величиной неопределенной. ↓электропроводности при ↑концентрации сильного электролита обусловлено электростатическим взаимодействием ионов.Дебай и Хюккель, предложив модель, кот.легла в основу теории сильных электролитов, постулировали:1)Электролит полностью диссоциирует, но в сравнительно разбавленных р-ах (C = 0,01 моль·л–1).2)Каждый ион окружен оболочкой из ионов противоположн.знака,каждый из этих ионов сольватирован(ионная атмосфера).Очевидно, что при электростатическом взаимодействии ионов противоположных знаков необходимо учитывать влияние ионной атмосферы. При движении катиона в электростатическом поле ионная атмосфера деформируется; она сгущается перед ним и разрежается позади него.Эта асимметрия ионной атмосферы оказывает тем более тормозящее действие движению катиона, чем выше концентрация электролитов и чем больше заряд ионов. Коэффициент активности по Дебаю–Хюккелю зависит по крайней мере от t, диэлектрической проницаемости растворителя (ε) и ионной силы (I); последняя служит мерой интенсивности электрического поля, создаваемого ионами в р-ре.
Для данного электролита ионная сила выражается уравнением Дебая–Хюккеля:
|
Ионная сила в свою очередь равна
|
Здесь C – аналитическая концентрация, z – заряд катиона или аниона. Для одно-однозарядного электролита ионная сила совпадает с концентрацией.
44.Проводники второго рода.Скорость движения ионов и подвижность ионов.Электрохимическая проводимость и эквивалентная электропроводность.Предельнаяэквивалентная электропроводимость. Проводник второго рода — проводник с ионной электропроводностью.Проводниками 2-го рода(электролитами)являются р-ры солей,кислот,щелочей и др,т е. в-ва с ионным строением молекул.Прохождение эл.тока через электролиты связано с явлением электролиза.При этом электрические заряды переносятся вместе с ионами. Абсолютная скорость движения ионов. В растворах электролитов сольватированные ионы находятся в беспорядочном движении. При наложении электрического поля возникает упорядоченное движение ионов к противоположно заряженным электродам.Сравнение скоростей движения различных видов ионов производят при градиенте потенциала поля 1 В/м. Для этих условий скорость движения ионов называют абсолютной, обозначают буквой w и выражают в м2×B–1×c–1. Абсолютная скорость движения иона –– это расстояние в метрах, которое проходит ион за 1 с при градиенте потенциала 1В/м. Численные значения абсолютных скоростей движения ионов в данном растворителе зависят только от их природы и температуры.Электропроводность р-ра электролита обеспечивается за счет потоков миграции ионов,присутствующих в р-ре.Как и для обычных проводников,сопротивление р-ров рассчитывается по формуле:где ρ–удельное сопротивление,l-расстояние между электродами,S–площадь электродов.Величина 1/ρ = χ называется удельной электропроводностью.Удельная электропроводность хар-зует электропроводность объема р-ра,заключенного между двумя параллельными электродами,имеющими площадь 1 м2 (или 1 см2)и расположенными на расстоянии 1 м (или 1 см) друг от друга.При С → 0 величина χ стремится к удельной электропроводности чистой воды.С ростом концентрации электролита χ сначала возрастает в связи с увеличением числа ионов в р-ре,однако с ростом концентрации начинает проявляться ион-ионное взаимодействие,приводящее к замедлению движения ионов,а также к их ассоциации.Поэтому почти всегда зависимость удельной электропроводности от концентрации электролита проходит через максим.Чтобы выделить эффект ион–ионного взаимодействия удельную электропроводность χ делят на Z+ν+C, где С – число молей в единице объема.
45 Зависимость электрической проводимости от различных факторов. Электропроводность неводных растворов
предельная электропроводность зависит от
– концентрации электролита;
– вязкости и диэлектрической проницаемости растворителя;
– температуры;
– скорости движения ионов, которая определяется величиной заряда иона и его радиуса с учетом гидратации.При увеличении концентрации электролита удельная электропроводность сначала увеличивается, а затем уменьшается Такая зависимость характерна как для сильных, так и для слабых электролитов. В случае слабых электролитов падение удельной электропроводности в области высоких концентраций объясняют уменьшением степени диссоциации, а сильных – электростатическим взаимодействием между ионами в растворе.Электропроводность неводных растворов обычно значительно меньше электропроводности водных. Исключение составляют аммиачные растворы, а также растворы в HCN, где электропроводность гораздо выше, чем в водных. Обычноэлектропроводность неводных растворов не так высока, как электропроводность водных растворов. Зависимостьэлектропроводности неводных растворов электролитов от концентрации носит сложный характер и не всегда возрастает с увеличением разбавления, как это отмечается для водных растворов, а в пределах некоторых концентраций даже убывает. Аномалии в электропроводности неводных растворов объясняются особенностями взаимодействия растворяемого вещества с растворителем.Экспериментальные измерения электропроводности неводных растворов электролитов убедительно подтверждают изложенное.Усанович доказал, что электропроводность неводных растворов возникает в результате кислотно-основного взаимодей-ствия между их компонентами. Прийдя, таким образом, к несогласию с господствовавшей в то время протонной теорией Брен-стеда, он выдвигает новую теорию кислот и оснований. Теоретические вопросы концентрационной зависимости электропроводности неводных растворов менее изучены, чем для водных. Принципиальное отличие в данном случае заключается в том, что природа носителей тока в неводных растворах в настоящее время остается еще во многом предположительной. В то время как большинство солей в водных растворах - сильные электролиты, в неводных растворах большая часть электролита присутствует в незаряженной форме, а ионы могут существовать в различных формах - одиночные ионы различной степени сольватации и различные ионные ассоциаты: тройники и более высокополимерные образования. Образование ионов в неводных растворах электролитов предопределяет, как и в водных, наличие электропроводности. Проводимость неводных растворов определяется концентрацией ионов и скоростью их движения, однако здесь сильно проявляются специфические свойства растворителя. Поскольку степень диссоциации в неводных растворителях, как правило, невелика, электропроводность неводных растворов значительно меньше электропроводности водных. Исключение составляют аммиачные растворы, а также растворы в HCN, где электропроводность гораздо выше, чем в подных.Зависимость эквивалентной электропроводности от квадратного корня из концентрации раствора электролита. Электропроводностью обладают не только водные, но и неводные растворы. Проводимость неводных растворов также определяется концентрацией ионов и скоростью движения. Электропроводность неводных растворов электролитов зависит от вязкости и диэлектрической проницаемости среды.Зависимость эквивалентной электропроводности от квадратного корпя из концентрации раствора электролита. Электропроводностью обладают не только водные, по и неводные растворы. Проводимость неводных растворов также определяется концентрацией ионов и скоростью движения. Электропроводность неводных растворов электролитов зависит от вязкости и диэлектрической проницаемости среды.