Глава 1. Строение атома углерода. Гибридизация
Введение.
К настоящему времени известно чуть более 120 элементов, часть из них получены искусственным путем и в природе не встречаются. Общее число химических соединений этих элементов около 25 тысяч. Есть только один элемент в периодической системе Д.И. Менделеева, количество соединений которого исчисляется десятками миллионов – это углерод. Атомы углерода обладают практически уникальной способностью образовывать устойчивые связи между собой с образованием цепочек, циклов и каркасных структур практически любой протяженности*. На основе соединений углерода базируется и «особый вид существования белковых тел» - жизнь. Изначально, когда соединения углерода выделяли исключительно из продуктов животного или растительного происхождения - эти соединения стали называть органическими.
 | Позднее, когда химики смогли получать многие из этих соединений без привлечения живой материи, название все равно сохранилось. Таким образом, за дисциплиной изучающей соединения углерода прочно закрепилось название «Органическая химия» в противовес «Неорганической химии», в чьем ведении осталась химические свойства всех остальных элементов. Органическая химия изучает не только огромное количество соединений, но и значительное количество разнообразных превращений органических веществ. Ориентировочно представить объем базовой информации, можно рассмотрев объем информации, собранный в наиболее полном справочнике – 12-ти томах «Общей органической химии»1. |
| Фридрих Веллер** |
Естественно, даже малую часть фактического материала известного на данный момент «утрамбовать» в небольшой спецкурс невозможно. Однако есть общие закономерности в свойствах основных классов органических соединений и направлениях протекания органических реакций. Именно общим свойствам, присущим целым классам органических соединений, и основным механизмам протекания органических реакций посвящен курс «Теоретические основы органической химии».
*Таким свойством в очень ограниченной степени обладает сера, она образует стабильные циклические молекулы S8 черенковой серы и метастабильные полимерные цепочки Sn пластической серы. Атомы кремния также способны образовывать связи Si-Si, однако, соединения, содержащие подобные связи весьма не устойчивы и легко подвергаются гидролизу или окислению. В отличие от углерода, кремний и имеет высокое сродство к кислороду, и большинство поликремниевых соединений содержат связь Si-O-Si.
**Фридрих Веллер в 1828 году осуществил первый в истории органический синтез. При нагревании цианата аммония он получил мочевину (карбамид) и в дальнейшем показал ее полную идентичность с природной.
Глава 1. Строение атома углерода. Гибридизация.

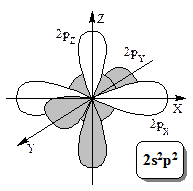 Простейшая органическая молекула – первый представитель класса алканов – метан. Из структурных исследований известно что молекула СН4 имеет строение правильного тетраэдра с атомом углерода в центре и атомами водорода в вершинах. Как известно, геометрия молекул определяется пространственным расположением электронных облаков соответствующих атомов образующих молекулу, как участвующих в образовании связей так и не участвующих. Однако для атома углерода сразу возникает противоречие. Электронное строение внешнего уровня атома углерода 2s2p2. При этом на s подуровне находится электронная пара, а на двух р-орбиталях по одному неспаренному электрону. Из этого строения вытекает двухвалентность атома углерода, что практически никогда не реализуется в действительности. Углерод практически всегда четырехвалентен, как в метане. Редким исключением является угарный газ СО, в котором углерод действительно двухвалентен.
Простейшая органическая молекула – первый представитель класса алканов – метан. Из структурных исследований известно что молекула СН4 имеет строение правильного тетраэдра с атомом углерода в центре и атомами водорода в вершинах. Как известно, геометрия молекул определяется пространственным расположением электронных облаков соответствующих атомов образующих молекулу, как участвующих в образовании связей так и не участвующих. Однако для атома углерода сразу возникает противоречие. Электронное строение внешнего уровня атома углерода 2s2p2. При этом на s подуровне находится электронная пара, а на двух р-орбиталях по одному неспаренному электрону. Из этого строения вытекает двухвалентность атома углерода, что практически никогда не реализуется в действительности. Углерод практически всегда четырехвалентен, как в метане. Редким исключением является угарный газ СО, в котором углерод действительно двухвалентен.
Современное объяснение четырехвалентности углерода основано на модели гибридизации атомных орбиталей. Предлагается, что четыре валентных электрона атома углерода располагаются на четырех вырожденных гибридных орбиталях (т.н. sp3-орбиталях). Эти орбитали направлены к вершинам правильного тетраэдра. Угол между орбиталями 109,5˚, что соответствует максимальному удалению их друг от друга. В отличие от р-орбиталей, гибридные sp-орбитали не симметричны относительно узла и плотность вероятности нахождения электрона в большей доле значительно выше. Химическая связь при наличии данного типа гибридизации осуществляется за счет фронтального перекрывания sp3-орбитали (σ-связь). Такую гибридизацию имеют атомы углерода в наиболее твердой аллотропической модификации углерода – алмазе.
sp3-Гибридизация объясняет тетраэдрическую конфигурацию атома углерода в насыщенных органических соединениях (содержащих одинарные, или «простые» связи С-С). Однако атомы углерода способны образовывать кратные связи (двойные и тройные) между собой и с атомами других элементов. Геометрия молекул содержащих кратные связи существенно отличается от тетраэдра. Углы при атоме углерода при двойной связи составляют 120◦, а при тройной 180◦. Для объяснения этого в концепции гибридизации постулируется возможность участия в образовании 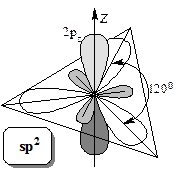 гибридных орбиталей не всех атомных р-орбиталей. В молекулах содержащих двойную связь в гибридизации участвует только две из трех р-орбиталей с образованием трех гибридных sp2-орбиталей лежащих в одной плоскости. Негибридизованная рz-орбиталь располагается перпендикулярно этой плоскости. При этом одна из кратных связей образуется за счет фронтального перекрывания гибридных орбиталей (σ-связь), а вторая – за счет бокового перекрывания негибридизованных р-орбиталей (π-связь).
гибридных орбиталей не всех атомных р-орбиталей. В молекулах содержащих двойную связь в гибридизации участвует только две из трех р-орбиталей с образованием трех гибридных sp2-орбиталей лежащих в одной плоскости. Негибридизованная рz-орбиталь располагается перпендикулярно этой плоскости. При этом одна из кратных связей образуется за счет фронтального перекрывания гибридных орбиталей (σ-связь), а вторая – за счет бокового перекрывания негибридизованных р-орбиталей (π-связь).  Гибридизацию sp2 имеют атомы углерода в самой распространенной аллотропической модификации углерода – графите, и открытых в конце 20-го века фуллеренах (молекулярная форма углерода).
Гибридизацию sp2 имеют атомы углерода в самой распространенной аллотропической модификации углерода – графите, и открытых в конце 20-го века фуллеренах (молекулярная форма углерода).
При образовании тройной связи две из трех связей образуются за счет бокового перекрывания взаимно перпендикулярных негибридизованных р-орбиталей (π-связи), а одна – за счет фронтального перекрывания одной из противоположно направленных sp-гибридных орбиталей (σ-связь).
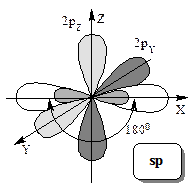 Увеличение кратности связи С-С приводит к уменьшению длины и увеличению прочности углерод-углеродной связи – (1,54Ǻ, 369 кДж) простая связь, (1,34Ǻ, 605 кДж) двойная связь и (1,20Ǻ, 814 кДж) тройная связь. Кроме того меняются другие физические характеристики связей, так барьер вращения вокруг двойной С=С связи значительно выше, чем вокруг одинарной, за счет наличия не осевой π-связи (вращение вокруг связи С=С возможно только за счет обратимого разрыва π-связи). Вращение вокруг тройной связи наблюдать не возможно по причине линейности ее строения. Углерод в состоянии sp-гибридизации присутствует в аллотропической модификации – карбине. Карбин представляет собой длинные молекулярные цепочки атомов углерода с чередованием одинарных и тройных связей.
Увеличение кратности связи С-С приводит к уменьшению длины и увеличению прочности углерод-углеродной связи – (1,54Ǻ, 369 кДж) простая связь, (1,34Ǻ, 605 кДж) двойная связь и (1,20Ǻ, 814 кДж) тройная связь. Кроме того меняются другие физические характеристики связей, так барьер вращения вокруг двойной С=С связи значительно выше, чем вокруг одинарной, за счет наличия не осевой π-связи (вращение вокруг связи С=С возможно только за счет обратимого разрыва π-связи). Вращение вокруг тройной связи наблюдать не возможно по причине линейности ее строения. Углерод в состоянии sp-гибридизации присутствует в аллотропической модификации – карбине. Карбин представляет собой длинные молекулярные цепочки атомов углерода с чередованием одинарных и тройных связей.
