Електропровідність розчинів електролітів
Електропровідність характеризує здатність середовища проводити електричний струм. Вона є оберненою електричному опору і вимірюється в сіменсах (См = Ом -1). Електропровідність розчину електроліту зумовлена міграцією наявних у даному розчині іонів. Її величина визначається як кількістю іонів, так і швидкістю їх руху в електричному полі.
Зазвичай електропровідність розчинів визначають вимірюванням опору електрохімічної комірки, що містить два платиновані платинові електроди і досліджуваний розчин. Для запобігання електролізу, який призводить до зміни концентрації розчину та поляризації електродів, при вимірюванні електричного опору комірки застосовують змінний струм, використовуючи так звані мости змінного струму.
Опір будь-якого провідника струму розраховується за рівнянням:
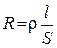 , (3.1)
, (3.1)
де 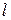 – довжина провідника (для розчинів – відстань між електродами);
– довжина провідника (для розчинів – відстань між електродами); 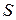 – площа поперечного перерізу провідника (площа електродів);
– площа поперечного перерізу провідника (площа електродів); 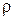 – питомий опір, який дорівнює опору провідника з одиничними довжиною та площею перерізу.
– питомий опір, який дорівнює опору провідника з одиничними довжиною та площею перерізу.
Величина, яка є оберненою питомому опору, називається питомою електропровідністю і позначається грецькою літерою 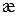 («каппа»). З рівняння (3.1) випливає, що
(«каппа»). З рівняння (3.1) випливає, що
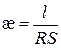 (3.2)
(3.2)
і має розмірність Ом -1×м -1 = См/м (у СІ) або Ом -1×см -1 = См/см (у системі СГС). Питома електрична провідність – це електропровідність об’єму розчину, який міститься між двома плоскими паралельними електродами одиничної площі, що розташовані на одиничній відстані один від одного. Вона залежить від природи електроліту та розчинника, концентрації розчину і температури.
Концентраційна залежність æ і для сильних, і для слабких електролітів зазвичай проходить через максимум. В розведених розчинах будь-яких електролітів внаслідок збільшення концентрації æ зростає внаслідок збільшення кількості іонів, які переносять електричний заряд. Після досягнення певної концентрації æ починає спадати, оскільки в розчинах сильних електролітів посилюється взаємодія між протилежно зарядженими іонами і швидкість їх руху сповільнюється, а у розчинах слабких електролітів доволі стрімко зменшується їх ступінь дисоціації. На відміну від металевих провідників опір електролітних розчинів внаслідок підвищення температури в переважній більшості випадків зменшується, тобто електропровідність зростає. Основною причиною цього є температурне зменшення в’язкості рідкого середовища.
Молярною (еквівалентною) електричною провідністю 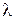 («лямбда») називається електропровідність об’єму розчину, який містить 1 моль (1 моль-екв) електроліту і знаходиться між двома паралельними електродами, що розташовані на одиничній відстані один від одного. Об’єм такого розчину залежить від його концентрації і називається розведенням розчину. Розведення розчину
(«лямбда») називається електропровідність об’єму розчину, який містить 1 моль (1 моль-екв) електроліту і знаходиться між двома паралельними електродами, що розташовані на одиничній відстані один від одного. Об’єм такого розчину залежить від його концентрації і називається розведенням розчину. Розведення розчину 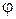 – величина, яка обернена молярній концентрації
– величина, яка обернена молярній концентрації 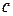 :
:
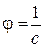 .
.
Для 1–1-валентних електролітів значення молярної і еквівалентної електропровідностей збігаються. Для електролітів інших валентних типів молярна електропровідність дорівнює добутку еквівалентної електропровідності та числа еквівалентів у одному молі речовини. У СІ молярну електропровідність обчислюють за формулою
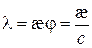 (3.3)
(3.3)
і вимірюють у См×м 2/моль. У системі СГС, в якій концентрацію зазвичай виражають у моль/дм3, а питому електропровідність – у См/см, рівняння (3.3) набуває вигляду
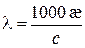 , (3.4)
, (3.4)
і молярна електропровідність має розмірність См×см 2/моль.
Молярна електропровідність залежить від таких самих факторів, що і питома. Внаслідок підвищення температури вона зростає. Збільшення концентрації розчину призводить до зменшення 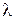 , тому що в розчинах сильних електролітів посилюється іон-іонна взаємодія, а в розчинах слабких електролітів зменшується їх ступінь дисоціації. При
, тому що в розчинах сильних електролітів посилюється іон-іонна взаємодія, а в розчинах слабких електролітів зменшується їх ступінь дисоціації. При 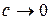 молярна електропровідність набуває максимального за певної температури значення
молярна електропровідність набуває максимального за певної температури значення 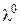 , яке називають граничною молярною електропровідністю.
, яке називають граничною молярною електропровідністю. 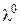 – це молярна електрична провідність гіпотетичного нескінченно розведеного розчину, що характеризується повною дисоціацією слабкого електроліту (
– це молярна електрична провідність гіпотетичного нескінченно розведеного розчину, що характеризується повною дисоціацією слабкого електроліту ( 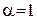 ) і відсутністю взаємодії між іонами сильного електроліту (середній іонний коефіцієнт активності електроліту
) і відсутністю взаємодії між іонами сильного електроліту (середній іонний коефіцієнт активності електроліту 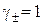 ).
).
Швидкість руху іона у розчині 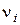 [м/с] прямо пропорційна напруженості електричного поля
[м/с] прямо пропорційна напруженості електричного поля 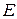 [В/м]:
[В/м]:
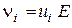 ,
,
де 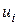 – абсолютна швидкість руху іона
– абсолютна швидкість руху іона 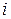 (за умови
(за умови 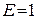 В/м). Молярна електропровідність або рухливість іона
В/м). Молярна електропровідність або рухливість іона 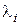 пов’язана з
пов’язана з 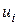 рівнянням
рівнянням
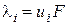 ,
,
в якому 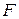 – стала Фарадея.
– стала Фарадея.
В розчинах слабких електролітів 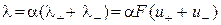 , (3.5)
, (3.5)
а в розчинах сильних електролітів, у яких 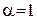 ,
,
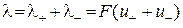 . (3.6)
. (3.6)
При нескінченному розведенні для будь-якого електроліту 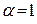 , і рівняння (3.5) і (3.6) записуються як
, і рівняння (3.5) і (3.6) записуються як
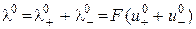 , (3.7)
, (3.7)
де 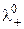 і
і 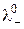 – граничні молярні рухливості катіона та аніона, відповідно;
– граничні молярні рухливості катіона та аніона, відповідно; 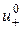 і
і 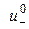 – абсолютні швидкості руху зазначених іонів у гранично розведеному розчині. Вираз (3.7) є математичним відображенням закону незалежного руху іонів Кольрауша, згідно з яким молярна електропровідність нескінченно розведеного розчину електроліту дорівнює сумі граничних іонних рухливостей. Фізичний зміст цього закону полягає в тому, що в зазначеному розчині іони переносять струм незалежно один від одного, тобто їх рухливості за певної температури є сталими і не залежать від природи протилежно зарядженого іона. Граничні молярні електропровідності іонів у воді за стандартної температури наведено в довіднику.
– абсолютні швидкості руху зазначених іонів у гранично розведеному розчині. Вираз (3.7) є математичним відображенням закону незалежного руху іонів Кольрауша, згідно з яким молярна електропровідність нескінченно розведеного розчину електроліту дорівнює сумі граничних іонних рухливостей. Фізичний зміст цього закону полягає в тому, що в зазначеному розчині іони переносять струм незалежно один від одного, тобто їх рухливості за певної температури є сталими і не залежать від природи протилежно зарядженого іона. Граничні молярні електропровідності іонів у воді за стандартної температури наведено в довіднику.
В розчинах слабких електролітів швидкість міграції іонів практично не залежить від їх кількості, тобто 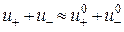 . З урахуванням цього факту на підставі рівнянь (3.5) та (3.7) для слабкого електроліту можна записати
. З урахуванням цього факту на підставі рівнянь (3.5) та (3.7) для слабкого електроліту можна записати
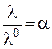 . (3.8)
. (3.8)
Для сильного електроліту з формул (3.6) і (3.7) випливає, що
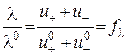 , (3.9)
, (3.9)
де 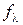 – коефіцієнт електропровідності, який враховує міжіонну взаємодію.
– коефіцієнт електропровідності, який враховує міжіонну взаємодію.
Константа рівноваги процесу електролітичної дисоціації (константа дисоціації) визначається за законом розведення Оствальда. Так, для дисоціації бінарного 1–1-валентного електроліту 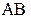 за схемою
за схемою
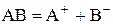

константа дисоціації 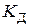 має вигляд:
має вигляд:
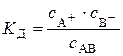 .
.
Якщо початкова концентрація електроліту дорівнює 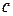 , а ступінь його дисоціації в розчині –
, а ступінь його дисоціації в розчині – 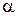 , то згідно із законом розведення Оствальда
, то згідно із законом розведення Оствальда
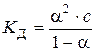 . (3.10)
. (3.10)
Константа дисоціації слабкого електроліту, як будь-яка константа рівноваги, є сталою величиною за умови 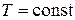 .
.
