Твердые вещества, в состав которых входит химически связанная вода;
2. твердые вещества, растворимые в воде;
3. твердые вещества, реагирующие с водой;
4. твердые вещества, не растворимые в воде.
43. Реакция, в которой окисляется водород:
1. CuO + H2 = Cu + H2O;
2. 2Na + H2 = 2NaH;
3. Mg + H2SO4 = MgSO4 + H2;
4. 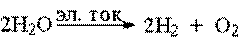
44. Галоген, в наибольшей степени проявляющий окислительные свойства: ____F2______ (впишите формулу простого вещества).
45. В ряду увеличивается восстановительная способность галогенидов:
1. KCl, KBr, KI, KF;
2. KI, KBr, KCl, KF;
3. KF, KI, KBr, KCl;
KF, KCl, KBr, KI.
46. Причина того, что алюминий не подвергается коррозии:
1. химически малоактивен;
2. пассивируется в концентрированных H2SO4 и HNO3;
3. взаимодействует со щелочами;
Покрыт защитной оксидной пленкой.
47. Опаснее всего подносить огонь к сосуду, в котором находится
1. азот;
2. кислород;
3. смесь водорода с кислородом;
4. водород.
48. Верное утверждение:
1. кислород имеет запах;
2. кислород хорошо растворим в воде;
3. кислород проводит электрический ток;
Кислород тяжелее воздуха.
49.
Вещество, не взаимодействующее с оксидом фосфора (V):
Оксид углерода (IV);
2. оксид кальция;
3. гидроксид калия;
4. вода.
50. Реакция, с помощью которой нельзя получить оксид цинка:
1. Zn + HCl 
2. 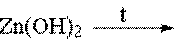
3. 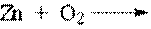
4. 
51. В уравнении реакции K2O + ZnO ®; : сумма коэффициентов равна
1. 3;
2. 4;
3. 5;
4. 6.
52. В уравнении реакции SO3 + Al2O3 ® : сумма коэффициентов равна
1. 3;
2. 4;
3. 5;
4. 6.
53. Водород в промышленности получают следующим способом:
1. действием кислот на активные металлы;
2. разделением воздуха;
Конверсией метана;
4. перегонкой нефти.
54. Для осушки аммиака его надо пропустить через
1. P2O5;
2. H2SO4 конц.;
NaOH;
4. CuSO4.
55. Качественный состав хлорида железа (III) можно установить, используя два раствора, содержащие соответственно ионы
1. CNS- и Ag+;
2. OH- и Ba2+;
3. CNS- и Ba2+;
4. OH- и H+.
56. Состав соли (NH4)2SO4 можно установить, используя два раствора, содержащие соответственно ионы
1. OH- и Ba2+;
2. OH- и H+;
3. Cl- и Cu2+;
4. CO32- и Ba2+.
57. Реакция, являющаяся качественной на ион SO42-:
1. SO3 + Ca(OH)2 = CaSO4 + H2O;
2. CuSO4 + Ni = NiSO4 + Cu;
3. Na2SO4 + BaCl2 = BaSO4 + 2NaCl;
4. 3Na2SO4 + 2Al(OH)3 = Al2(SO4)3 + 6NaOH.
58. Имеются газы: H2S, Cl2, SO2, CO2. Реактив, являющийся лучшим поглотителем всех этих газов:
1. H2O;
2. раствор HCl;
3. H2SO4;
NaOH.
5.
59. Выделение водорода будет наблюдаться в реакции:
1. Cu + H2SO4 (конц.) ® ;
2. Fe + H2SO4 (разб.) ® ;
3. Cu + HNO3 (конц.) ® ;
4. Fe + HNO3 (разб.) ®.
60. Ряд, в котором все вещества при добавлении воды образуют щелочи:
1. Na2O, Li, CaO, K;
2. Fe2O3, Li, CaO, Na;
3. Al2O3, CO2, Li, Fe2O3;
4. CaO, Na2O, Al2O3, Ca.
61. Ряд, в котором каждое из веществ образует с раствором щелочи осадок малорастворимого основания:
1. NaCl, FeCl3, Al2(SO4)3;
2. NH4Cl, CuSO4, MnCl2;
3. KNO3, Na2SO4, Cr(NO3)3;
4. CuSO4, FeCl3, Cr(NO3)3.
62. Ряд, в котором каждое из веществ реагирует с оксидом серы (IY):
1. H2O, SO3, NaCl;
2. H2O, O2, CaO;
3. Na2O, SiO2, H3PO4;
4. H2O, CaO, HCl.
63. Ряд, в котором каждое из веществ реагирует с молекулярным водородом:
1. HCl, NaCl, KOH;
2. Fe2O3, KOH;
3. Fe2O3, Cl2;
4. Fe2O3, KOH, Cl2.
64. Ряд, в котором каждое из веществ реагирует с хлороводородной кислотой:
1. Ca, H2, BaO;
2. Zn, H2O, BaSO4;
3. Al2O3, CO2, Cu;
4. MgO, Na2CO3, Fe.
65. Ряд, в котором каждый из металлов реагирует с разбавленной серной кислотой:
1. Na, Ag, Ba;
K, Ca, Ni;
3. Mg, Al, Pt;
4. Pb, Cr, Cu.
66. Ряд, в котором каждое из веществ взаимодействует с оксидом углерода (IV):
1. CaO, P2O5;
2. HCl, CaO;
3. NaCl, CaO;
4. Na2O, NaOH.
67. Ряд, в котором каждое из веществ вступает в реакцию с водным раствором карбоната натрия:
1. HNO3, CO2;
2. NaCl, CaCO3;
3. CO2, NaOH;
4. O2, Ba(NO3)2.
68. Ряд, в котором каждый из оксидов пригоден для использования в качестве осушителя (поглотителя воды):
1. CuO, P2O5;
2. BaO, CuO;
3. P2O5, BaO;
4. Fe3O4, P2O5.
69. Ряд, в котором каждое из веществ можно использовать для получения кислорода лабораторным способом:
1. KMnO4, H2SO4, NaCl;
2. NaNO3, Ba(OH)2, Al2O3;
3. HgO, Ba(OH)2, NaNO3;
4. KMnO4, H2O2, KClO3.
70. Ряд, в котором каждое из веществ несовместимо с присутствием озона:
1. SO2, CO2, H2S, HF;
2. SO2, H2S, H2, HF;
3. KJ, SO3, CO2, N2;
4. SO2, H2S, KJ, N2.
71. На чашках весов уравновешены стаканчики с растворами гидроксида натрия и хлорида натрия. Через некоторое время стрелка весов
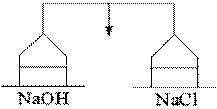
1. отклонится влево;
2. отклонится вправо;
3. не изменит своего положения.
72. Вещество, с которым взаимодействует сульфид натрия с образованием PbS:
1. Pb;
2. PbO;
3. Pb(NO3)2;
4. PbO2.
73. Реагент(ы), в реакции с которым(и) оксид азота (IV) образует только нитрат натрия и воду:
1. NaOH, Ca;
2. Na2S;
3. Na2SO4;
4. NaOH, O2.
74. Продукты, образующиеся при термическом разложении нитрата меди (II):
1. Cu(OH)2, O2, N2;
2. CuO, NO2, O2;
3. CuO, NO2;
4. Cu(NO3)2, O2.
75. Кислота, которую нельзя хранить ни в обычной посуде, ни в посуде из кварцевого стекла:
1. HNO3;
2. H2SiO3;
3. HBr;
HF.
76. В трех пробирках находятся растворы хлорида калия, бромида калия и иодида калия. Реактив, с помощью которого можно распознать все соли:
1. H2SO4;
2. HCl;
3. AgNO3;
4. AgCl.
77. В трех пробирках находятся концентрированные растворы кислот: H2SO4, HCl, HNO3. Реактив, с помощью которого можно распознать все кислоты:
1. BaCl2;
2. метиловый оранжевый;
Zn;
4. AgNO3.
78. Смесь железа, меди и алюминия обработали концентрированной азотной кислотой на холоду. При этом растворились следующие металлы:
1. Fe, Cu;
2. Все металлы;
3. Fe, Al;
Cu.
79. Масса стакана с концентрированной серной кислотой при длительном хранении
Увеличится;
2. уменьшится;
3. не изменится.
80. Из перечисленных процессов:
o а) растворение концентрированной серной кислоты в воде;
o б) испарение спирта;
o д) разложение воды
o в) гашение извести;
o г) горение водорода;
к экзотермическим относятся
А, в, г;
7. а, б, в, г, д;
8. б, д;
9. а, в, г, д.
1. В реакционной системе в равновесии находятся
 .
.
Чтобы сместить равновесие реакции вправо, необходимо
1. увеличить концентрацию CO2;
