Изменился ли подход к проблеме устойчивости дисперсных систем на современном этапе развития коллоидной химии?
Б.Д. Сумм предлагает различать 4 вида неустойчивости коллоидных систем:
(Давайте вспомним: под устойчивостью лиофобных дисперсных систем понимается их способность сопротивляться протеканию процессов, ведущих к изменению их дисперсности, характера распределения частиц по размерам, а также в объеме дисперсионной среды.)
1) Термодинамическая (агрегативная) неустойчивость проявляется в постепенном увеличении размеров дисперсных частиц или образования агрегатов из слипшихся частиц.
Эволюцию агрегативно неустойчивой дисперсной системы количественно характеризуют зависимостью размера частиц и их распределения по размерам от времени, а также временнóй зависимостью концентрации частиц. (Поясните, к чему в последнем случае ведет укрупнение частиц при неизменной общей массе дисперсной фазы.)
Избыточная поверхностная энергия As дисперсной системы описывается уравнением:
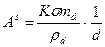 ,
,
где K – коэффициент формы; σ – удельная поверхностная энергия; ρd – плотность вещества дисперсной фазы, md – масса дисперсной фазы.
Это уравнение (Поясните, как оно получается.) показывает, что возможны два разных процесса уменьшения поверхностной энергии дисперсной системы:
-Укрупнение дисперсных частиц, приводящее к увеличению их размера (σ = const). Этот процесс называют коалесценцией (слиянием). Он характерен для систем с жидкими или газообразными частицами.
-Уменьшение удельной поверхностной энергии (поверхностного натяжения, d = const). Соответствующий процесс называется коагуляцией. Он заключается в образовании агрегатов из многих дисперсных частиц, разделенных тонкими прослойками дисперсионной среды. Коагуляция характерна для систем с твердыми частицами.
2) Седиментационная неустойчивость. Вызывается различием плотностей веществ дисперсной фазы и дисперсионной среды (ρo). Это различие приводит к постепенному оседанию (седиментации) более крупных частиц (если ρd > ρo) или их всплыванию (если ρd < ρo).
Размер дисперсных частиц влияет на агрегативную и седиментационную устойчивости противоположным образом. Чем выше степень дисперсности (меньше размер частиц), тем сильнее проявляется их агрегативная неустойчивость, однако растет их устойчивость по отношению к седиментации.
3) Фазовая неустойчивость. Имеется в виду изменение структуры частиц при сохранении их размеров. Например, при синтезе коллоидных растворов металлов, оксидов и гидроксидов дисперсные частицы обычно аморфны, а со временем внутри частиц может происходить энергетически выгодный процесс кристаллизации.
4) Поверхностная неустойчивость. Ее причины различны. Например, ПАВ с большой молекулярной массой (белки) медленно диффундируют из объема дисперсионной среды на поверхность частиц и со временем образуют адсорбционный слой. Другой возможный механизм – растворение вещества дисперсных частиц в дисперсионной среде. Оно обусловливает несколько процессов:
-изменение химического состава раствора вблизи поверхности частиц и изменение строения ДЭС;
-изменение микрорельефа твердой поверхности и, как следствие, изменение краевых углов смачивания.
Анализ причин и форм неустойчивости дисперсных систем приводит к следующему принципиальному заключению: неравновесность вызывает эволюцию дисперсных систем. Таким образом, характеристики дисперсных систем могут существенно изменяться во времени.
Основная проблема теории устойчивости дисперсных систем заключается в определении конкретных причин и механизма объединения отдельных дисперсных частиц в более крупные агрегаты и в выяснении факторов, которые препятствуют их агрегированию.
Теорию устойчивости гидрофобных золей детально разработали Б. Дерягин и Л. Ландау и независимо Э. Фервей и Т. Овербек (теория ДЛФО). (Вспомните, какие две силы в соответствии с основным упрощающим положением в теории ДЛФО действуют на твердые дисперсные частицы.) В зависимости от соотношения этих сил возможны два варианта поведения коллоидного раствора:
1) Если преобладает сила притяжения (|fd| >|fe|), то дисперсные частицы сближаются, между ними возникает контакт, и они объединяются в более крупный агрегат (коллоидный «димер»). Таким образом, в этом случае элементарный акт процесса коагуляции может состояться.
2) Если преобладает электростатическое отталкивание (|fd| <|fe|), то частицы могут не вступать в непосредственное соприкосновение, и коагуляция золя не происходит.
Таким образом, в качестве основного фактора термодинамической устойчивости дисперсной системы в теории ДЛФО принимают электростатическое (кулоновское) отталкивание дисперсных частиц.
Для расчета условий коагуляции вводятся дополнительные концепции:
1) Частицы имеют призматическую форму и разделены плоскопараллельным зазором шириной h (см. рис.).
2) Частицы перемещаются только в направлении, перпендикулярном зазору. Броуновское движение исключается.
Для расчета условий сопоставляются не силы притяжения, а соответствующие им энергии взаимодействия (Ud, Ue).
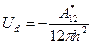
где 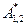 – сложная константа Гамакера; знак «–» указывает на взаимное притяжение.
– сложная константа Гамакера; знак «–» указывает на взаимное притяжение.
Энергия электростатического взаимодействия (Ue) создается вследствие перекрывания диффузных слоев противоионов в тонкой пленке раствора электролита в зазоре между частицами.
Ue, которая зависит от толщины пленки, создает в пленке дополнительное давление – расклинивающее давление (Π). Π – это термодинамический параметр тонкой жидкой пленки в пространстве между частицами:
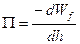 ,
,
где Wf – это работа, которую нужно затратить для увеличения поверхности тонкой пленки на единицу площади при постоянной температуре.
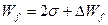 ,
,
где ΔWf – это дополнительная энергия пленки, которую нужно затратить для сближения поверхностных слоев ABB′A′ и CDD′C′. (Поясните коэффициент 2 в приведенном выражении.)
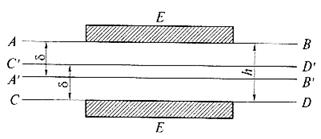
Рис. Возникновение расклинивающего давления в плоской тонкой пенной пленке с перекрыванием поверхностных слоев (h < 2δ)
По физическому смыслу величину Wf можно рассматривать как энергетическое определение поверхностного натяжения тонкой пленки.
Физический смысл величины Π – это избыточное давление в тонкой пленке по сравнению с гидростатическим давлением в большом объеме жидкости.
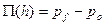 ,
,
где pf – давление в тонкой пленке.
Положительное расклинивающее давление препятствует утоньшению пленки!
Возникновение Π связано с поверхностными силами разной природы (электрическими, магнитными, молекулярными). Для коллоидной химии особенно важны первые и последние.
При толщине жидкой пленки 1 мкм Π может достигать 400 Па, а 0,04 мкм – 1,88∙104 Па.
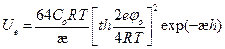 , (1)
, (1)
где 1/æ = δ – толщина ионной атмосферы.
Не обязательно запоминать формулы! Главное уяснить, что Ue и Ud имеют разные знаки и по-разному зависят от толщины разделяющей пленки h:
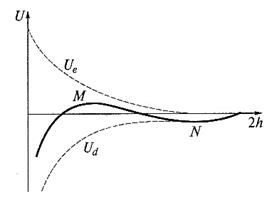
Рис. Изменение энергии (U) тонкой пленки электролита в зависимости от ее толщины (h)
Как видно из рисунка, Ue изменяется по экспоненциальному закону (пропорциональна e-æh), Ud – по степенному (пропорциональна 1/h2). Поэтому на малых расстояниях будет преобладать притяжение (при h → 0 Ud → ∞). На больших расстояниях также преобладает притяжение, т. к. степенная функция убывает медленнее, чем экспонента. На средних расстояниях возможен локальный (дальний) максимум. Он соответствует энергетическому (потенциальному) барьеру, который препятствует сближению частиц и их коагуляции.
Анализ уравнения и графика позволяет выделить три случая поведения дисперсной системы в зависимости от соотношения высоты энергетического барьера UM, глубины потенциальной ямы UN на больших расстояниях, и на малых расстояниях энергии тепловых колебаний kБT. (Проведите этот анализ!)
Как отмечалось ранее, изучение устойчивости дисперсных систем – это одна из самых важных и сложных проблем коллоидной химии. Выше были рассмотрены факторы, обеспечивающие стабильность во времени основных параметров дисперсных систем – дисперсности и равновесного распределения дисперсной фазы в дисперсионной среде. Приведите примеры, в которых стабилизация дисперсных систем является нежелательным явлением.
Зачастую образование коллоидных систем является нежелательным явлением, с которым приходится бороться. Так, при проведении многих технологических процессов имеет место пенообразование, которого стремятся избежать, например, в процессе очистки воды, при производстве лекарственных препаратов и т. п. Пенообразование чаще всего является результатом присутствия в системе примесей различных ПАВ; следовательно, образуется лиофильная коллоидная система, которая трудно поддается разрушению. (Вспомните, что понимают под терминами лиофильные и лиофобные системы. Приведите критерий лиофильности, который предложил Ребиндер.) Широко распространено также явление нежелательного образования устойчивых дисперсных систем типа Т-Ж. Самопроизвольное диспергирование глин в воде является примером образования стабильного лиофильного коллоида. Лиофобная высокодисперсная суспензия гидроксида железа, которая подлежит коагуляции, формируется при электроочистке воды. Процессы коагуляция широко используется в современной медицине для остановки кровотечения, удаления опухолей, соединения тканей и др.
Укажите примеры воздействий на дисперсные системы, которые могут снизить их агрегативную и седиментационную устойчивости, а также вызвать протекание структурных и химических превращений с участием веществ, образующих дисперсную фазу и дисперсионную среду.
Среди таких воздействий можно выделить:
-Изменение состава дисперсной системы (разбавление, концентрирование, введение электролитов и иных веществ).
-Механическое воздействие (интенсивное встряхивание, растирание, перемешивание, ультразвуковое воздействие, центрифугирование, действие магнитного поля и др.).
-Тепловое воздействие (нагревание или охлаждение).
-Действие излучений (рентгеновское, видимое, ультрафиолет, радиочастотное).
Указанные воздействия обычно одновременно нивелируют несколько факторов устойчивости дисперсных систем. (Подумайте, на какой фактор устойчивости будет в наибольшей степени влиять каждое из воздействий в случае а) мыльной пены, б) геля желатина, в) крови человека, г) золя оксогидроксида железа?)
