Общее уравнение баланса энергии
Уравнение баланса энергии в интегральной форме может быть получено из первого закона термодинамики и имеет вид
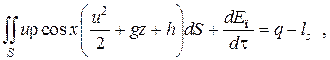
где первое слагаемое в скобках – кинетическая энергия движения жидкости, второе – потенциальная энергия положения, третье – энтальпия жидкости, Дж/кг;
Еп – полная энергия в контрольном объеме, Дж;
q – тепловой поток через контрольную поверхность, Вт;
ls – мощность на преодоление внешних сил, в основном трения, Вт;
u – скорость потока, м/с;
r – плотность среды, кг/м3;
x – угол между нормалью и контрольной поверхностью;
g – ускорение силы тяжести, м/с2;
z – геометрический напор, м;
h – удельная энтальпия, Дж/кг;
S – контрольная поверхность;
t – время, с.
Для химических процессов кинетическая и потенциальная энергии, а также мощность на преодоление внешних сил пренебрежимо малы по сравнению с энтальпией, поэтому можно записать
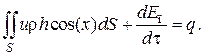
Это уравнение, по сути, является уравнением теплового баланса.
Для простого контрольного объема, ограниченного контрольными поверхностями, перпендикулярными вектору потока жидкости, интегрирование последнего уравнения дает
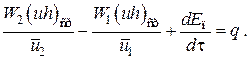
Первые два слагаемых в этом уравнении получены следующим образом. Если принять плотность постоянной, а cos(x)=±1, то
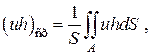 тогда
тогда 
Так как W=rūS, то получаем 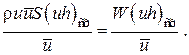
Если скорость незначительно меняется в обоих сечениях, а поток жидкости стационарен в гидродинамическом отношении, то уравнение баланса тепла можно записать следующим образом
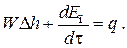
Если система стационарна и в тепловом отношении, то:
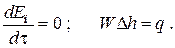
Если в системе не происходит фазовых превращений и химических реакций, то можно от энтальпий перейти к теплоемкостям и тогда
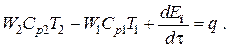
Рассмотрим пример применения уравнений теплового баланса в нестационарных условиях.
Пример 9.1. Два резервуара объемом по 3 м3 каждый заполнены водой при температуре 25 °С. Оба имеют мешалки, обеспечивающие практически полное перемешивание. В определенный момент времени в первый резервуар начинают подавать 9000 кг/ч воды при температуре 90 °С. Вода, выходящая из первого резервуара, поступает во второй. Определить температуру воды во втором резервуаре через 0,5 часа после начала подачи горячей воды. Резервуары считать теплоизолированными.
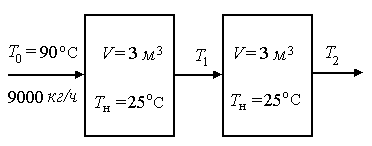 |
| Рис. 9.1. К примеру 9.1 |
Решение: Составим схему тепловых потоков (рис. 9.1) и тепловой баланс для первого резервуара. При отсутствии теплообмена q=0 и при условиях
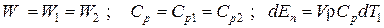
уравнение теплового баланса примет вид
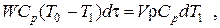
откуда 9000(90-T1)dt=3·1000dT1, или

После интегрирования от 0 до t и от 25 °С до T1 получим
T1=90-65exp(-3t).
Составим аналогичным образом тепловой баланс второй емкости
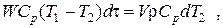
откуда 9000(T1-T2)dt=3·1000dT2, или

Получено линейное дифференциальное уравнение первого порядка. Его можно проинтегрировать известным способом аналитически. Тогда имеем
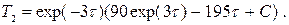
Начальные условия: при t=0 Т2=25 °С. Произвольная постоянная С = -65.
Окончательно решение примет вид
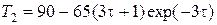 ;
;
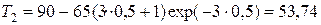 °С.
°С.
