В одинаковых объемах различных газов при одинаковых условиях (температура и давление) содержится одинаковое число частиц.
Из этого закона вытекают два следствия:
Следствие 1: 1 моль любого газа при нормальных условиях занимает объем 22,4 л/моль. Этот объем называется молярным и обозначается Vm
n =V/Vm (4)
Если условия нормальные (н.у.), то есть температура равна 00С (или 273,15 К – читается Кельвина), а давление 101,3 кПа, томолярный объем равен 22,4 л/моль.
Задача 3.2.1
Вычислите объем, который займет при нормальных условиях (н. у.) хлороводород массой 48.6 г
Дано: Решение:
m (HCl) = 48,6 г 1. Находим количество вещества
хлороводорода по формуле (2)
_____________ n = m (HCI) \ M(HCl)
Найти:V (HCl) - ? n = 48,6 \ 36,5 = 1.33 моль
2. Рассчитываем объем, который займет
хлороводород при н.у., используя формулу V = n *Vm
V(HCl) = 1,33* 22,4 = 27,79 л
Задача 3.2.2
Определите число частиц, которое содержится в 2,8 л оксида
серы (IV).
Дано: Решение:
V (SO2) = 2,8 л 1. Определяем количество вещества:
__________ n = V \Vm , V = 2,8 \ 22,4 = 0,125 моль
Найти: n (SO2)-? 2. Рассчитываем число молекул SO2
по формуле: n = n*NA ,
n = 0,125 * 6,02 * 1023 = 7,5*1022
Следствие 2: Плотность одного газа (D) относительно другого равна отношению молярных масс этих газов:
D=M (неизвестного газа) / M (известного газа) (5)
Наиболее часто пользуются значениями относительных плотностей газов по водороду и по воздуху:
D H2 = M / M (H2) = M /2
D воздуху = M / M (воздуха) = M / 29.
Задача 3.2.3
Определите плотность углекислого газа по воздуху и кислороду.
Дано: Решение:
М (СО2) = 44 г/моль 1. D воздуху (СO2) = 44/29 = 1, 52
D H2 (СО2)= 44/32=1,375
М (О2) = 32 г/моль
___________________
Найти: Dвоздуху (СO2) -?
D H2 (СО2)
Для идеального газа применимо уравнение Менделеева - Клапейрона,которое является математическим выражением объединенного газового закона и позволяет перейти от нормальных условий к условиям эксперимента:
PV= vRT (6)
Где, Р – давление, Па, V - объем, м3,
R -газовая постоянная = 8,31 кДж/моль,
v -количество вещества, моль
T-температура, К (читается кельвин)
Задача 3.2.4
Какой объем занимает при температуре 200С и давлении 250 кПа аммиак массой 51 г.
Дано: Решение:
t =200 С 1. Температура T(K)=273+ 20 =293К
P=250 КПа. 2. Находим количество вещества аммиака
m (NH3) = 51г n = m (NH3) \ M(NH3)
___________ n (NH3) = 51/17 = 3 моль
V- ? 3. Используя уравнение Менделеева-Клапейрона
рассчитываем объем:
V = nRT/P
V = 3*8,31*296/250 = 0,03 м3
ГЛАВА 4 ОСНОВНЫЕ ТИПЫ РАССЧЕТНЫХ
ЗАДАЧ
4.1 РАСЧЕТЫ ПО ХИМИЧЕСКОЙ ФОРМУЛЕ
Формула химического вещества показывает его стехиометрический состав. Например, формула воды Н2О показывает, что один моль этого вещества образован из 2 моль атомного водорода и 1 моль атомного кислорода. Это позволяет проводить различные расчеты, используя формулы химических соединений.
Задача 4.1.1
Определите металл, если молярная масса иодида трехвалентного металла в 3,972 раза больше молярной массы фторида этого же металла.
Дано: Решение
M (MeJ3)>M (MeF3) 1. Пусть М - молярную массу неизвестного
в 3,972 раза металла. Тогда, молярная масса иодида
______________ М+(127*3) = М+381 г/моль
Найти: М (Ме)- ? Молярная масса фторида М+(18*3) =
= М +54 г/моль
2. М+381/М+54 = 3,972
Решая уравнение, получаем М = 52,
это хром.
Задача 4.1.2
В смеси карбида кальция СаС2 и карбоната кальция содержится по 1,81 *1024 атомов кальция и кислорода. Вычислите массу этой смеси.
Дано: Решение:
СаС2, СаСО3 1. Пусть х - количество моль СаС2 ,
n(Ca)=n(O)=1,81*1024 у - количество моль СаСО3
______________
2. Количество вещества кальция в смеси - х +у,
Найти: количество моль кислорода в смеси - 3у
m-?
3. Найдем количества вещества, используя
формулу: n=n*NA
nCа =nо = 1,81*1024/6,02*1023 = 3 моль
4. Составляем систему уравнений: количество моль кальция в смеси х+у=3, количество моль кислорода 3у = 3
х+у = 3
{3у = 3 Решая систему, получаем х. = 2, у = 1.
5. Массу карбида кальция и карбоната кальция рассчитываем по
формуле: m = n*M
m (CaC2) = 2*64 = 128г m (CaCO3) =1*100 = 100 г
Масса смеси (128 +100)=228 г
МАССОВАЯ ДОЛЯ ЭЛЕМЕНТА в сложном веществе W – это отношение массы данного элемента m эл-та к массе всего вещества mв-ва.
Массовая доля – безразмерная величина. Ее выражают в долях, от нуля до единицы или в %.
ω=mэл-та / m в-ва (7)
Задача 4.1.3
Вычислите массовую долю алюминия в карбиде алюминия.
Дано: Решение:
Al4C3 1. Пусть количество вещества карбида
_______ алюминия равно 1, тогда масса карбида
будет равна: m=1*M = М
Найти: M(Al4C3) = ((27х4) + (12х3) = 144г /моль
ω (Al) - ? m (Al4C3) = 144 г
2. Из формулы карбида Al4C3 следует, что количество моль
алюминия в карбиде равно 4, тогда масса атомного алюминия, который содержится в карбиде:
m (Al) = n (Al) * M (Al), m (Al) = 4 * 27 = 108 г.
3. Массовую долю алюминия в карбиде можно найти, используя
формулу (7): ω (Al) = m (Al) / m (Al4C3),
ω (Al) = 108 / 144 x 100% = 75 %
Задача 4.1.4
Вычислите массовую долю натрия в кристаллогидрате гидрофосфата натрия, в котором число атомов водорода в 1,364 раза больше числа атомов кислорода.
Дано: Решение:
Na2HPO4*хH2O 1. Кристаллогидраты - это соли, в состав
n (H)/n(O) =1,364 которых входит химически связанная вода.
Пусть х – это число молекул воды в
_______________ кристаллогидрате.
Найти: 2. Число атомов водорода в кристаллогидрате
ω (Na) - ? 1+2х, а число атомов кислорода – 4+х
3. По условию задачи nH/no=1,364, составляем уравнение 1,364 = 1+2х/ 4+х
Решая это уравнение, находим х. = 7.
Значит формула кристаллогидрата Na2HPO4*7H2О
3. Пусть количество вещества кристаллогидрата - 1 моль, тогда масса
кристаллогидрата равна:
m (Na2HPO4*7H2О) = 1*M
M (Na2HPO4*7H2О) =1*268 = 268 г.
4. Из формулы Na2HPO4*7H2О следует, что количество моль натрия в кристаллогидрате равно 2, тогда масса атомного натрия равна:
m (Na) = n* M (Na), m (Na) = 2* 23 = 48 г.
5. Массовую долю натрия в кристаллогидрате можно найти, используя формулу (7): ω (Na) = m (Na) / m (Na2HPO4*7H2О)
ω (Na) = m (Na) / m (Na2HPO4*7H2О)
ω (Na) = 46 / 268* 100% = 17,2 % (или 0,172 - в долях).
Задача 4.1.5
В смеси оксида меди (I) и оксида меди (II) на 4 атома меди приходится 3 атома кислорода. Вычислите массовые доли веществ в такой смеси
Дано: Решение:
Cu2O 1. Пусть х – это количество моль Cu2O
СuO y- количество моль СuO
N /n (Cu) = 4/3 Количество моль меди в смеси 2х+у,
__________ а количество моль кислорода х+у
ω (CuO)- ?
ω (Сu2O)-? 2. По условию задачи: 4/3=2х+4/х+у.
Преобразуя это выражение, получаем у = 2х
3. Масса оксида меди (1) равна 144 х (m=n*M), масса оксида меди (2) равна 80у. Масса смеси оксидов составляет 144х + 80у
4. Массовая доля меди в смеси равна:
w (Сu) = m (Сu)/m (Сu2О + СuО),
w (Сu) = 144x /144x+80у
Подставляя выражение у = 2х, получаем уравнение с одной переменной:
144х/144х+80*2х = 0,4737 (или 47,37%).
Массовая доля оксида меди (II) =100% - 47,37% = 52,63%
Ответ: ω(Сu2O) = 47,37 % , ω(CuO) = 52,63 %
Задача 4.1.6
В каком соотношении (моль) смешаны гидрофосфат кальция СаНРО4 и дигидрофосфат кальция Са(НРО4)2, если массовая доля кальция в смеси составляет 20%.
Дано: Решение:
СаНРО4 1 Пусть х - количество моль СаНРО4,
Са(НРО4)2 у - количество моль Са(НРО4)2 ,
ω (Са) = 20 % тогда массы гидрофосфата и
__________________ дигидрофосфата кальция рассчитываем
Найти: по формуле m = n *M
nСаНРО4 /nСа(НРО4)2 m (СаНРО4) = 136х
m (Са(НРО4)2 = 234у
2.Суммарное количество (моль) кальция в солях х+у, масса m (Са) = n*M , m (Ca) = (х+у)*40
3. Массовая доля кальция в смеси будет равна
ω(Сa)= m(Сa)/ m СaHPO4 + m Сa(HPO4)2
ω (Сa) = 40(х+у) / 136х + 234у = 0,2
Преобразуя это выражение, получаем у/х =1,87, то есть
nСаНРО4 /nСа(НРО4)2 = 1:1,87
ВЫВОД ФОРМУЛ СОЕДИНЕНИЙ
Химические формулы отражают количественный и качественный состав соединения.
В качестве примера рассмотрим сульфит натрия Na2SO3. Качественный состав показывает, какие элементы образуют соединение: в состав сульфита натрия входят: кислород, сера и натрий. Количественный состав: в этом соединении 2 моль натрия, 1 моль серы и 3 моль кислорода.
Задача 4.2.1
В состав соединения входят натрий, фосфор и кислород. Массовые доли элементов составляют: натрия – 34,6 % (в долях – 0,346), фосфора – 23,3 % (в долях – 0,233), кислорода – 42,1 % (в долях 0,421). Определите формулу соединения.
Дано: Решение:
ω (Na) = 34,6 % 1 . Пусть масса вещества равна 100 г. Тогда по
ω (P) = 23,3 % формуле (3) масса натрия, фосфора и
ω (O) = 42,1 % кислорода составляют:
m(Na)=100*W(Na), m(Na) =100*0,346 =34,6 г
_____________ m(P) = 100*W (P) , m(P) = 100*0,233 = 23,3 г.
Найти: m(O) = 100*W(O), m(O) = 100* 0,421= 42,1 г.
формулу
2. Определяем количество вещества атомных
натрия, фосфора и кислорода:
n (Na) =m(Na)/M, n (Na) = 34,6/23 = 1,50 моль.
n (P) = m(P)/M(P), n(P) = 23,3/31 = 0,75 моль.
n (O) = m (O)/M(O), n(O) = 42,1/16 = 2,63 моль.
CОКРАЩАЕМ ДО СОТЫХ.
3. Количество вещества натрия относится к количеству вещества фосфора и относится к количеству вещества кислорода как:
n (Na) : n (P) : n (O) = 1,50 : 0,75 : 2,63
ДЕЛИМ НА МЕНЬШЕЕ ЧИСЛО.
В данном примере: разделим на 0,75
n (Na) : n (O) : n (P) = 1,50/0,75 : 0,75/0,75: 2,63/0,75 = 2 : 1: 3,5
Так как в формулах соединений обычно используют целочисленные коэффициенты, то необходимо умножить это отношение на множитель, так, чтобы получилось целое число. В данном случае, умножаем на 2.
n (Na) : n (P) : n (O) = 4 : 2 : 7.
Следовательно, формула соединения, Na4P2O7.
Задача 4.2.2
Молярная масса соединения азота с водородом равна 32 г/моль. Определите формулу этого соединения, если массовая доля азота в нем составляет 87,5 %.
Дано: Решение:
M (NХHУ) = 32 г/моль 1. Обозначим х – количество моль азота
у - количество моль водорода.
ω (N) = 87,5 % 2. Т.к. соединение содержит два элемента,
______________ то массовая доля водорода составляет 12,5%
Найти: NхHу (все соединение 100 %, а азота в нем
87,5 %, значит массовая доля водорода
равна (100 – 87,5 = 12,5%)
3. Пусть масса вещества равна 100 г. Тогда по формуле (3) масса
азота и водорода составляют:
m (N) = m * ω (N), m (N) = 100 *0,875 = 87,5 г
m (H) = m * ω (H), m (Н) = 100 * 0,125 = 12,5 г
4. Определяем количество вещества атомных азота и водорода (используем формулу 2):
n(N) = m (N) / M (N), n (N) = 87,5 / 14 = 7,29 моль.
n (H) = m (H) / M (H), n (H) = 12,5 / 1 = 12,5 моль.
5. Находим отношение количеств веществ:
n (N) : n (H) = 7,29 : 12,5
ДЕЛИМ НА МЕНЬШЕЕ ЧИСЛО.
В данном случае разделим на 7,29.
Получаем: n (N) : n (H) = 7,29 / 7,29 : 12,5 / 7,29 ,
n (N) : n (H) = 1 / 2.
Следовательно, простейшая формула соединения NH2.
6. Проверим, соответствует ли молярная масса NH2 молярной
массе, предложенной в условии задачи.
Молярная масса (NH2) = (14+2)=16. Для того, чтобы получить истинную формулу соединения, необходимо все умножить на два. Значит, формула единения – N2H4.
Задача 4. 2.3
В состав соли входят: железо, азот, кислород и химически связанная вода. Определите формулу соли, если массовая доля железа составляет 13,86 %, массовая доля азота –10,4%, кислорода – 35,64%, воды – 40,1%.
Дано: Решение:
ω (Fe) = 13,86 % 1. Пусть масса соли равна 100 г
ω (N) = 10,4 % Подставляя это значение в формулу 4
ω (O) = 35,64% ω (Fe) = m(Fe) /100 *100% = 13,86%
ω (H2O) = 40,1% получаем массу железа - m(Fe) = 13,68г,
_______________ Аналогично определяем массу азота
Найти: формулу кислорода и воды:
m (N) = 10,4 г
m (O) = 35,64 г
m (H2O) = 40,1г
3.Определим количества вещества железа, азота, кислорода и воды соответственно, используя формулу (2):
n (Fe) : n(N) : n(O) : n (H2O)
13,86 /56 : 10,4 /14 : 35,64/16 : 40,1/18
4. Получим соотношение:
n (Fe): n(N): n(O): n(H2O)
0,25 : 0,74: 2,23 : 2,23.
Разделим на наименьшее значение, получаем
n (Fe) : n (N) : n (O) :n (H2O)
1 : 2,96 : 8,92 : 8,92
округляем: 1 : 3 : 9 : 9
Формула соли – Fe N3О9(H2O)9 . Преобразуя, получаем:
Fe(NО3)3 *9H2O
Задача 4.2.4
Выведите формулу кристаллогидрата сульфата натрия, если известно, что массовая доля кристаллизационной воды в нем равна 55,9 %.
Дано: Решение
ω (*х H2O)=55,9 % 1. Массовая доля воды в кристаллогидрате
равна:
ω(ХН2O)=m ((х Н2O)/m (Na2SO4*хH2O)=0,559
_______________ 2. Возьмем 1 моль кристаллогидрата, тогда
Найти: m = 1*М (Na2SO4 *хН2О) = (142+ 18х) г
Na2 SO4 *х H2 O ? m =М (х H2O)=(18* х) г
Подставляем в формулу (7) значения и получаем уравнение:
0,559=18х/142+18х, решая его, получаем х=10
Na2SO4*10H2O- это глауберова соль.
Задача 4.2.5
Массовая доля кислорода в кристаллогидрате нитрата железа (III) равна 0,713.Установите формулу кристаллогидрата.
Дано: Решение:
Fe (NO3)3*x H2O 1. Пусть количество моль Fe(NO3)3*xH2О = 1,
ω(O)в кристал.=0,713 тогда масса кристаллогидрата по формуле:
__________________ m = n *M
Найти формулу m (Fe(NO3)3*x H2O) = 242+ 18х
кристаллогидрата - ?
2. Количество моль кислорода в кристаллогидрате: 9+х, тогда массу кислорода рассчитываем по формуле: m (О) = n *M
m (О) = (9+х)*16 г
3. Массовая доля кислорода в кристаллогидрате:
w (О) = m (О) / m Fe(NO3)3 *H2O
w (О) = (9+х)*16/242+ 18х
Решая это уравнение, находим х = 9.
Значит, формула кристаллогидрата - Fe(NO3)3*9 H2O
РАСТВОРЫ
Растворами называют однородные системы переменного состава, состоящие из двух или более, компонентов. Состав растворов обычно выражают в массовых долях растворенного вещества.
МАССОВАЯ ДОЛЯ РАСТВОРЕННОГО ВЕЩЕСТВАω– это отношение массы данного компонента m (х) к массе раствора m p-pa
ω(Х) = m (х)/m p-pa (8)
Массу раствора можно найти, если известна плотность (г/мл) и объем раствора (мл):m p-pa = (V*р) р-ра, тогда формула (8) примет вид:
ω(х) = m(х)/(V*р) р-ра (9)
Задача 4.3.1
В воде массой 800 г растворили оксид серы (IV) объемом 7.84 л (н.у.) Вычислите массовую долю SO2 в растворе.
Дано: Решение:
M (H2O) = 800 г 1. Находим по формуле количество вещества
V (SO2) = 7,84 л n (SO2)=V/Vm ,
_____________ n (SO2) = 7,84 / 22,4 = 0,35 моль
Найти: 2. Масса оксида серы по формуле (2) равна:
ω(SO2) в р-ре-? m (SO2) = 64 * 0, 35 = 22,4 г
3. Масса полученного раствора равна:
m (p-pa) = m (SO2) + m (H2O) ,
m (p-pa) = 22,4 + 800 = 822,4 г
4. Массовую долю растворенного оксида серы (IV) можно рассчитать по формуле (6):
ω (SO2) в р-ре = 22,4 / 822,4 *100 % = 2,72 %
ω (SO2)=2,72%
Задача 4.3.2
Определите массу соли и массу воды, которые потребуются для
приготовления раствора объемом 120 мл (плотностью 1,1 г/ мл) с массовой долей 0,15 (15 %).
Дано: Решение:
V p-pa=120 мл 1. Массу раствора можно определить,
р р-ра = 1,1 г/мл используя формулу: m p-pa = V* p
ω = 15 % m p-pa = 120*1,1 = 132 г
2. Используя формулу (6), рассчитываем массу
___________ соли m (соли) = ω * m (p-pa) ,
Найти: mсоли -? m (соли) = 0,15*132 = 19,8 г
Задача 4.3.3
Какой объем раствора серной кислоты плотностью 1,8 г/мл c массовой долей 88 % H2SO4 надо взять для приготовления 300 мл и плотностью 1,3 г/мл с массовой долей кислоты H2SO4 40%.
Дано: Решение:
V2 p-pa (H2SO4)=300 мл 1. Определяем массу H2SO4 , необходимую
ω2 = 40 % для приготовления второго раствора
р2 = 1,3 г/м m в-ва = V*p*ω
р1 = 1,8 г/мл m (H2SO4) = 300*1,3*0,4 = 156 г
ω 1 = 88%
_______________ 2. Подставляем это значение для расчета
Найти объема первого раствора:
V p-pa H2SO4 -? 156 = 88 %* 1,8* V (p-pa) ,
V (p-pa) = 156/0,88*1,8 = 98,48 мл
Задача 4.3.4
Определите массу воды, которую надо добавить к 20 г 70%-ного раствора уксусной кислоты для получения 3%-ного раствора уксуса.
Дано: Решение
m р-ра(СН3СООН) = 20 г 1. Найдем массу уксусной кислоты,
ω1 = 70 % содержащаяся в 70%-ном растворе:
ω2 = 3 % m(CH3COOH) = m(раствора 1)∙ω1
_________________ m(CH3COOH = 20∙0,7 = 14 г.
Найти:
m (Н2О) -? 2. Масса 3%-ного раствора уксуса
m (раствора 2) складывается из массы 70%-ного раствора и массы воды (x), которую надо добавить к этому раствору:
m(раствора 2) = m(раствора 1) + x = 20 + x.
ω2 = 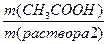 ; 0,03 =
; 0,03 = 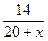 , откуда x = 447 г
, откуда x = 447 г
МОЛЯРНАЯ КОНЦЕНТРАЦИЯ (молярность) С – показывает количество моль растворенного вещества, содержащееся в 1л раствора.
C = n/V (10)
Где, С - молярная концентрация, моль/л
V - объем раствора, л
Задача 4.3.5
Определите молярную концентрацию раствора, полученного при растворении сульфита натрия массой 42,6 г в воде массой 300 г, если плотность полученного раствора равна 1,12 г/мл.
Дано: Решение
m (Na2SO3) = 42,6 г 1. Найдем массу раствора
m (Н2О) = 300г m (p-p) = m (Na2SO3)+m (H2O):
р = 1,12 г/мл m (p-p) = 42,6+300 = 342,6 г
_____________
Найти 2. Рассчитаем объем раствора:
С-? V p-p (Na2SO3) = mр-р /pр-р
Vр-ра = 342,6/1,12 = 305,89 мл
3. Найдем количество моль сульфита натрия
n = m /М (Na2SO3)
n (Na2SO3) = 42,6/126 = 0,34 моль
4 . Молярная концентрация соли в растворе:
С (Na2CO3) = n/V
C = 0,34/305,89*10-3 =1,11 моль/л
УПРАЖНЕНИЯ
1. Масса молекулы хлорофилла равна 1,485*10-18 мг. Вычислите
молярную массу хлорофилла
2. Молярная масса оксида двухвалентного металла в 3,928 раз
меньше молярной массы фосфата этого же металла. Определите металл.
3. Плотность по воздуху хлорида и бромида одного и того же элемента равна соответственно 5,31 и 11,45. Какой элемент образует указанные галогениды ?
4. Рассчитайте массовую долю элементов в K4[Fe(CN)6]
5. Органическое соединение содержит углерод (массовая доля
84,21 %) и водород. Определите формулу этого соединения, если плотность паров этого соединения по воздуху равна 3,93
6. Массовые доли элементов, входящих в состав некоторого химическуого соединения, составляют железа – 23,1%, азота – 17,4 %, кислорода – 59,5% . Определите химическую формулу этого соединения.
7. Выведите формулу кристаллогидрата нитрата кальция, если известно, что массовая доля воды в нем равна 30,5 %
8. В смеси хлоридов железа (II) и (III) на 5 атомов железа приходится 13 атомов хлора. Вычислите массовые доли веществ в такой смеси
9. В смеси карборунда (SiC) и кварца (SiO2) содержится по 3,01*1024 атомов кремния и кислорода. Вычислите массу смеси.
10. В каком соотношении (моль) были смешаны гидросульфит и гидросульфид натрия, если массовая доля серы в смеси составила 45% .
ЗАДАЧИ ИЗ ТЕСТОВ ЕГЭ
1. Какая масса осадка образуется при взаимодействии избытка раствора хлорида кальция с 65,6 г раствора фосфата натрия с массовой долей растворенного вещества 10%.
2. Массовые доли кислорода, фосфора и водорода в кислоте составляют соответственно 62,92%, 34,83% и 2,25%. Определите формулу кислоты.
3. Найти массу сульфида железа (II), вступающего в реакцию с 8,4 л (н.у.) кислорода.
4. К 200 г 10%-ного раствора хлорида калия добавили 50 г воды. Чему равна массовая доля KCl в получившемся растворе?
5. Найти массу соли, которая водится в организм при вливании 353 г физиологического раствора, содержащего 0,85% NaCl.
6. Определите массу карбоната натрия, которую надо добавить к 120 г 12%-ного раствора карбоната натрия для получения 20%-ного раствора.
7.Смешали 120 г раствора серной кислоты с массовой долей 20 % и 40 г 50% раствора того же вещества. Определить массовую долю кислоты в полученном растворе.
8. Определите массу серной кислоты, содержащейся в 196 мл 10 % раствора серной кислоты ( плотностью 1,07 г.мл)
9. Найти массу 30%-ного раствора серной кислоты, которую необходимо прибавить к 300 г воды, чтобы получить 10%-ный раствор серной кислоты.
10. Какой объем раствора с массовой долей серной кислоты 9,3%
(плотность 1,05 г/мл) потребуется для приготовления раствора с молярной концентрацией 0,35 моль/л серной кислоты объемом 40 мл
