Рефрактометрический метод определения концентрации этилового спирта
Показатель преломления водно-спиртового раствора зависит от его крепости.
Эта зависимость носит экстремальный характер: сначала с увеличением концентрации спирта показатель преломления растет. Достигнув максимума в определенной точке (80% масс.), показатель преломления в дальнейшем с увеличением концентрации растворов постепенно падает.
Поэтому водно-спиртовые растворы, содержащие до 52 масс. % спирта, рефрактометрируются непосредственно, а более концентрированные растворы разбавляются вдвое по массе дистиллированной водой (не по объему), а затем найденную концентрацию удваивают.
Работая с водно-спиртовыми растворами, особенно строго соблюдают температуру растворов и призм рефрактометра, т.к. показатель преломления спирта резко изменяется в зависимости от температуры.
Этиловый спирт очень летуч, поэтому все работы с ним проводят быстро, очень осторожно и без потерь. Для определения концентрации спирта в продукции рефрактометрируют, как правило, также дистиллят, а не исходный продукт. Исключение составляют приборы учета алкоголя на производстве, принцип действия которых основан на измерении показателя преломления. В них определение крепости осуществляется в готовой продукции.
5.3 Определение содержания спирта в вине ареометрическим методом
5.3.1 Приборы, посуда, материалы: установка для перегонки (электрическая плитка, перегонная колба 1000 см3, каплеуловитель, холодильник, приемная колба 250 см3, емкость с холодной водой), термометр, спиртомер (ареометр), цилиндр 250 см3, анализируемое вино.
5.3.2 Получение дистиллята
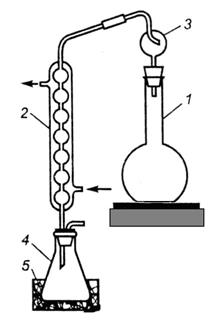 Рисунок 5.1 – Перегонная установка Рисунок 5.1 – Перегонная установка | 1 – перегонная колба 2 – холодильник 3 – каплеуловитель 4 – приемная колба 5 – емкость с холодной водой |
Довести исследуемый образец вина до 20оС.
Наполнить мерную колбу на 250 см3 анализируемым раствором до метки.
Количественно перенести содержимое мерной колбы в перегонную колбу (для этого перелить содержимое мерной колбы в перегонную, ополоснуть мерную колбу 3 раза дистиллированной водой, сливая воду в перегонную колбу).
В мерную колбу которая будет служить приемной, поместить 10-15 см3 дистиллированной воды и погрузить в нее узкий конец стеклянной трубки холодильника, затем колбу поместить в емкость с холодной водой.
Перегонную колбу соединить через каплеуловитель с холодильником и поместить ее на электроплитку.
Во время перегонки следить за тем, чтобы кипение проходило равномерно.
Когда приемная колба наполнится примерно на 3/4 объема, закончить перегонку.
Довести температуру дистиллята до 20оС.
Довести объем дистиллята до метки дистиллированной водой, тщательно перемешать.
5.3.3 Определение объемной доли спирта в дистилляте
Перелить дистиллят (t=20оС) в мерный цилиндр, установленный на поддон.
Плавно погрузить в дистиллят чистый и сухой ареометр (соблюдая все правила, указанные в п.4.2.2.2).
Произвести отсчет по шкале ареометра.
Определение объемной доли спирта с помощью ареометра провести дважды.
После использования ареометр тщательно вымыть и вытереть насухо.
Допускается не доводить температуру дистиллята до 20оС. В этом случае измеряют температуру дистиллята, при этой температуре с помощью спиртомера определяют объемную долю спирта в дистилляте и затем используют таблицу для расчета объемной доли спирта в водно-спиртовых растворах при 20оС.
5.4 Результаты определения
Результаты определения поместить в таблицу. Полученное среднее значение объемной доли спирта в вине сравнить с данными, указанными на таре. Сделать выводы.
| Объемная доля спирта в вине, % об. | Х1 | |
| Х2 | ||
| ХCP | ||
| Х(норма) |
5.5 Контрольные вопросы
1)Какое технологическое значение имеет определение содержания спирта в продуктах и полуфабрикатах бродильной промышленности?
2)В чем состоит суть большинства методов определения содержания спирта в алкогольной продукции?
3)Что такое дистилляция? Ее цель при определении концентрации спирта.
4)Из каких основных элементов состоит перегонная установка?
5)Правила проведения перегонки.
6)Какими методами определяют концентрацию спирта в растворе? В каких случаях применяют тот или иной метод?
7)Опишите ареометрический метод определения концентрации спирта.
8)Опишите пикнометрический метод определения концентрации спирта.
9)Как определяется концентрация спирта в готовой продукции с помощью рефрактометра?
10)В чем особенность рефрактометрического определения концентрации спирта?
6 Лабораторная работа №4 «Определение активности ферментов»
6.1 Цель работы: освоить методику определения активности амилолитических ферментов в свежепроросшем солоде методом Виндиша-Кольбаха.
6.2 Теоретические сведения
Ферменты – биологические катализаторы белковой природы, ускоряющие в несколько раз химические реакции в живом организме, но сами не входящие в состав конечных продуктов реакций
Среди ферментов в пивоваренной и спиртовой промышленности большое значение имеют амилолитические ферменты, под действием которых происходит гидролиз крахмала на сбраживаемые углеводы.
Крахмал представлен двумя полисахаридами. Это амилоза и амилопектин. Молекула амилозы представляет собой длинную цепочку глюкозных остатков, связанных между собой α-1,4 связями. Молекула амилопектина представляет собой разветвленную цепь, состоящую из большого числа глюкозных остатков. Остатки глюкозы в молекуле амилопектина связаны в пределах цепочки α-1,4 связями, в местах ветвления α-1,6 связями.
Гидролиз крахмала под действием ферментов солода α-амилазы и β-амилазы происходит следующим образом.
Фермент α-амилаза гидролизует α-1,4 связи внутри молекулы амилозы и амилопектина. Механизм действия неупорядоченный. В результате образуются продукты неполного гидролиза – декстрины. При длительном воздействии α-амилазы на амилозу фермент почти полностью превращает ее в мальтозу, мальтотриозу и небольшое количество глюкозы. Действие α-амилазы на амилопектин приводит к образованию мальтозы и низкомолекулярных декстринов (предельных декстринов) с 5-8 глюкозными остатками, поскольку фермент не действует на α-1,6 связи.
Фермент β-амилаза гидролизует α-1,4 связи с нередуцирующих концов амилозы и амилопектина, отщепляя по молекуле мальтозы (также не расщепляет α-1,6 связи).
При совместном действии α- и β-амилаз на крахмал образуется 95% сбраживаемых сахаров и 5% несбраживаемых предельных декстринов.
В проросшем зерне ячменя, ржи, пшеницы содержатся активные α-амилаза и β-амилаза. Они хорошо растворяются в воде и могут быть получены в виде водной вытяжки. В непроросшем зерне содержится только β-амилаза, α-амилаза переходит в активное состояние и частично образуется лишь при прорастании.
Поэтому главной целью солодоращения является образование и накопление амилолитических ферментов.
Активность амилолитических ферментов свежепроросшего солода свидетельствует о его качестве. В пивоварении принято определять суммарную активность амилолитических ферментов α- и β-амилаз. В международной практике используют метод Виндиша–Кольбаха, сущность которого заключается в том, что солодовой вытяжкой анализируемого солода осахаривают 2%ный раствор крахмала при рН=4,3 и образовавшуюся мальтозу определяют йодометрически.
Обычно амилолитическая активность (по Виндишу-Кольбаху) светлого свежепроросшего солода составляет 300-400 ед W-K. АС больше 250 ед. W-K считается очень хорошей, от 200 до 250 ед. W-K – достаточно хорошей.
6.3 Определение амилолитической активности солода методом Виндиша-Кольбаха
6.3.1 Приборы, посуда, материалы: весы технические, водяная баня, термометр, бюретка, пипетки, колбы мерные (200 см3), колбы конические (250 см3), свежепроросший солод, дистиллированная вода, 2%-ный буферный раствор крахмала (рН=4,3); 1н раствор NaOH, 1н раствор H2SO4, 0,1н раствор йода, 0,1н раствор тиосульфата натрия (Na2S2O3).
6.3.2 Приготовление солодовой вытяжки
Тщательно растереть свежепроросший солод в ступке. Отвесить навеску 20 г растертого солода в предварительно взвешенную коническую колбу на 500 см3, прилить
450 см3 дистиллированной воды и поставить на водяную баню (40оС) на 1 ч.
После этого содержимое колбы охладить до 20оС, довести его массу до 520 г и отфильтровать через бумажный складчатый фильтр.
6.3.3 Определение массовой доли влаги в свежепроросшем солоде
Массовая доля влаги в свежепроросшем солоде определяется методом высушивания с предварительным подсушиванием.
6.3.4 Осахаривание крахмала
В мерную колбу на 200 см3 отмерить пипеткой 100 см3 буферного раствора крахмала и выдержать колбу 10 мин в водяной бане при 20оС.
После этого прибавить 5 см3 солодовой вытяжки, хорошо перемешать и поместить колбу на водяную баню (20оС) точно на 30 мин.
Прекратить осахаривание крахмала путем добавления 3 см3 1н раствора NaOH.
Довести объем до метки и тщательно перемешать.
6.3.5 Определение мальтозы
Отмерить 50 см3 осахаренного крахмала в коническую колбу на 250 см3.
Прилить к раствору 25 см3 0,1н раствора йода и 3 см3 1н раствора NaOH, перемешать и выдержать 5 мин при комнатной температуре.
Прилить к раствору 4,5 см3 1н раствора H2SO4.
Избыток йода оттитровать 0,1н раствором тиосульфата натрия (Na2S2O3).
Индикатором в данном случае служит содержащийся в растворе неосахаренный крахмал. Количество йода пошедшего на окисление мальтозы должно находиться в пределах 5…15 см3. Если в реакции связывается больше 15 см3 йода, то опыт повторяют с вытяжкой, приготовленной из 10 г солода. Если меньше 5 см3, то берут 40 г солода.
Кроме того, определенное в опыте количество йода идет не только на окисление образовавшейся мальтозы, но и связывается веществами солодовой вытяжки и крахмалом. В связи с этим необходимо ввести следующие поправки.
6.3.6 Определение поправки на солодовую вытяжку
Отобрать 12,5 см3 солодовой вытяжки в коническую колбу на 250 см3.
Прилить 37,5 см3 воды, 25 см3 раствора йода, 3 см3 раствора NaOH и выдержать 5 мин при комнатной температуре.
Добавить 4,5 см3 раствора H2SO4 и оттитровать избыток йода раствором Na2S2O3.
Поскольку в основном опыте в 50 см3 реакционной смеси содержится 1,25 см3 солодовой вытяжки, то при расчетах берут десятую часть найденной величины.
6.3.7 Определение поправки на раствор крахмала
25 см3 буферного раствора крахмала смешать в колбе с 10 см3 раствора йода.
Добавить 3 см3 раствора NaOH и выдержать 5 мин.
Подкислить смесь с помощью 4,5 см3 раствора H2SO4 и оттитровать раствором Na2S2O3.
6.3.8 Расчет амилолитической активности
Расчет амилолитической активности (в ед. W-K) ведется по формуле:
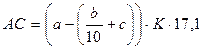
где a – количество 0,1н раствора йода, связанного в основном опыте, см3;
b – количество 0,1н раствора йода, связанного солодовой вытяжкой, см3;
c – количество 0,1н раствора йода, связанного раствором крахмала, см3;
K – коэффициент, учитывающий разбавление солодовой вытяжки (при использовании 10 г солода К=4, при 20 г К=2, при 40 г К=1);
17,1 – количество мг мальтозы, эквивалентное 1 см3 0,1н раствора йода.
В пересчете на сухое вещество солода амилолитическая активность рассчитывается по следующей формуле: 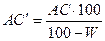 ,
,
где W – влажность свежепроросшего солода, %.
6.4 Контрольные вопросы
1)Ферменты. Общее понятие. Их роль в бродильной промышленности.
2)Амилолитические ферменты солода. Их характеристика.
3)Гидролиз крахмала под действием α-и β-амилаз.
4)В чем сущность определения амилолитической активности методом Виндиша-Кольбаха?
5)Физический смысл единицы Виндиша-Кольбаха (ед. W-K).
6)С какой целью и каким методом определяется массовая доля влаги в свежепроросшем солоде?
7)Как готовится солодовая вытяжка по методу Виндиша-Кольбаха?
8)С какой целью определяют поправки на раствор крахмала и солодовую вытяжку?
9)Опишите йодометрический метод определения мальтозы.
10)Назовите основные этапы определения амилолитической активности свежепроросшего солода методом Виндиша-Кольбаха.
7Лабораторная работа №5 «Вода в бродильной промышленности»
7.1 Цель работы: освоить методику определения жесткости воды комплексонометрическим методом, закрепить теоретический материал по выбору способов водоподготовки.
7.2 Теоретические сведения
Важное значение для нормального протекания технологических процессов имеет показатель жесткости воды, которая обусловлена содержанием в ней солей кальция и магния. Жесткость выражается в ммоль Са2+ или Mg2+, содержащихся в 1дм3 воды. Различают жесткость общую, временную, постоянную.
Общая жесткость характеризуется суммарным содержанием ионов кальция и магния. Она равна сумме временной и постоянной жесткости.
Временная (карбонатная, устранимая) жесткость обусловлена наличием в воде гидрокарбонатов кальция и магния. Эта жесткость исчезает при кипячении. Гидрокарбонаты превращаются в карбонаты, выпадающие в осадок.
Ca(HCO3)2 →CaCO3 ↓+ CO2 + H2O
Постоянная (некарбонатная, неустранимая) жесткость характеризуется присутствием в воде преимущественно сульфатов, хлоридов, нитратов и других солей кальция и магния, кроме гидрокарбонатов. При кипячении не выпадают в осадок.
С другой стороны жесткость можно подразделять на кальциевую и магниевую. Что показывает соответственно содержание в воде ионов кальция и ионов магния.
По жесткости вода классифицируется следующим образом:
очень мягкая – до 1,5 мг-экв/дм3;
мягкая – 1,5-3,0 мг-экв/дм3;
средней жесткости - 3,0-6,0 мг-экв/дм3;
жесткая - 6,0-10,0 мг-экв/дм3;
очень жесткая - более 10,0 мг-экв/дм3.
В соответствии с последними стандартами жесткость измеряют в градусах жесткости, соответствующих мг-экв/дм3.
Трудно переоценить значение показателя жесткости воды в бродильных производствах. Жесткая вода снижает ферментативную активность солода, влияет на выход экстракта и качество готового продукта в пивоварении. Повышенная жесткость воды может привести к перерасходу лимонной кислоты при производстве безалкогольных напитков, поскольку соли кальция и магния будут вступать в реакцию с кислотой. В ликероводочном производстве жесткость воды строго нормируется, т.к. при смешивании со спиртом растворимость солей кальция и магния снижается, и они выпадают в осадок, водно-спиртовая смесь становится мутной. Жесткая вода придает водке неприятный вкус. В зависимости от рН и щелочности воды жесткость выше 10оЖ может вызывать образование шлаков в распределительной системе водоснабжения и накипи при нагревании.
Таким образом, жесткая вода не пригодна для ряда производств и использования в котельных, поэтому такую воду умягчают.
Жесткость воды определяют комплексонометрическим методом либо методами атомной спектрометрии. При комплексонометрическом определении жесткости ионы алюминия, кадмия, свинца, железа, кобальта, меди, марганца, олова и цинка влияют на установление эквивалентной точки и мешают определению. Также определению могут помешать некоторые органические вещества. Если мешающее влияние устранить невозможно, рекомендуется проводить определение жесткости методами атомной спектрометрии.
Комплексонометрический метод определения жесткости воды основан на образовании комплексных соединений трилона Б с ионами щелочноземельных металлов. Определение проводят титрованием пробы раствором трилона Б при рН=10 в присутствии индикатора.
7.3 Определение жесткости воды комплексонометрическим методом
7.3.1 Посуда, реактивы, материалы: конические колбы на 250 см3, пипетки, бюретка; раствор сульфата магния (25 ммоль/дм3), буферный раствор (рН=10±0,1), индикатор эриохром черный Т, раствор трилона Б (25 ммоль/дм3); дистиллированная вода, анализируемая вода.
7.3.2 Установление коэффициента поправки к концентрации раствора трилона Б
В коническую колбу вместимостью 250 см3 вносят 10 см3 раствора ионов магния, добавляют 90 см3 дистиллированной воды, 5 см3 буферного раствора, 5-7 капель индикатора и титруют раствором трилона Б до изменения окраски от винно-красной до синей.
Раствор трилона Б в начале титрования добавляют довольно быстро при постоянном помешивании. Затем, когда цвет раствора начинает меняться, раствор трилона Б добавляют медленно. Эквивалентной точки достигают при изменении окрашивания, когда цвет раствора перестает меняться при добавлении капель раствора трилона Б.
Титрование следует проводить на фоне титрованной контрольной пробы. В качестве контрольной пробы можно использовать немного перетированную анализируемую пробу.
За результат принимают среднеарифметическое значение результатов не менее двух определений.
Коэффициент поправки К к концентрации раствора трилона Б вычисляют по формуле
К=10/V,
где V – объем раствора трилона Б, израсходованный на определение, см3; 10 – объем раствора ионов магния, см3.
7.3.3 Ход определения
Выполняют два параллельных определения.
В две колбы вместимостью 250 см3 помещают по 100 см3 анализируемой воды, по 5 см3 буферного раствора, по 5-7 капель раствора индикатора. Первую колбу титруют раствором трилона Б также, как описано в п.7.3.2. Во вторую колбу добавляют раствор трилона Б в количестве на 0,5 см3 меньше, чем пошло на первое титрование, быстро и тщательно перемешивают и аккуратно дотитровывают до достижения точки эквивалентности.
Жесткость воды Ж (оЖ) вычисляют по формуле
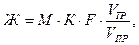
где М – коэффициент пересчета, равный 2 СТР (концентрация раствора трилона Б, моль/дм3); К – коэффициент поправки к концентрации раствора трилона Б; F – множитель разбавления анализируемой воды (F=1); VТР – объем раствора трилона Б, израсходованный на титрование, см3; VПР – объем пробы воды, взятой для анализа, см3.
За результат измерения принимают среднеарифметическое значение результатов двух определений при условии |Ж1-Ж2| ≤ 0,05 оЖ
Примечание
Нечеткое изменение окраски индикатора в эквивалентной точке или изменение окраски на серый цвет указывает на присутствие мешающих веществ.
В этом случае для уменьшения влияния содержащихся в воде цинка до 200 мг/дм3, алюминия, кадмия, свинца до 20 мг/дм3, железа до 5 мг/дм3, марганца, кобальта, никеля, меди до 1 мг/дм3 к аликвоте пробы до введения индикатора добавляют 2 см3 раствора сульфида натрия; для уменьшения влияния марганца до 1 мг/дм3, железа, алюминия до 20 мг/дм3, меди до 0,3 мг/дм3 добавляют 5-10 капель раствора гидроксиламина гидрохлорида.
Мутность пробы устраняют фильтрованием через бумажные обеззоленные фильтры «синяя лента».
7.4 Задание
При помощи лекционных материалов и дополнительной рекомендованной литературы [3] решить следующую задачу.
Требуется скорректировать показатели качества воды, поступающей из городского водопровода на производство ликероводочных изделий.
| Наименование показателя | Требования СанПиН и ТИ | Исходное значение |
| Цвет, град. | ||
| Запах | отс. | отс. |
| Мутность, мг/дм3 | 1,5 | 1,5 |
| рН | <7,8 | 6,9-7,4 |
| Сухой остаток, мг/дм3 | <500 | 260-510 |
| Общая жесткость, мг-экв/дм3 | <0,2 | 4,4-6,8 |
| Щелочность, мг-экв/дм3 | <4,0 | 3,1-4,8 |
| Железо, мг/дм3 | <0,15 | 0,7-1,4 |
| Окисляемость, мг О2/дм3 | <6,0 | 3,2-7,5 |
Подобрать способы и оборудование для водоподготовки для исправления качества воды. Ответ привести в виде технологической схемы водоподготовки с пояснениями.
7.5 Контрольные вопросы
1)Дайте определение жесткости воды.
2)Какие виды жесткости различают?
3)Как классифицируют воду по жесткости?
4)В каких единицах измеряют жесткость?
5)Какое значение имеет жесткость воды в бродильной промышленности?
6)Какими методами определяют жесткость воды? В каких случаях используют тот или иной метод?
7)В чем суть комплексонометрического метода определения жесткости воды?
8)Назовите способы умягчения воды.
9)Опишите комплексонометрический метод определения жесткости воды.
10)Присутствие каких веществ в воде создает помехи при определении жесткости комплексонометрическим методом? Как устранить влияние мешающих веществ?
8Лабораторная работа №6 «Определение содержания углеводов в продуктах, полуфабрикатах и сырье в бродильной промышленности»
8.1 Цель работы: познакомиться с методами определения углеводов продуктах, полуфабрикатах и сырье в бродильной промышленности, освоить методику определения сахаров в вине .
8.2 Теоретические сведения
В растительном сырье сухие вещества на 70-80% состоят из углеводов, и от полноты их использования зависит экономика производства. Основная масса углеводов представлена крахмалом или сахарами, которые и определяют ценность сырья. Так, расход сырья и выход готовой продукции зависят от исходного содержания в сырье крахмала или сахара. Контроль технологического процесса ведется также главным образом по углеводам: определяется полнота осахаривания крахмала, количество сахара на разных стадиях производства, концентрация сахара – один из основных показателей готовой продукции в винодельческой и ликероводочной промышленности.
Для количественного определения разных видов углеводов разработано много различных методов. По принципу действия их можно разбить на несколько групп:
1)поляриметрические методы, основанные на свойстве углеводов вращать плоскость поляризации поляризованного света.
Для анализа чистых сахаров этот метод является достаточно быстрым и точным, однако им нельзя определить какой-либо один сахар в присутствии других сахаров и оптически активных несахаров. При измерении угла вращения такой смеси получают алгебраическую сумму углов вращений право- и левовращающих веществ.
2)колориметрические методы, основанные на способности сахаров в сильно кислой среде превращаться в фурфурол или оксиметилфурфурол, которые с антроном и резорцином дают окрашенные соединения. При этом оптическая плотность раствора будет пропорциональна концентрации сахарного раствора, и измерив оптическую плотность раствора с помощью фотоэлектроколориметра, можно найти содержание сахара в растворе. В зависимости от применяемого реагента выделяют:
-антроновый метод (для определения альдоз – сахаров, содержащих альдегидную группу);
-резорциновый метод (для определения кетоз – сахаров, содержащих кетонную группу).
3)ферментативные методы, основанные на специфичности фермента катализировать только определенную химическую реакцию или разрывать строго определенную химическую связь.
4)химические методы, основанные на способности моносахаридов и некоторых более сложных сахаров окисляться оксидами тяжелых металлов.
В связи с тем, что оксиды металлов, окисляя сахар, сами восстанавливаются, сахара, способные восстанавливать окислители, называют редуцирующими. К редуцирующим сахарам относятся все моносахариды, а также мальтоза, мальтотриоза и некоторые другие продукты гидролиза крахмала. Однако истинное содержание сахаров химическими методами невозможно определить без предварительного гидролиза углеводов до моносахаров. Выделяют следующие химические методы:
-методы, основанные на реакции восстановления в щелочной среде оксида меди (II) в оксид меди (I) – метод Бертрана, метод Лейна и Эйнона (метод прямого титрования),
-методы, основанные на реакции восстановления в щелочной среде оксида железа (III) в оксид железа (II),
-методы, основанные на реакции восстановления в щелочной среде йода.
Группа методов, в которой для определения сахаров используются медьсодержащие растворы, применяется наиболее часто.
Щелочной раствор оксида меди (II) готовят по способу, разработанному Фелингом, чьим именем эта жидкость и названа.
Жидкость Фелинга получается при смешивании двух растворов: Фелинга I и Фелинга II. Фелинг I – это раствор сульфата меди, а Фелинг II – щелочной раствор тартрата калия-натрия (сегнетова соль). При смешивании этих растворов сначала образуется голубой осадок гидроксида меди:
CuSO4 + 2 NaOH = Cu(OH)2↓ + Na2SO4
Гидроксид меди сразу же вступает в реакцию с сегнетовой солью:
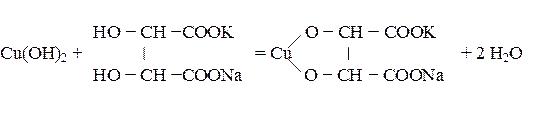
В результате реакции получается хорошо растворимое комплексное медьсодержащее соединение, интенсивно окрашивающее жидкость в темно-синий цвет. При нагревании в присутствии редуцирующего сахара двухвалентная медь комплексного соединения восстанавливается в одновалентную. Выделившийся при этом кислород окисляет сахар, а оксид меди (I) выпадает в виде красного осадка, количество которого эквивалентно количеству окислившегося сахара.
Однако процесс окисления в сильно щелочной жидкости Фелинга при высокой активности иона меди протекает сложно с образованием различных продуктов окисления, состав которых зависит от природы сахара, условий протекания анализа, концентрации раствора Фелинга, степени его щелочности и ряда других причин. Кроме того, при нагревании происходит частичное самопроизвольное восстановление меди фелинговой жидкости с образованием небольшого количества осадка Cu2O, а некоторое количество сахара разлагается под влиянием высокой щелочности среды.
По этим причинам для определения количества сахара приходится пользоваться специальными таблицами, составленными опытным путем для каждого метода.
8.3 Определение концентрации сахаров в виноматериале методом прямого титрования
8.3.1 Приборы, посуда, материалы: водяная баня, плитка электрическая, мерная колба на 100 см3, коническая колба, пипетки, бюретка, растворы Фелинга, раствор соляной кислоты (20%), раствор гидроксида натрия (20%), индикаторы фенолфталеин и метиленовый голубой, дистиллированная вода, виноматериал.
8.3.2 Подготовка к определению
При исследовании сладких вин необходимо предварительно их разбавить с таким расчетом, чтобы массовая концентрация сахара в испытуемом растворе была примерно 0,20-0,35 г в 100 см3.
В случае если содержание сахара определяется в темно окрашенном вине или виноматериале, вино осветляют с помощью уксуснокислого свинца (удаляют дубильные и красящие вещества). В случае сильных разбавлений (не менее чем в 10 раз) удаление дубильных и красящих веществ становится излишней операцией из-за малой их концентрации в разбавленном растворе.
Кроме того, устанавливают поправочный коэффициент к титру раствора Фелинга по раствору инвертного сахара с известной концентрацией.
Обычно в вине определяют содержание инвертного сахара (сумму глюкозы и фруктозы), для чего предварительно проводят инверсию.
Отмеряют 10 см3 вина и помещают в колбу на 100 см3. К вину приливают 5 см3 20%го раствора HCl и помещают на водяную баню температурой 67-690С на 5 минут. Затем раствор охлаждают, добавляют в него 2 капли фенолфталеина и приливают по капле из пипетки 20%ный раствор NaOH до появления розовой окраски. Доводят объем в колбе до метки. Содержимым колбы заполняют бюретку.
8.3.3 Ход определения
В коническую колбу налить по 5 см3 раствора Фелинга I и раствора Фелинга II. Поместить колбу на плитку и довести раствор до кипения. После этого добавить в раствор 3-5 капель индикатора метиленового голубого. Титровать фелинговую жидкость исследуемым раствором до исчезновения синей окраски индикатора и выпадения красного осадка.
Объем раствора, пошедшего на титрования, умножают на поправочный коэффициент фелинговой жидкости. По полученному значению по таблице в приложении В находят массу инвертного сахара в мг в 100 см3 раствора (m).
Концентрацию сахара X (г/дм3) в вине рассчитывают по формуле:
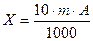 ,
,
где m – масса инвертного сахара в 100 см3 испытуемого раствора, найденная по таблице, мг; А – кратность разбавления вина; 10 – коэффициент пересчета объема испытуемого раствора на дм3; 1000 – коэффициент для перевода мг инвертного сахара в г.
За результат анализа принимают среднее арифметическое результатов двух параллельных определений.
8.4 Контрольные вопросы
1)Почему такой показатель как содержание углеводов имеет очень важное значение в бродильной промышленности? Поясните на примерах.
2)Перечислите и кратко охарактеризуйте группы методов определения содержания углеводов в сырье, полуфабрикатах и готовой продукции.
3)В чем суть колориметрических методов определения сахаров? Назовите методы определения сахаров, относящиеся к колориметрическим.
4)Как классифицируют химические методы определения сахаров?
5)На чем основаны химические методы?
6)Какие методы, основанные на реакции восстановления медьсодержащих растворов, вам известны?
7)В чем суть методов определения сахаров с помощью растворов Фелинга?
8)Почему для разных методов, использующих фелингову жидкость, составлены различные эмпирические таблицы?
9)Как и с какой целью удаляют дубильные и красящие вещества в темноокрашенном виноматериале при определении в нем сахаров методом прямого титрования?
10)Как определяют содержание сахаров в виноматериале методом прямого титрования?
9Лабораторная работа №7 «Точность методов и результатов измерений»
9.1 Цель работы: познакомиться с терминами точность, достоверность, сходимость и воспроизводимость метода, с основными видами погрешностей измерений, научиться анализировать точность проведенных измерений, познакомиться с основными правилами записи числовых значений при измерениях и расчетах.
9.2 Ошибки определения
Случайная ошибка – ошибки, приводящие к разбросу результатов, вызванные различными причинами (температура в лаборатории, сотрясение приборов, недостаточная чувствительность органов чувств наблюдателя и т.п.)
Случайную ошибку нельзя предотвратить, но можно уменьшить их последствия путем проведения большего количества параллельных определений
Систематическая ошибка – ошибка, оказывающая одинаковое влияние на все определения, меняя результат анализа на постоянную величину (например, по следующим причинам – неточно отградуированная шкала, неточная концентрация раствора реактива, температура раствора отлична от стандартной)
Систематическая ошибка устранима.
Грубая ошибка – следствие небрежного выполнения анализа.
Грубую ошибку можно устранить, лишь повторив определение.
Ошибки могут быть допущены на любой из стадий определения.
1)при отборе проб – негомогенная проба, перепутана проба, потери влаги в пробе при хранении и т.д.;
2)при использовании реактивов – реактивы низкого качества или с истекшим сроком хранения, вода, используемая для приготовления реактивов, низкого качества, перепутаны реактивы, концентрация реактивов неточная и т.д.;
3)при работе с оборудованием – прибор не откалиброван, использование неисправного прибора, несоблюдение правил эксплуатации и т.д.;
4)при работе с посудой – грязная посуда, неверное использование пипеток для дозирования, неточный объем аликвоты для определения и т.д.;
5)ошибки при расчетах – арифметические ошибки, не учтена влажность, не учтено разбавление пробы и т.д.
Абсолютная ошибка – разность между полученным результатом и истинным значением, выражается в тех же единицах, что и проводимое измерение.
Относительная ошибка – отношение абсолютной ошибки к истинному или среднему значению определяемой величины, выражается в процентах, дает более наглядное представление о точности анализа.
9.3 Точность и достоверность
Термин «точность» (точность метода) характеризует разброс результатов анализа вокруг установленного среднего значения.
Достоверным считается результат, если он принимает желаемое значение. Метод, обладающий хорошей точностью, не обязательно даст достоверные результаты (и наоборот), как показано на рисунке 9.1.
Точность метода характеризуется следующими метрологическими показателями:
-среднее арифметическое значение результатов серии определений,
-среднее квадратичное отклонение,
-коэффициент вариации,
-сходимость,
-воспроизводимость.
 |  |  |
| а) результаты достоверны, точность определения низкая, влияют случайные ошибки | б) точность определения хорошая, результаты не достоверны, влияет систематическая ошибка | в) точность и достоверность хорошие, ошибки отсутствуют |
| Рисунок 9.1 – Достоверность и точность измерений |
9.3.1 Анализ точности проведенного испытания
Анализ случайных погрешностей основывается на теории случайных ошибок, дающей с определенной гарантией вычислить действительные значения измеренной величины и оценить возможные ошибки.
Основу теории случайных ошибок составляют предположения:
-при большом числе измерений случайные погрешности одинаковой величины, но разного знака встречаются одинаково часто;
-при бесконечно большом числе измерений истинное значение измеряемой величины равно среднеарифметическому значению всех результатов измерений.
Среднее арифметическое:
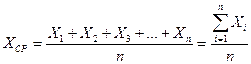
где ХСР – среднее арифметическое значение, Х1,2,3…n – значения результатов отдельных опытов, n – количество опытов.
Для характеристики разброса значений принято пользоваться средним квадратичным отклонением (σ):
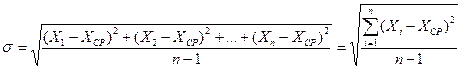
Для получения наглядного представления о существенности разброса вычисляется коэффициент вариации V.
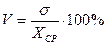
Коэффициент вариации обычно не превышает 45-50% и часто бывает гораздо ниже этого уровня.
В ряду отдельных измерений нередко появляется величина, резко отличающаяся от других. Эта выделяющаяся величина (очень маленькая или очень большая) может быть оценена с помощью критерия выпада Тв
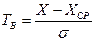
где Х – выделяющийся результат измерения, ХСР – среднее арифметическое значение без выделяющегося результата, σ – среднее квадратичное отклонение, подсчитанное также без выделяющегося результата.
Полученное значение критерия выпада сравнивают со стандартным значением критерия выпада Тст (эти значения приведены в таблице 9.1) в соответствии с числом определения n. При Тв>Тст выделяющийся результат исключают из обработки.
Таблица 9.1
| Общее число определений(n) | Тст | Общее число определений(n) | Тст | Общее число определений(n) | Тст |
| 77,96 | 3,17 | 2,86 | |||
| 11,46 | 3,12 | 2,85 | |||
| 6,53 | 3,08 | 2,84 | |||
| 5,04 | 3,04 | 2,83 | |||
| 4,36 | 3,01 | 2,82 | |||
| 3,96 | 2,98 | 2,81 | |||
| 3,71 | 2,95 | 2,80 | |||
| 3,54 | 2,93 | 2,74 | |||
| 3,41 | 2,91 | 2,68 | |||
| 3,31 | 2,90 | 2,63 | |||
| 3,23 | 2,88 | >120 | 2,58 |
Также для оценки среднего арифметического значения вычисляют ошибку среднего арифметического х
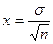
Величина ошибки среднего арифметического дает пределы, в которых может заключаться истинное значение среднего арифметического измеряемого показателя, которое с учетом ошибки составит ХСР±х.
Определение ошибки среднего арифметического имеет практическое значение при оценке результатов опытов и, в первую очередь, для установления надежности найденного среднего значения.
Критерием надежности среднего арифметического является Тн
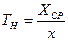
Если найденная величина Тн>3, то среднее арифметическое считается надежным. В случае, если Тн≤3, найденное среднее значение нельзя считать надежным.
9.3.2 Сходимость и воспроизводимость
Прецизионность – степень близости друг к другу результатов измерений, полученных в конкретных условиях.
Сходимость – прецизионность в условиях сходимости.
Условия сходимости – результаты измерений получаются одним и тем же методом на идентичных объектах испытаний, в одной и той же лаборатории, одним и тем же оператором, с использованием одного и того же оборудования в пределах достаточно короткого промежутка времени.
Воспроизводимость – прецизионность в условиях воспроизводимости.
Условия воспроизводимости – результаты измерений получены одним и тем же методом на идентичных объектах испытания в разных лабораториях, разными операторами, с использованием различного оборудования.
На практике, если используется гостируемый метод определения, в стандарте указывается допустимое расхождение между параллельными определениями (например, 0,2% при определении влажности зерна). В случае если расхождение между параллельными определениями больше, определение повторяют до тех пор, пока не будут достигнуты требуемые значения точности. Тогда за окончательный результат принимают среднее арифметическое между этими двумя значениями. Фактически этот показатель в ГОСТе (допустимое расхождение между определениями) характеризует сходимость. Также в стандарте обычно указывается допустимое расхождение между двумя результатами, полученными в разных лабораториях для одной и той же пробы. Эта величина характеризует воспроизводимость метода.
9.4 О количестве знаков в записях и при вычислении
Основное правило, которого нужно придерживаться при оформлении результата анализа, заключается в том, что точность результата определяется точностью метода или измерительных приборов и не может быть повышена за счет арифметических действий.
Критерием точности измерения является цена деления шкалы или десятая доля наименьшего деления шкалы. Результаты измерений записываются с таким количеством знаков, которое соответствует точности прибора, причем последний знак должен считаться сомнительным, а предпоследний точным.
Пример: если при титровании раствора пользуются бюреткой с ценой наименьшего деления 0,1 мл, то израсходованный на титрование объем раствора записывают с точностью до сотых долей, т.к. на глаз можно приблизительно отсчитать промежуточное между двумя делениями положение мениска. Но в этом случае последняя цифра считается сомнительной.
Все цифры, кроме нуля, считаются значащими. Нуль является значащим в тех случаях, когда он стоит между другими значащими цифрами и в правом конце числа, если он указывает, с какой точностью проводилось определение.
Пример: при взвешивании на аналитических весах навеска составила 0,3050 г. В этом числе нули между 3 и 5 и в конце числа значащие, поэтому запись 0,305 будет неверной, отбрасывать значащие нули в конце числа нельзя.
Если все определения проводились, например, с точностью до сотых долей, то результат вычислений нужно округлять также до сотых (даже если последняя цифра – нуль).
При выполнении арифметических действий над результатами измерений, проводившихся с различной точностью, в окончательном результате записывают столько знаков после запятой, сколько их имеется в наименее достоверном числе.
Пример: 197,1 + 106, 372 = 303,5.
Но при умножении приближенного числа на точное разряд последней цифры произведения одинаков с разрядом последней цифры исходного приближенного числа.
Пример: 3,2∙4=12,8 или 0,1∙12=1,2.
9.5 Задание
1) При определении кислотности в пробе пива получились следующие результаты (в см3 раствора NaOH концентрацией 0,1 моль/дм3 на 100 см3 пива):
2,2; 2,6(2); 2,5;2,7;3,4
Проанализируйте точность полученных результатов. Достоверны ли результаты?
2) Проанализируйте одну из выполненных ранее лабораторных работ на возможность систематических, случайных и грубых ошибок.
3) Составьте по выбранной лабораторной работе задачу на анализ точности полученных результатов. Решите эту задачу.
4)Сделайте выводы по данной работе.
9.5 Контрольные вопросы
1)Какие виды ошибок могут возникнуть при выполнении лабораторных определений?
2)Приведите примеры случайных ошибок.
3)Что такое систематическая ошибка? Приведите примеры?
4)Что подразумевает понятие «грубая ошибка»?
5)Как минимизировать воздействие вышеназванных ошибок на результат определения?
6)Что такое абсолютная и относительная погрешность? Какая из них дает более наглядное представление о точности опыта?
7)В каких случаях результаты опыта могут считаться достоверными?
8)Охарактеризуйте с помощью примера точность и достоверность результатов измерений.
9)Какими метрологическими показателями характеризуется точность проведенного испытания?
10)С какой целью при анализе точности результатов измерений определяют критерий выпада?
11)Что такое сходимость? Как этот показатель характеризует точность метода?
12)В каких случаях результаты определения считаются воспроизводимыми?
13)Что означает термин «прецизионность» по отношению к результатам измерений?
14)Назовите основные правила записи числовых значений при измерениях и расчетах. Приведите примеры.
Список рекомендуемой литературы
1)Грачев Ю.П. Математические методы планирования эксперимента / Ю.П. Грачев, Ю.М. Плаксина. – М.: ДеЛи принт, 2005
2)Великая Е.И. Лабораторный практикум по курсу общей технологии бродильных проиводств (общие методы контроля) / Е.И. Великая, В.Ф. Суходол. – М.: Легкая и пищевая пром-сть, 1983
3)Рябчиков Б.Е. Современные методы подготовки воды для промышленного и бытового использования / Б.Е. Рябчиков. – М.: ДеЛи принт, 2004
4)Таблицы для определения содержания спирта в водно-спиртовых растворах. – М.: Изд-во стандартов, 1979
5)ГОСТ 13586.5-93 Зерно. Метод определения влажности
6)ГОСТ Р 51619-2000 Алкогольная продукция и сырье для ее производства. Метод определения относительной плотности
7)ГОСТ Р 51653-2000 Алкогольная продукция и сырье для ее производства. Метод определения объемной доли спирта
8)ГОСТ Р 52407-2005 Вода питьевая. Методы определения жесткости
9)СТП 12570-2006 Общие требования к текстовым, графическим и программным документам.
Приложение А
Форма титульного листа отчета о лабораторной работе
Министерство образования и науки Российской Федерации
Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования
«Алтайский государственный технический университет
им. И.И. Ползунова»
Факультет (институт) _____________________________________________
Кафедра ________________________________________________________
наименование кафедры
Отчет защищен с оценкой__________
Преподаватель __________________
(подпись) (и.о.фамилия)
“____”___________ 20__ г.
Отчет
по лабораторной работе №____
___________________________________________
название лабораторной работы
по дисциплине _________________________________________
наименование дисциплины
_____________________________________________________
обозначение документа
Студент группы ___________________________________________________
и.о., фамилия
Преподаватель __________________________________________________
должность, ученое звание и.о., фамилия
БАРНАУЛ 20__
Приложение Б
Соотношение между относительной плотностью жидкости и
содержанием экстрактивных веществ
