Соляная кислота и хлороводород
Получают хлороводород таким образом:
1) слабое нагревание
NaCl + H  SO
SO  = NaHSO
= NaHSO  + HCl
+ HCl 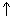
2) сильное нагревание
2NaCl + H  SO
SO  = Na
= Na  SO
SO  + 2HCl
+ 2HCl 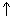
HCl – бесцветный газ с резким запахом, немного тяжелее воздуха, во влажном воздухе дымит. При 0 градусов в одном объеме воды растворяется 500 объемов хлороводорода.
Химические свойства соляной кислоты:
1ое свойство: изменяет окраску индикаторов: лакмус в соляной кислоте краснеет, метилоранж – розовеет, фенолфталеин остается бесцветным.
2ое свойство: взаимодействует с металлами:
Mg + 2HCl = MgCl  + H
+ H 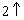
3е свойство: взаимодействует с основными оксиды:
Fe  O
O  + 6HCl = 2FeCl
+ 6HCl = 2FeCl  + 3H
+ 3H  O
O
Примечание: HCl + AgNO  = AgCl
= AgCl 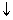 +HNO
+HNO 
Основания
CaO + H  O = Ca(OH)
O = Ca(OH) 
В этой реакции образовался гидрат оксида кальция, или гидроксид кальция. Основания состоят из металла и одновалентных гидроксильных групп (OH), число которых соответсвует валентности металла.
Основания:
NaOH – гидроксид натрия
Mg(OH)  - гидроксид магния
- гидроксид магния
Ba(OH)  - гидроксид бария.
- гидроксид бария.
Fe(OH)  - гидроксид железа (II)
- гидроксид железа (II)
Fe(OH)  - гидроксид железа (III)
- гидроксид железа (III)
Все основания имеют немолекулярное строение.
По растворимости в воде разделяются на:
А) растворимые (щелочи)
Пример: гидроксид натрия NaOH, гидроксид калия KOH, гидроксид бария Ba(OH)  и т.п.
и т.п.
Б) нерастворимые
Пример: гидроксид меди (II) Cu(OH)  , гидроксид железа (III)
, гидроксид железа (III)
Fe(OH)  и т.п.
и т.п.
Растворимые основания можно получить при взаимодействии активных металлов с водой и оксидов активных металлов с водой, которые называются основными оксидами:
2Na + 2H  O = 2NaOH + H
O = 2NaOH + H 
BaO + H  0 = Ba(OH)
0 = Ba(OH) 
Вывод: все основания реагируют с кислотами, образуя соль и воду.
Например:
NaOH + HNO  = NaNO
= NaNO  + H
+ H  O
O
Cu(OH)  + 2HCl = CuCl
+ 2HCl = CuCl  + 2H
+ 2H  O
O
Амфотерные оксиды и гидроксиды
Основания реагируют с кислотами и наоборот. Всегда получается соль и вода.
Ca(OH)  + 2HCl = CaCl
+ 2HCl = CaCl  + 2H
+ 2H  O
O
H  CO
CO  + 2NaOH = Na
+ 2NaOH = Na  CO
CO  + 2H
+ 2H  O
O
Есть такие хим. элементы, которые образуют оксиды и гидроксиды, обладающие двойственными свойствами – и основными и кислотными ( в зависимости от условий).
Это такие элементы как цинк, алюминий и др. Например:
Zn(OH)  + 2HCl = ZnCl
+ 2HCl = ZnCl  + 2H
+ 2H  O
O
 сильная
сильная  кислота
кислота
Zn(OH)  + 2NaOH = Na
+ 2NaOH = Na  ZnO
ZnO  + 2H
+ 2H  O
O
 сильное основание
сильное основание
Пример с оксидом цинка:
ZnO + 2HNO  = Zn(NO
= Zn(NO  )
)  + H
+ H  O
O
ZnO + 2KOH = K  ZnO
ZnO  + H
+ H  O (процесс сплавления)
O (процесс сплавления)
Способность химических соединений проявлять кислотные или основные свойства в зависимости от природы веществ, с которыми они реагируют, называется амфотерностью.
Zn(OH)  - амфотерный гидроксид
- амфотерный гидроксид
ZnO – амфотерный оксид
Соли
Соли – это сложные вещества, образованные атомами металлов и кислотными остатками.
Сумма единиц валентностей атомов металла должна равняться сумме единиц валентностей кислотного остатка.
Примеры солей:
NaCl - хлорид натрия
AgCl - серебра
K  S - сульфид калия
S - сульфид калия
NaNo  - нитрат натрия
- нитрат натрия
Mg(NO  )
)  - магния
- магния
Na  SiO
SiO  - силикат натрия
- силикат натрия
Al  (SO
(SO  )
)  - сульфат алюминия
- сульфат алюминия
Na  SO
SO  - натрия
- натрия
BaSO  - бария
- бария
Na  SO
SO  - сульфит натрия
- сульфит натрия
K  PO
PO  - фосфат калия
- фосфат калия
CaCO  - карбонат кальция
- карбонат кальция
Химические свойства солей
Соли реагируют:
А) с металлами:
Cu + 2AgNO  = Cu(NO
= Cu(NO  )
)  + 2Ag
+ 2Ag
Образуется новая соль и металл.
Примечание: реагируют с водой только те металлы, которые в вытеснительном ряду размещаются левее от того металла, который входит в состав соли.
Но для таких реакций нельзя брать очень активные металлы, типо Li, Na, K, Ca, Ba и т.п., которые реагируют с водой в н.у.
Б) с растворимыми основаниями (щелочами):
AlCl  +3NaOH = Al(OH)
+3NaOH = Al(OH) 
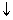 + 3NaCl
+ 3NaCl
K  SO
SO  + Ba(OH)
+ Ba(OH)  = 2KOH + BaSO
= 2KOH + BaSO 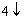
Образуется новая соль и новое основание.
Примечание: реагирующие вещества надо подбирать так, чтобы в результате реакции одно из образующихся веществ (основание или соль) выпадало в осадок.
В) с кислотами:
CaCo  + 2HCl = CaCl
+ 2HCl = CaCl  + H
+ H  CO
CO 
/ \
H  O CO
O CO 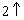
Образуется новая соль и новая кислота.
Поскольку H  CO
CO  очень непрочная, она разлагается на воду и CO
очень непрочная, она разлагается на воду и CO  .
.
Примечание: реакция между солью и кислотой будет происходить при таких условиях:
а) когда образуется осадок, не растворимый в кислотах:
AgNO  + HCl = AgCl
+ HCl = AgCl 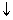 + HNO
+ HNO 
б) когда реагирующая кислота сильнее, чем та, которой образована соль:
Ca  (PO
(PO  )
)  + 3H
+ 3H  SO
SO  = 3CaSO
= 3CaSO 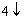 + 2H
+ 2H  PO
PO 
в) когда соль образована летучей кислотой, а реагирующая кислота нелетучая:
2NaNO  + H
+ H  SO
SO  = Na
= Na  SO
SO  + 2HNO
+ 2HNO 
Г) с солями:
BaCl  + Na
+ Na  SO
SO  = BaSO
= BaSO  + 2NaCl
+ 2NaCl
Примечание: реакция будет происходить только тогда, когда обе исходные соли будут взяты в растворах, но одна из вновь образующихся солей будет выпадать в осадок.
Выводы по всем этим темам ( с параграфа 29-38 ) и классификация неорганических веществ и их реакций: 
Ответы на некоторые вопросы после параграфов:
Какие вещества называют оксидами?
Оксиды – это сложные вещества образованные двумя элементами одним из которых является кислород.
Какие вещества относятся к кислотам?
К кислотам относятся сложные вещества, в состав которых входят водород и кислотный остаток.
Что называется реакцией соединения?
Это реакция в результате которой из двух или нескольких веществ (простых или сложных) образуется одно новое сложное вещество.
Напишите уравнения химических реакций которые происходят при таких превращениях: C 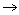 CO
CO 
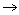 H
H  CO
CO 
P 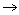 P
P  O
O 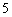
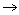 HPO
HPO 
C + O  = CO
= CO 
CO  + H
+ H  O = H
O = H  CO
CO 
P + O  = P
= P  O
O 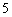
Как химическим путем отличить серебро от цинка?
Что такое хлороводород и как его получить?
Хлороводород – это бесцветный газ с резким запахом, немного тяжелее воздуха, во влажном воздухе “дымит”. Очень хорошо растворяется в воде. Получить хлороводород можно из кристаллического хлорида натрия NaCl при нагревании его с концентрированной серной кислотой.
Почему хлороводород на воздухе дымит?
Как доказать что выданный вам раствор кислота и это соляная кислота?
Надо юзить на него индикатором. Лакмус опустить – краснеет, метилоранж – розовеет, фенолфталеин – бесцветный.
Какие вещества относятся к основаниям и как их классифицируют? Привести примеры.
К основаниям относятся вещества имеющие гидроксильную группу и металл. Основания классифицируют на щелочи и нерастворимые.
Все металлы не растворяются, а неметаллы наоборот.
Растворимые – NaOH, KOH, нерастворимые – Cu(OH)  Fe(OH)
Fe(OH)  .
.
10) Что вам известно о гидроксиде натрия?
Гидроксид натрия NaOH – растворимый в воде…
11) Ca 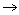 CaO
CaO  Ca(OH)
Ca(OH) 
 Ca(NO
Ca(NO  )
) 
2Ca + O  = 2CaO
= 2CaO
CaO + H  O = Ca(OH)
O = Ca(OH) 
Ca(OH)  + 2HNO
+ 2HNO  = Ca(NO
= Ca(NO  )
)  + 2H
+ 2H  O
O
12) P  P
P  O
O 
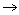 H
H  PO
PO 
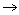 Mg(PO
Mg(PO  )
) 
4P + 5O  = 2P
= 2P  O
O 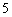

P  O
O 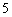 + 3H
+ 3H  O = 2H
O = 2H  PO
PO 
Что называется амфотерностью?
Амфотерность – это способность химических соединений
Проявлять кислотные или основные свойства в зависимости от природы веществ, с которыми они реагируют.
Что такое соли?
Соли – это сложные вещества, образованные атомами металлов и кислотными остатками.
Сформулируйте правило для составления формул солей.
Сумма единиц валентностей атомов металла должна равняться сумме единиц валентностей атомом кислотного остатка.
Ca 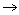 CaO
CaO 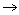 Ca(OH)
Ca(OH) 
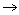 CaCl
CaCl 
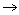 CaSO
CaSO 
2Ca + O  = 2CaO
= 2CaO
CaO + H  O = Ca(OH)
O = Ca(OH) 
Ca(OH)  + 2HCl = CaCl
+ 2HCl = CaCl  + 2H
+ 2H  O
O
CaCl  + H
+ H  SO
SO  = CaSO
= CaSO  + 2HCl
+ 2HCl
Ba 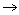 Ba(OH)
Ba(OH) 
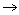 Ba(NO
Ba(NO  )
) 
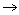 BaCO
BaCO 
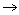 BaCl
BaCl 
Ba + H  O = Ba(OH)
O = Ba(OH) 
Ba(OH)  + 2HNO
+ 2HNO  = Ba(NO
= Ba(NO  )
)  + 2H
+ 2H  O
O
Ba(NO  )
)  + H
+ H  CO
CO  = BaCO
= BaCO  + 2HNO
+ 2HNO 
BaCO  + 2HCl = BaCl
+ 2HCl = BaCl  + H
+ H  CO
CO 
Обобщение знаний:
Какие вещества называются простыми? На какие две группы их можно разделить? Сравнить характерные свойства металлов и неметаллов.
Простые вещества – это вещества состоящие из одного элемента. Их можно разделить на металлы и неметаллы. Металлы – нерастворимые в воде вещества. Они имеют металлический блеск и пластичность. Неметаллы – это растворимые в воде вещества, которые хрупкие и т.п.
Какие вещества называются сложными? На какие классы делятся неорганические вещества?
Сложные вещества – это вещества состоящие из двух или более элементов. Неорганические вещества делятся на простые и сложные. Сложные делятся на оксиды, основания, кислоты и соли.
По какому признаку оксиды делят на основные и кислотные?
Оксиды которым соответствуют основания называют основными, а те которым соответствуют кислоты - кислотными.
21) С чем могут взаимодействовать кислотные и основные оксиды? Что получается?
Кислотные и основные оксиды могут взаимодействовать с водой и получается кислоты или основания.
Короче, об этом дальше.
Что такое основания? Какие элементы их образуют?
Какие свойства для них характерны?
Основания – это сложные вещества, состоящие из металла и гидроксильных групп. Их можно получить при Взаимодействии активных металлов с водой и оксидов активных металлов с водой. Щелочи хорошо растворимы в воде.
Некоторые очень едкие. Они разъедают кожу, бумагу и другие материалы. Их называют едкими щелочами.
Какие вещества называют кислотами? Какие элементы их
Образуют? Какие свойства для них характерны?
Кислотами называют сложные вещества в состав которых входят водород и кислотный остаток. Получить кислородосодержащие кислоты можно взаимодействовать кислотных оксидов с водой. Для них характерны свойства: многие кислоты при н.у. – жидкости, но есть твердые кислоты.
Они хорошо растворяются в воде. Почти все кислоты бесцветны.
Какие вещества относятся к солям? С какими веществами могут реагировать соли?
К солям можно отнести сложные вещества, образованные атомами металлов и кислотными остатками.
Какие продукты образуются во время взаимодействия:
А) основания и кислоты
Образуются соль и вода: NaOH + HCl = NaCl + H  O
O
Б) основного и кислотного оксидов
Образуется тоже самое что и дано.
В) основного оксида и кислоты?
Образуется соль и вода
Na  O + H
O + H  SO
SO  = NaSO
= NaSO  + H
+ H  O
O
Написать уравнения реакций.
Написать уравнения реакций получения фосфата кальция четырьмя способами.
26) Написать уравнения реакций получения гидроксида калия тремя способами.
Как осуществить следующие превращения:
Натрий – Гидроксид натрия – Сульфат натрия – Хлорид натрия – Нитрат натрия
Na + H  O = NaOH + H
O = NaOH + H 
NaOH + H  SO
SO  = NaSO
= NaSO  + H
+ H  O
O
NaSO  + HCl = HSO
+ HCl = HSO 
27) Что называется реакцией замещения и реакцией обмена?
Что с чем взаимодействует и что получается?
Основный оксид + кислота = соль + вода (обмен)
Оксид активных металлов + вода = щелочь (соединение)
Оксид неметаллов + вода = кислота (соединение)
Активные металлы + вода = гидроксид металлов (щелочь) + H 
Кислоты + металлы = соль + H 
Соляная кислота + металл = соль + H 
Соляная кислота + основный оксид = соль + вода (обмен)
Основания + кислота = соль + вода
Щелочи + оксид неметаллов = соль  + вода
+ вода
Соль + металл (не все) = новая соль + новый металл (обмен)
Соль + щелочь = новая соль + новое основание (обмен)
Соль + кислота = новая соль + новая кислота (обмен)
Кислотные оксиды – это оксиды неметаллов – это щелочи.
Читать полностью:http://www.km.ru/referats/EA89387A0A554F82A979EB356B9F7E4F#
