Физические свойства элементов главной подгруппы III группы
Электронное строение элементов главной подгруппы III группы
| Ат. номер | Название исимвол | Электроннаяконфигурация | Атомныйрадиус, нм. | ПИ, эВ | ЭО по Полингу | Степениокисления |
| Бор В | [Не]2s22р1 | 0,083 | 8,3 | 2,0 | +3 | |
| Алюминий Аl | [Nе]3s2Зр1 | 0,143 | 6,0 | 1,5 | +3 | |
| Галлий Gа | [Аr]3d104s24р1 | 0,122 | 6,0 | 1,6 | + 1, +3 | |
| Индий In | [Кr]4d105s25р1 | 0,163 | 5,8 | 1,7 | + 1, +3 | |
| Таллий Тl | [Хе]4f145d106s26р1 | 0,170 | 6,1 | 1,8 | + 1, +3 |
С увеличением атомной массы усиливается металлический характер элементов. Бор — неметалл, остальные элементы (подгруппа алюминия) — металлы. Бор значительно отличается по свойствам от остальных элементов и больше похож на углерод и кремний. Остальные элементы — легкоплавкие металлы, In и Тl — чрезвычайно мягкие.
Физические свойства элементов главной подгруппы III группы
| Элемент | Энергия связи, эВ | ρ, г/см3 | tпл, °C | tкип, °C |
| В | 5,83 | 2,34 | ||
| Аl | 3,38 | 2,70 | ||
| Gа | 2,87 | 5,91 | 29,8 | |
| In | 2,52 | 7,30 | ||
| Тl | 1,89 | 11,85 |
Все элементы группы трехвалентны, но с увеличением атомного номера более характерной становится валентность 1 (Тl преимущественно одновалентен).
В ряду В—Аl—Gа—In—Тl уменьшается кислотность и увеличивается основность гидроксидов R(ОН)3. Н3ВО3 — кислота, Аl(ОН)3 и Gа(ОН)3 — амфотерные основания, In(ОН)3 и Тl(ОН)3 — типичные основания. ТlOН — сильное основание.
Рассмотрим свойства только двух элементов: подробно — алюминия, как типичного представителя р-металлов, чрезвычайно широко применяемого на практике, и схематично — бора, как представителя «полуметаллов» и проявляющего аномальные свойства по сравнению со всеми другими элементами подгруппы.
Алюминий — самый распространенный металл на Земле (3-е место среди всех элементов; 8% состава земной коры). В виде свободного металла в природе не встречается; входит в состав глиноземов (Аl2О3), бокситов (Аl2О3 • xН2О). Кроме того, алюминий обнаруживается в виде силикатов в таких породах, как глины, слюды и полевые шпаты.
Содержание бора в земной коре составляет всего 0,001%. Его важнейшим природным минералом является бура Na2B4O7.10Н2О.
Алюминий имеет единственный стабильный изотоп 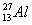 , бор — два:
, бор — два: 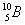 19,9% и
19,9% и 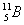 80,1%.
80,1%.
Получение ;
1. Электролиз расплава AlCl3:
2AlCl3 = 2Al + 3Cl2
2. Основной промышленный способ - электролиз расплава Al2O3 (глинозема) в криолите 3NaF • AlF3:
2Al2O3 = 4AI + 3O2
3. Вакуумтермический:
AlCl3 + ЗК = Al + 3KCl
Физические свойства.
Алюминий в свободном виде — серебристо-белый металл, обладающий высокой тепло- и электропроводностью. Алюминий имеет невысокую плотность — примерно втрое меньше, чем у железа или меди, и одновременно — это прочный металл.
Бор существует в нескольких аллотропных модификациях. Аморфный бор представляет собой темно-коричневый порошок. Кристаллический бор — серо-черный, с металлическим блеском. По твердости кристаллический бор занимает второе место (после алмаза) среди всех веществ. При комнатной температуре бор плохо проводит электрический ток; так же, как кремний, он обладает полупроводниковыми свойствами.
Химические свойства.
Поверхность алюминия обычно покрыта прочной пленкой оксида Аl2О3, которая предохраняет его от взаимодействия с окружающей средой. Если эту пленку удаляют, то металл может энергично реагировать с водой:
2Аl + 6Н2О = 2Аl(ОН)3 + ЗН2↑.
В виде стружек или порошка он ярко горит на воздухе, выделяя большое количество теплоты:
2Аl + 3/2O2 = Аl2О3 + 1676 кДж.
Это обстоятельство используется для получения ряда металлов из их оксидов методом алюмотермии. Так назвали восстановление порошкообразным алюминием тех металлов, у которых теплоты образования оксидов меньше теплоты образования Аl2О3, например:
Сr2О3 + 2Аl = 2Сr + Аl2О3 + 539 кДж.
Бор, в отличие от алюминия, химически инертен (особенно кристаллический). Так, с кислородом он реагирует только при очень высоких температурах (> 700°С) с образованием борного ангидрида В2О3:
2В + ЗО2 = 2В2О3,
с водой бор не реагирует ни при каких обстоятельствах. При еще более высокой температуре (> 1200°С) он взаимодействует с азотом, давая нитрид бора (служит для изготовления огнеупорных материалов):
2B + N2 = 2BN.
Лишь со фтором бор реагирует при комнатной температуре, реакции же с хлором и бромом протекают только при сильном нагревании (400 и 600 °С соответственно); во всех этих случаях он образует тригалогениды ВНal3 — дымящие на воздухе летучие жидкости, легко гидролизующиеся водой:
2В + 3Наl2 = 2ВНаl3.
В результате гидролиза образуется ортоборная (борная) кислота H3BO3:
ВНаl3 + 3Н2О = Н3ВО3 + ЗННаl.
В отличие от бора, алюминий уже при комнатной температуре активно реагирует со всеми галогенами, образуя галогениды. При нагревании он взаимодействует с серой (200 °С), азотом (800 °С), фосфором (500 °С) и углеродом (2000 °С):
2Аl + 3S = Аl2S3 (сульфид алюминия),
2Аl + N2 = 2АlN (нитрид алюминия),
Аl + Р = АlР (фосфид алюминия),
4Аl + 3С = Аl4С3 (карбид алюминия).
Все эти соединения полностью гидролизуются с образованием гидроксида алюминия и, соответственно, сероводорода, аммиака, фосфина и метана.
Алюминий легко растворяется в соляной кислоте любой концентрации:
2Аl + 6НСl = 2АlСl3 + ЗН2↑.
Концентрированные серная и азотная кислоты на холоде не действуют на алюминий. При нагревании алюминий способен восстанавливать эти кислоты без выделения водорода:
2Аl + 6Н2SО4(конц) = Аl2(SО4)3 + 3SО2 + 6Н2О,
Аl + 6НNO3(конц) = Аl(NO3)3 + 3NO2 + 3Н2О.
В разбавленной серной кислоте алюминий растворяется с выделением водорода:
2Аl + 3Н2SО4 = Аl2(SО4)3 + 3Н2.
В разбавленной азотной кислоте реакция идет с выделением оксида азота (II):
Аl + 4HNО3 = Аl(NО3)3 + NO + 2Н2О.
Алюминий растворяется в растворах щелочей и карбонатов щелочных металлов с образованием тетрагидроксоалюминатов:
2Аl + 2NаОН + 6Н2О = 2Na[Аl(ОН)4] + 3Н2↑.
Кислоты, не являющиеся окислителями, с бором не реагируют и только концентрированная HNO3 окисляет его до борной кислоты:
В + HNO3(конц) + Н2О = Н3ВO3 + NO↑
Соединения со степенью окисления +3. Важнейшими соединениями бора являются гидриды, галогениды, оксид, борные кислоты и их соли.
Оксид бора - B2O3 - бесцветная хрупкая стеклообразная масса, кислотный оксид, энергично присоединяет воду с образованием ортоборной кислоты:
B2O3 + 3H2O = 2H3BO3
H3BO3 - очень слабая одноосновная кислота, причем ее кислотные свойства проявляются не за счет отщепления катиона водорода, а за счет связывания гидроксид-аниона:
H3BO3 + H2O  H+ + [B(OH)4]-; рКа = 9,0
H+ + [B(OH)4]-; рКа = 9,0
При нагревании борная кислота ступенчато теряет воду, образуя вначале метаборную кислоту, а затем оксид бора:
- H2O - H2O
H3BO3 ¾® HBO2 ¾® B2O3
При взаимодействии со щелочами образует тетрабораты - соли гипотетической тетраборной кислоты:
4H3BO3 + 2NaOH = Na2B4O7 + 7H2O
Большинство солей – боратов – в воде нерастворимы, исключение составляют бораты s-элементов. Более других используется тетраборат натрия Na2B4O7. В большинстве своем бораты полимерны, выделяются из растворов в виде кристаллогидратов. Полимерных борных кислот из раствора выделить не удается, в связи с тем, что они легко гидратируются. Поэтому при действии кислот на полибораты обычно выделяется борная кислота (эта реакция используется для получения кислоты):
Na2B4O7 + H2SO4 + 5H2O = 4H3BO3 + Na2SO4
Безводные метабораты получают сплавлением оксида бора или борной кислоты с оксидами металлов:
CaO + B2O3 = Ca(BO2)2
Важнейшими соединениями алюминия является алюминий оксид и алюминий гидроксид.
Алюминий оксид Al2O3 - белая тугоплавкая кристаллической вещество, нерастворимое в воде. В лабораторных условиях алюминий оксид добывают сжигание алюминия или термическими разложением алюминий гидроксида:
4Al + 3O2 → 2Al2O3
2Al (OH) 3→ Al2O3 + 3H2O.
По химическим свойствам алюминий оксид являются амфотерными. Он реагирует с кислотами, проявляя свойства основных оксидов:
Al2O3 + 6HCl = 2AlCl3 + 3H2O.
Реагируйте со щелочами, он проявляет свойства кислотных оксидов. В растворах щелочей образуются комплексные соединения:
Al2O3 + 2KOH + 3H2O = 2K [Al (OH) 4].
При сплавления образуются соли метаалюминиевой кислоты, например, метаалюминат калия:
Al2O3 + 2KOH→2KAlO2 + H2O.
Естественную кристаллическую модификацию алюминий оксида (корунд) применяются в РАЗЛИчНЫХ областях науки и производства. Рубины, например, является материалом для изготовления рабочих камней точных механизмов. Кристаллы корунда - рабочие тела лазеров. Рубины и сапфиры используют для отделки ювелирных изделий. Алюминий оксид является главной составляющей наждака - абразивного материала. Тугоплавкость и коррозионная стойкость алюминий оксида предопределяет его применение для изготовления термостойких химической посуды, кирпича для кладки стекловаренных печей.
Алюминий гидроксид Al (OH) 3 - это нерастворимые в воде кристаллической вещество белого цвета. В лаборатории алюминий гидроксид добывают из растворимых солей алюминия при их взаимодействии с растворами щелочей, например:
AlCl3 + 3КOH = Al (OH) 3 ↓+ 3КCl.
Полученный алюминий гидроксид имеет вид студенистого осадка.
Алюминий гидроксид проявляет амфотерные свойства и растворяется как в кислотах, так и в щелочах:
Al (OH) 3 + 3HCl →AlCl3 + 3H2O
Al (OH) 3 + NaOH → Na [Al (OH) 4].
При сплавления алюминий гидроксида с натрий гидроксидом образуется натрий метаалюминат:
Al (OH) 3 + NaOH→ NaAlO2 + 2H2O.
Способность алюминий гидроксида реагировать с кислотами используют в терапии. Он входит в состав лекарственных препаратов, Которые используются для снижения кислотности и уменьшение изжоге.
Реакция с хлоридом бария. Борат-ионы при взаимодействии с хлоридом бария в водных растворах образуют белый кристаллический осадок метабората бария Ba(BO2)2
Аналитические реакции катиона алюминия Al3+
1. Реакция с щелочами:
А13+ + 3 ОН→А1(ОН)3↓ (белый)
2. Реакция с нитратом кобальта - образование -тенаровой сини.
-Тенаровая синь- - смешанный оксид алюминия и кобальта синего цвета.
2 A12(SO4)3 + 2 Co(NO3)2 —tT-> 2 Со(А1О2)2 + 4 NO2 + 6 SO3 + O2.
Бор относится к примесным микроэлементам, его массовая доля в организме человека составляет 10-5 %. Бор концентрируется главным образом в легких (0,34 мг), щитовидной железе (0,30 мг), селезенке (0,26 мг), печени, мозге (0,22 мг), почках, сердечной мышце (0,21 мг). Биологическое действие бора еще недостаточно изучено. Известно, что бор входит в состав зубов и костей, очевидно, в виде труднорастворимых солей борной кислоты с катионами металлов.
Избыток бора вреден для организма человека. Имеются данные, что избыток бора угнетает амилазы, протеиназы, уменьшает активность адреналина.
По содержанию в организме человека (10-5 %) алюминий относится к примесным микроэлементам. Алюминий концентрируется главным образом в сыворотке крови, легких, печени, костях, почках, ногтях, волосах, входит в структуру нервных оболочек мозга человека.
Суточное потребление алюминия человеком составляет 47 мг. Алюминий влияет на развитие эпителиальной и соединительной тканей, на регенерацию костных тканей, влияет на обмен фосфора.
Алюминий оказывает воздействие на ферментативные процессы.
Избыток алюминия в организме тормозит синтез ге–моглобина, так как благодаря довольно высокой комп-лексообразующей способности алюминий блокирует активные центры ферментов, участвующих в кроветво–рении. Имеются данные, что алюминий может катали–зировать реакцию трансаминирования.
Галлий – примесный микроэлемент (содержание в ор–ганизме человека 10?6—10?5%). Биологическая роль галлия в живых организмах почти не выяснена.
Таллий относится к весьма токсичным элементам. Даже весьма незначительные количества соединений Т1 + при попадании в организм вызывают выпадение волос.
В качестве противоядия при отравлении ионами Т1 используют серосодержащий лиганд – аминокислоту цистин.
