Скорость химических реакций и химическое равновесие. Катализ
Раздел химии, изучающий скорости химических процессов, называется химической кинетикой. Основной величиной химической кинетики является скорость химической реакции. Химические реакции протекают с различной скоростью: со взрывом и медленно. Скоростью химической реакции называется число элементарных актов реакции, происходящих в единицу времени в единице объема. Скорость химической реакции выражается изменением концентрации реагирующих веществ в единицу времени.
Скорость химической реакции зависит от ряда факторов. Важнейшими факторами, влияющими на скорость реакции, являются температура, давление, концентрация, катализатор и природа реагирующих веществ.
Критерием осуществления реакций является выполнение условия ΔGp,Т < 0.
Влияние концентрации. При взаимном столкновении активных молекул происходят химическое взаимодействие, число аффективных столкновений будет расти с увеличением концентрации, следовательно, будет возрастать и скорость реакции.
Закон действия масс, выражающий зависимость скорости от концентрации, читается так:
Скорость химической реакции прямо пропорциональна произведению концентраций реагирующих веществ, возведенных в степени их стехиометрических коэффициентов.
В общем виде для реакции типа mА+nВ=АВ
скорость выражается уравнением υ= k[A]m.[B]n,
где [А] и [В]- молярные концентрации веществ; k – константа скорости, зависящая от природы взаимодействующих веществ, катализаторов и температуры; m,n – стехиометрические коэффициенты в уравнении реакции.
При гетерогенных реакциях концентрации веществ, находящихся в твердой фазе, не включаются в уравнение заклна действия масс.
Пользуясь законом действия масс, можно вычислить скорость реакции в зависимости от концентрации реагирующих веществ.
Пример 1. Как изменится скорость реакции 2SO2+O2® 2SO3, если уменьшить объем газовой смеси в 3 раза?
Обозначим концентрации [SO2] и [O2] до изменения объема через a и b соответственно, тогда υ=k[SO2]2.[O2]=k.a2.b.
Вследствие уменьшения объема в 3 раза концентрации [SO2] и [O2] увеличились в 3 раза и стали SO2=3а и [O2] =3b. При новых концентрациях скорость реакции V1=k(3а)2. 3b= k27a2b.
Сравнивая υ и υ1, видим, что скорость реакции увеличилась в 27 раз.
Влияние температуры. Количественно эта зависимость может быть выражена эмпирическим правилом Вант-Гоффа: при повышении температуры на каждые 10оС скорость большинства химических реакций увеличивается в 2-4 раза. Число, показывающее, во сколько раз увеличивается скорость химической реакции при повышении температуры на 10оС, называется температурным коэффициентом скорости реакции и обозначается символом γ:
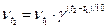
гдеυt1 и υt2– скорости реакции при температурах t1 и t2; γ-температурный коэффициент скорости реакции.
Пример 2. Во сколько раз увеличится скорость реакции при повышении температуры от 30 да 200оС, если температурный коэффициент скорости равен 2?
Подставляя значение в уравнение 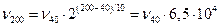 , получим
, получим
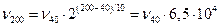
Скорость возрастает в 65000 раз.
Каждая химическая реакция характеризуется определенным энергетическим барьером; для его преодоления необходима энергия активации – некоторая избыточная энергия (по сравнению со средней энергией молекул при данной температуре), которой должны обладать молекулы для того, чтобы их столкновение было эффективным.
Энергия активации Еа связана с температурой уравнением Аррениуса: К = А∙е-Еа/RT.
Влияние катализатора. Одним из наиболее распространенных методов ускорения химических реакций является применение катализаторов.
Катализаторами называются вещества, изменяющие скорость реакции, но остающиеся после реакции химически неизменными и в первоначальном количестве.
Благодаря участию катализатора в химическом процессе увеличивается, дола активных молекул, и поэтому возрастает скорость реакции при положительном катализе.
Допустим, реакция А + В=АВ протекает очень медленно. Но вещество А хорошо взаимодействует c катализатором K, А + K = AK, а вещество AK хорошо взаимодействует с веществом B, образуя АB и К:АК + В = АВ + K. В результате реакций катализатор К остается без изменения. Катализатор – вещество, вcтупающее в промежуточное химическое взаимодействие с участниками реакции, но после каждого цикла промежуточных взаимодействий, восстанавливающее свой химический состав.
Пример 3.
1 реакция. Уравнение без катализатора идет очень медленно: O2 + NaSO3 = 2H2SO4 илиА+В=АВ.
2 реакция. С участием катализатора: О2 + 2NO = 2NO2 или А+К=АК.
Далее 2NO2+2H2SO3 = 2H2SO4 + 2NO или АК+В=АВ+К
Суммарное уравнение: O2 + 2NO + H2SO3 =H2SO4 +2NO, A+K+B=AB+K.
В результате оксид азота (II) остается без изменений. Катализаторы бывают положительными и отрицательными. Примеры отрицательных катализаторов: уротропин, униколь, мылонафт и др.
Явление изменения скорости реакции под действием катализаторов называется катализом; реакции, протекающие с помощью катализаторов – каталитическими.
Катализ бывает гомогенный и гетерогенный. При гомогенном катализе катализатор и реагирующие вещества образуют одну фазу; при гетерогенном – катализатор находится в системе самостоятельной фазой.
Химическое равновесие. Многие химические реакции протекают в противоположных направлениях. Когда скорости прямой и обратной реакции равны, то наступает химическое равновесие.
Например, для реакции СО + Н2= СО + Н2О прямой реакцией является реакция, идущая слева направо: υ1= k 1 [CO2].[H2], обратной реакцией – реакция, идущая справа налево (), то есть СО+Н2О « СО + Н2 , скорость υ2= k 2 [CO].[H2О].
При химическом равновесии и υ1= υ2 и k 1 [CO2].[H2]= k 2 [CO].[H2О]. Величины, k1 и k2 постоянны при данной температуре. Постоянным будет и их отношение. С наступлением химического равновесия реакция не прекращается, а между двумя взаимно противоположными процессами устанавливается подвижное (динамическое) равновесие, где К – константа химического равновесия:
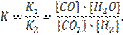
Если К>1, то равновесие сдвинуто влево, а при К<1 равновесие сдвинуто вправо.
Константа химического равновесия К изменяется только с изменением температуры и не зависит от концентраций реагирующих веществ. Она обозначает глубину протекания реакции. Концентрация отдельных составных частей системы, которая соответствует ее состоянию равновесия, принято называть равновесной концентрацией. Концентрации твердых веществ, участвующих в реакции, не входят в выражение константы равновесия. Например: СаСО3 = СаО+СО2, К= [CO2].
При изменении условий (температуры, давления и концентрации), в которых протекает обратимая реакция, нарушается химическое равновесие; это изменение называется смещением равновесия. Направление смещения равновесия определяется принципом Ле Шателье:
Если изменить одно из условий, при которых система находится в состояния химического равновесия (температуру, давление или концентрацию), то равновесие будет смещатся в направлении той реакции, которая противодействует произведенному изменению.
Согласно принципу Ле Шателье при повышении температуры равновесие смещается в сторону реакции, идущей с поглощением тепла; при повышении давления смещение равновесия будет направлено в сторону реакции, сопровождающейся уменьшением объема системы. Однако следует учесть, что, если реакция идет без изменения объема, то изменение давления не смещает равновесия, например:
N2 + O2 « 2NO + 49,2 кДж; I : I « 2.

 Пример 4. При состоянии равновесия системы 2NО + O2 « 2NO2 концентрация оксида азота (II) оказалась равной 0,056 моль/л, кислорода 0,028 моль/л, диоксида азота (IV) 0,044 моль/л. Вычислить исходные концентрации.
Пример 4. При состоянии равновесия системы 2NО + O2 « 2NO2 концентрация оксида азота (II) оказалась равной 0,056 моль/л, кислорода 0,028 моль/л, диоксида азота (IV) 0,044 моль/л. Вычислить исходные концентрации.
Решение
В первоначальный момент концентрация двуоксида азота равна 0. Каждый моль образуется из одного моля NO и 0,5 моль O2. Тогда для образования 0,044 моль/л NO2 в соответствии с уравнением реакции израсходовано 0,044 моль/л NOи 0,044/2 = 0,022 моль/л.
Исходные концентрации оксида азота и кислорода:
[NO]исх =[NO]р + 0,044=0,056+0,044=0,1 моль/л
[O2]исх =[O2]р + 0,022=0,028 + 0,022=0,05 моль/л.
Пример 5. Исходная концентрация йода [J2] равна 1 моль/л.
[Н2] = 2 моль/л. Вsчислить равновесные концентрации веществ при температуре 500°С, если К – константа химического равновесия реакции H2+J2 « 2HJ при этой температуре равна 50.
Решение
Обозначим число молей водорода, прореагировавшего к моменту наступления равновесия на каждый литр смеси, через X. Из уравнения реакции видно, что должно было одновременно прореагировать Х молей йода, тогда количество образовавшегося HJ будет равно 2Х:
Решая уравнение, получим: х = 0,93.
Равновесные концентрации: [J2]р= 0,07 моль/л, [Н2]р=1,07 моль/л.
Пример 6. Как отразится повышение давления на следующем равновесии: СО2 +Ств. = 2СО?
Решение
Повышение давления вызовет смещение равновесия влево, т.е. в сторону процесса, идущего с уменьшением количества реагирующего вещества.
КОНТРОЛЬНЫЕ ВОПРОСЫ И ЗАДАНИЯ
91. Как изменится скорость реакции образовании NO N2+O2=2NO, если объем газовой смеси уменьшить в 2 раза?
92. Как возрастают скорости реакции при повышении температуры от 50 до 100оС, если температурный коэффициент реакции равен 2?
93. Константа равновесия для реакции 2N2+O2=2N2O составляет 1,21. Равновесные концентрации были: [N2]=0,72 моль/л, [N2O]=0,84 моль/л. Найти исходную концентрацию кислорода.
94. Константа равновесия гомогенной системы CO – HO =CO – H при 850оС равна 1. Вычислите концентрации всех веществ при равновесии, если исходные концентрации были: [CO]исх=3 моль/л, [HO]исх=2 моль/л. (ответы: [CO]р = 1,8 моль/л ; [HO]р = 0,8 моль/л).
95. В какую сторону при понижении температуры будут смещаться равновесия следующих систем:
| 2NO +O2 « N2O4+Q, 2CO+O2 « 2CO2+Q, C+H2O « CO+H2 – Q, | N2+3H2 « 2NH3+Q, COCl2 « CO+Cl2 –Q, N2+O2 « 2NO – Q? |
96. Напишите выражение для скорости прямой и обратной реакции каждого из следующих процессов: а) N2+O2 « 2NO; б) N2+3H2 « 2NH3; в) CO+Cl2 « COCl2. Вычислите, во сколько раз увеличатся или уменьшатся скорости этих реакций, если при неизменной температуре: а) уменьшить концентрацию каждого вещества в 2 раза; б) увеличить давление в 3 раза.
97. Во сколько раз возрастает скорость химической реакции при повышении температуры от 20 до 120оС (температурный коэффициент реакции равен 2).
98. 
 Вычислите константу химического равновесия реакции 2NO+ O2 « 2NO2 и исходные концентрации NO и O2, если при химическом равновесии концентрации были: [NO]р = 0,004 моль/л , [O2]р = 0,04 моль/л, [NO2]р = 0,004 моль/л.
Вычислите константу химического равновесия реакции 2NO+ O2 « 2NO2 и исходные концентрации NO и O2, если при химическом равновесии концентрации были: [NO]р = 0,004 моль/л , [O2]р = 0,04 моль/л, [NO2]р = 0,004 моль/л.
99. Константа равновесия реакции FeO+CO « CO2+F равна 0,5. Найти равновесные концентрации оксида (II) и диоксида углерода (IV), если начальная концентрация [CO] равна 0,1 моль/л; [CO2] =0,02 моль/л.
100. Как изменится скорость прямой реакции N2+3H2 « 2NH3, если при неизменной температуре в 2 раза повысить давление?
101. Вычислите температурной коэффициент реакции, зная, что с повышением температуры на 70оС скорость реакции возрастает в 128 раз.
102. Константа равновесия обратимой реакции, протекающей по уравнению CO+H2O « H2+CO2, при некоторой температуре равняется 1. При состоянии равновесия концентрация веществ были: [H2O]р=0,03 моль/л; [CO]р=0,04 моль/л. Вычислите исходную концентрацию [CO2]. (Ответ: 0,093 моль/л).
103. Сколько времени будет протекать реакция при температуре: a) 200°C, б) 100°С, если известно, что при 160°С она заканчивается за 100 мин? Температурный коэффициент равен 2.
104. Константа скорости реакции 3 А + 2 В « С равна 0,4. Начальная концентрация вещества А равна 0,3 моль/л, вещества В-0,5 моль/л. Найдите начальную скорость реакции и скорость реакции по истечении некоторого времени, когда концентрация вещества А уменьшилась на 0,060 моль/л.
105. Рассчитайте константу равновесия для реакции CH4+2O2 « CO2+2H2O, если известно, что исходные концентрации [CH4] =3 моль/л, [O2]=4 моль/л и что к моменту равновесия прореагировало 50% кислорода.
106. Определите, как будет влиять увеличение температуры и давления на состояние равновесия в следующих реакциях:
N2+O2 « 2NO – Q, N2+3H2 « 2NH3+Q,
H2+Cl2 « 2HCl+Q, CO+H2O « CO2+H2 – Q.
107. Во сколько раз возрастет скорость химической реакции при повышении температуры с 10 до 400С, если известно, что с повышением температуры на 100С скорость химической реакции возрастет в 2 раза?
108. Равновесие гомогенной системы 4HCI(г)+O2(г)= 2H2O(г)+2CI2(г) установилось при следующих концентрациях реагирующих веществ: [H2C]p = 0,14моль/л; [CI2]p = 0,14 моль/л; [HCI]p= 0,20 моль/л; [О2]p= 0,32 моль/л. Вычислите исходные концентрации хлористого водорода и кислорода. (Ответы: [HCI]исх = 0,28 моль/л; [О2]исх = 0, 39 моль/л.)
109. Обратимая реакция идет согласно уравнению 3А+2В ↔С + 2D. Константа равновесия равна 1/3. Вычислите равновесные концентрации веществ [A], [В], [С], [D] в моль/л, если начальные концентрации были [А] = 2 моль/л, [В] = 4 моль/л.
110. С учетом увеличения давления покажите, как сместится равновесие при каждом из указанных случаев:
NO2↔N2O4, 2NO2↔2NO+O2, 3H2+N2↔2NH3, FeO+H2↔Fe+H2O(г). Напишите выражение константы равновесия.
