Строение атома. Химическая связь
1. Массовое число атома равно:
а) числу электронов;
б) числу протонов;
в) числу нейтронов;
г) числу нуклонов.
2. Изотопы – это разновидности атомов одного и того же элемента, которые отличаются друг от друга:
а) числом протонов;
б) числом электронов;
в) числом электронных слоёв;
г) атомной массой.
3. Изотопы одного элемента содержат одинаковое количество:
а) электронов;
б) нейтронов;
в) нуклонов;
г) протонов
4. Какие из перечисленных нуклидов являются изотопами по отношению друг к другу?
а) 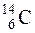 ;
;
б) 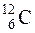 ;
;
в) 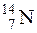 ;
;
г) 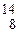 О.
О.
5. Для радиоактивного нуклида период полураспада – это время, за которое разрушается:
а) один его атом;
б) половина имеющихся атомов;
в) четвертая часть имеющихся атомов;
г) все имеющиеся атомы.
6. Сколько в сумме протонов, электронов и нейтронов содержится в атоме нуклида 40К?
а) 52;
б) 56;
в) 59;
г) 61.
7. Изотопами являются:
а) нуклиды, имеющие одинаковые массовые, но разные протонные числа;
б) нуклиды, имеющие одинаковые протонные, но разные массовые числа;
в) нуклиды, содержащие одинаковое число нейтронов в ядре;
г) нуклиды, содержащие одинаковое число нейтронов и электронов.
8. Период полураспада радиоактивного нуклида – это время, за которое распадается:
а) 10% имеющихся атомов;
б) 25% имеющихся атомов;
в) 50% имеющихся атомов;
г) 75% имеющихся атомов.
9. Укажите относительную массу атома, содержащего 19 электронов и 21 нейтрон:
а) 38;
б) 39;
в) 40;
г) 42.
10. Главное квантовое число всегда указывает на:
а) количество электронных слоев в атоме;
б) номер электронного слоя в атоме по мере удаления от ядра;
в) номер периода, в котором данный атом расположен в таблице элементов Д.И.Менделеева;
г) номер группы, в которой данный атом расположен в таблице элементов Д.И.Менделеева.
11. Орбитальное квантовое число l для электронов, расположенных на f-подуровне 5-го энергетического уровня, равно:
а) 2;
б) 3;
в) 4;
г) 5.
12. Возможное значение магнитного квантового числа ml для электрона, расположенного на d-подуровне 4 энергетического уровня, равно:
а) –3;
б) –2;
в) +1;
г) +4.
13. Возможное значение магнитного квантового числа ml для электрона, расположенного на 7р-подуровне, равно:
а) –3;
б) 0;
в) +2;
г) +7.
14. Число электронных орбиталей на внешнем электронном слое у атома элемента, расположенного в 3 периоде таблицы Д.И. Менделеева, равно:
а) 3;
б) 6;
в) 8;
г) 9.
15. Наибольшее число атомных орбиталей содержится на:
а) р-подуровне;
б) s-подуровне;
в) f-подуровне;
г) d-подуровне.
16. Порядок заполнения электронами орбиталей с одинаковым значением главного и орбитального квантовых чисел определяется:
а) правилами Клечковского;
б) правилом Вант – Гоффа;
в) правилом Хунда;
г) правилом Ле – Шателье.
17. Порядок заполнения электронами подуровней с разными значениями суммы главного и орбитального квантовых чисел определяется:
а) первым правилом Клечковского;
б) вторым правилом Клечковского;
в) правилом Хунда;
г) правилом Панета – Фаянса.
18. Порядок заполнения электронами подуровней с одинаковыми значениями суммы главного и орбитального квантовых чисел определяется:
а) принципом Паули;
б) первым правилом Клечковского;
в) вторым правилом Клечковского;
г) правилом Ле – Шателье.
19. Общее число электронов в молекуле серы равно 128. Сколько атомов серы входит в состав ее молекулы:
а) 6;
б) 8;
в) 9;
г) 10.
20. Какие частицы имеют такую же электронную конфигурацию, как и атом Кr?
а) Вr-;
б) Cl-;
в) Rb+;
г) Sr2+.
21. Какие из приведенных электронных конфигураций атомов или ионов невозможны в принципе?
а) 1s22s22p42d1;
б) 1s22s22p63s13p33d4;
в) 1s22s23s13p73d104s1;
г) 1s22s22p63s23p63d9.
22. На какой орбитали электрон будет обладать наибольшей энергией?
а) 4f;
б) 5s;
в) 5р;
г) 4d.
23. Какое максимальное число электронов может содержаться на четвертом энергетическом уровне?
а) 24;
б) 32;
в) 48;
г) 56.
24. Анион Э2- некоторого элемента имеет электронную конфигурацию 1s22s22p63s23p6. Сколько протонов содержат ядра атомов этого элемента?
а) 15;
б) 16;
в) 17;
г) 18.
25. На какой орбитали электрон будет обладать наименьшей энергией:
а) 5s;
б) 4d;
в) 4f;
г) 5р.
26. Энергетическим уровнем называется совокупность электронов в атоме, имеющих:
а) одинаковые главные квантовые числа;
б) близкое значение энергии;
в) одинаковое значение спинового квантового числа;
г) одинаковое значение орбитального квантового числа.
27. Атому какого элемента соответствует данная электронная конфигурация 1s22s22p63s13p3?
а) фосфора;
б) кремния;
в) серы;
г) азота.
28. Электронная формула иона Ве2+ выглядит следующим образом:
а) 1s22s2;
б) 1s22s22p2;
в) 1s2;
г) 1s22s1.
29. Электронная конфигурация хлорид-иона имеет вид:
а) 1s22s22p5;
б) 1s22s22p63s23p4;
в) 1s22s22p63s23p5;
г) 1s22s22p63s23p6.
30. Электронная формула иона S2– имеет вид:
а)…3s23p4;
б) …3s23p6;
в) …3s23p2;
г) …3s23p1.
31. Какие электронные формулы принадлежат элементам-металлам?
а) 1s22s1;
б) …3s13p1;
в) 1s22s22p3;
г) …3s23p4.
32. Какие из перечисленных элементов являются s-элементами?
а) калий;
б) серебро;
в) бериллий;
г) цинк.
33. Какие электронные формулы принадлежат р-элементам?
а) 1s22s22p3;
б) … 3s23p4;
в) …3s23p33d1;
г) …3s13p1.
34. Какие электронные формулы принадлежат s-элементам:
а) 1s22s1;
б) 1s22s22p63s13p1;
в) 1s22s22p1;
г) 1s22s22p5.
35. Какие электронные формулы соответствуют невозбужденному состоянию атома?
а) …3s23p43d1;
б) …3s23p63d14s2;
в) … 3s23p6;
г) …3s23p63d24s14p1.
36. Возбужденному состоянию атома хлора соответствует электронная конфигурация:
а) 1s22s22p63s23p43d1;
б) 1s22s22p63s23p5;
в) 1s22s22p63s23p33d2;
г) 1s22s22p63s13p33d3.
37. Возбужденному состоянию атома серы соответствует электронная конфигурация:
а) 1s22s22p63s23p4;
б) 1s22s22p63s23p33d1;
в) 1s22s22p63s13p33d2;
г) 1s22s22p63s23p6.
38. Какие электронные формулы соответствуют возбужденному состоянию атома?
а) …3s23p43d1;
б) …3s23p63d14s2;
в) … 3s13p2;
г) …3s2 3p63d24s14p1.
39. Порядковый номер элемента в таблице Менделеева соответствует:
а) высшей валентности элемента;
б) числу электронов в его атомах;
в) числу нейтронов в ядрах его атомов;
г) числу протонов в ядрах его атомов.
40. Электроотрицательность элементов в периодической системе Д.И. Менделеева:
а) возрастает в периоде слева направо;
б) уменьшается в периоде слева направо;
в) возрастает в группе сверху вниз;
г) уменьшается в группе сверху вниз.
41. В периодах слева направо:
а) увеличивается энергия ионизации атомов;
б) уменьшается энергия ионизации атомов;
в) атомные радиусы увеличиваются;
г) атомные радиусы уменьшаются.
42. Энергия сродства к электрону увеличивается:
а) в периодах слева направо;
б) в группах сверху вниз;
в) в периодах справа налево;
г) в группах снизу вверх.
43. У элементов, входящих в состав одной и той же А группы одинаково:
а) число энергетических уровней;
б) число электронов на внешнем электронном слое;
в) величина заряда атомного ядра;
г) низшая степень окисления.
44. Основные свойства сильнее всего выражены у гидроксида:
а) Ве (ОН)2;
б)Mg (ОН)2;
в) Са (ОН)2;
г) Ва (ОН)2.
45. Наиболее сильно кислотные свойства выражены у:
а) H2SiO3;
б) H3PO4;
в) H2SO4;
г) HClO4.
46. Номер периода всегда указывает для расположенных в нем элементов на:
а) число электронов на внешнем электронном слое их атомов;
б) число электронных слоев в их атомах;
в) число подуровней на внешнем электронном слое их атомов;
г) число вакантных орбиталей на внешнем электронном слое их атомов.
47. Номера А-групп в таблице Д.И. Менделеева указывают для расположенных в них элементов на:
а) число электронных слоев в атоме;
б) число электронов на внешнем слое атома;
в) число электронов в атоме;
г) число протонов в ядре атома.
48. Химические элементы, образующие летучие водородные соединения состава H2R, входят в:
а) II A группу;
б) III A группу;
в) V A группу;
г) VI A группу.
49. Химические элементы, образующие высшие оксиды состава R2O7, могут входить в:
а) VB группу;
б) VIIA группу;
в) VIIB группу;
г) VIB группу.
50. Элемент, образующий оксид состава R2O3, может входить в:
а) VA группу;
б) VIA группу;
в) IIIA группу;
г) IIIB группу.
51. Радиусы атомов в А группах сверху вниз:
а) закономерно уменьшаются;
б) закономерно увеличиваются;
в) сначала уменьшаются, а потом увеличиваются;
г) не изменяются.
52. Период в таблице Д.И.Менделеева образуют элементы:
а) проявляющие одинаковые химические свойства;
б) проявляющие в соединениях одинаковую высшую в валентность, равную номеру периода;
в) имеющие одинаковое число энергетических уровней у своих атомов;
г) содержащие на внешнем электронном слое одинаковое число электронов, равное номеру периода.
53. А-группы в полудлинном варианте таблицы Д.И. Менделеева объединяют элементы:
а) имеющие одинаковые значения электроотрицательности;
б) заполняющие электронами s- или р-подуровень внешнего слоя;
в) принадлежащие только к неметаллам;
г) валентные электроны которых расположены только на внешнем электронном слое.
54. В-группы в полудлинном варианте таблицы Д.И. Менделеева объединяют элементы:
а) имеющие одинаковые значения энергии ионизации;
б) принадлежащие как к металлам, так и к неметаллам;
в) заполняющие электронами d-подуровень предвнешнего электронного слоя;
г) валентные электроны которых расположены как на внешнем, так и на предвнешнем слое.
55. У d- и f-элементов с увеличением порядкового номера:
а) не увеличивается величина заряда ядра атома;
б) на внешнем электронном слое атомов не изменяется число электронов;
в) на внешнем электронном слое атомов уменьшается число электронов;
г) не изменяется атомная масса.
56. В периоде с увеличением порядкового номера элемента наблюдается:
а) увеличение атомного радиуса и уменьшение энергии сродства к электрону;
б) увеличение энергии ионизации и энергии сродства к электрону;
в) уменьшение атомного радиуса и уменьшение значения электроотрицательности;
г) увеличение значения электроотрицательности и увеличение энергии сродства к электрону.
57. В группе с увеличением порядкового номера элемента наблюдается:
а) уменьшение энергии ионизации и уменьшение атомного радиуса;
б) уменьшение энергии сродства к электрону и уменьшение электроотрицательности;
в) увеличение атомного радиуса и увеличение энергии ионизации;
г) увеличение значения электроотрицательности и энергии сродства к электрону.
58. Элемент, образующий твердое водородное соединение вида ЭН2, может входить в:
а) VI А группу;
б) VI В группу;
в) II А группу;
г) III В группу.
59. По номеру группы, в которой находится химический элемент, можно определить:
а) число энергетических уровней в его атоме;
б) число энергетических подуровней на внешнем электронном слое его атома;
в) возможные значения валентности и степени окисления его атомов в соединениях;
г) формулу его высшего оксида.
60. Какой период в таблице Д.И. Менделеева образован только s-элементами?
а) седьмой;
б) первый;
в) второй;
г) никакой.
61. В состав каких периодов могут входить d-элементы?
а) первого;
б) третьего;
в) пятого;
г) седьмого.
62. Электронная формула внешнего электронного слоя у атома элемента, образующего оксид состава R2О, может иметь следующий вид:
а) ns1;
б) ns2nр5;
в) 2s22р3;
г) ns2nр4.
63. Электронная формула внешнего электронного слоя у атома элемента, образующего оксид состава R2О3, может иметь следующий вид:
а) ns2;
б) ns2nр1;
в) ns2nр3;
г) ns2nр4.
64. Элементы какой группы проявляют одинаковую валентность в летучих водородных соединениях и высших оксидах?
а) II А;
б) IV А;
в) V А;
г) III В.
65. Высший оксид элемента имеет формулу RО2. Какова будет формула его летучего водородного соединения?
а) Н2R;
б) RН2;
в) RН4;
г) RН.
66. Формула летучего водородного соединения, которое образует данный элемент RН2. Какова будет формула его высшего оксида?
а) RО2;
б) R2О;
в) RО3;
г) RО4.
67. Электроотрицательность элемента – это:
а) энергия, которую необходимо затратить, чтобы присоединить к внешнему электронному слою его атома 1 электрон;
б) условная величина, характеризующая способность его атомов притягивать к себе электроны в химических соединениях от других атомов;
в) энергия, которая выделяется при образовании атомом ковалентной химической связи;
г) энергия, которая выделяется при отрыве от атома одного электрона.
68. Атомы элемента в возбужденном состоянии имеют
следующую электронную конфигурацию 1s22s22p63s23p63d104s14p34d1. Формула летучего водородного соединения этого элемента:
а) RH2;
б) RH;
в) RH3;
г) RH4.
69. Суммарное количество электронов у атома элемента, находящегося в возбужденном состоянии, равно 53. Формула высшего оксида, который образует данный элемент:
а)R2О3;
б) R2О5;
в) R2О7;
г) RО4.
70. Отметьте верные характеристики для химического элемента с атомным номером 33:
а) данный элемент является неметаллом;
б) его электронная формула в возбужденном состоянии 1s22s22p63s23p63d104s24p3;
в) формула его высшего оксида R2О5;
г) в соединениях он может проявлять только положительную степень окисления.
71. К какой группе относится элемент, катион которого Э2+ имеет электронную конфигурацию 1s22s22p63s23p63d9?
а) II A;
б) V B;
в) I В;
г) VIII В.
72. К какому периоду относится элемент, катион которого Э3+ имеет следующую электронную конфигурацию 1s22s22p63s23p63d104s24p6?
а) 3;
б) 4;
в) 5;
г) 6.
73. Масса всех электронов у атома элемента равна 2,639∙10-26 г. В какой группе находится данный элемент, если известно, что масса одного электрона равна 9,1∙10-31 кг?
а) II A;
б) V B;
в) I В;
г) III A.
74. Масса всех электронов у аниона элемента вида Э-2 равна 4,914∙10-26 г. В какой группе находится данный элемент, если известно, что масса одного электрона равна 9,1∙10-31 кг?
а) V B;
б) VI А;
в) III A;
г) IV B.
75. В какой массе меди содержится 1 г электронов, если известно, что масса одного электрона равна 9,1·10-31кг?
а)3,26кг;
б) 4,002 кг;
в) 4,032 кг;
г) 4,324 кг.
76. В каком ионе степень окисления фосфора равна «+5»?
а) Н2Р2О72-;
б) НРО32-;
в) РО3-;
г) НРО42-.
77. В каком ионе хром проявляет максимальную степень окисления?
а) СrО42-;
б) НСr2О7-;
в) Сr(ОН)2+;
г) Сr3+.
78. Отметьте формулы молекул, в которых атом неметалла находится в состоянии sр3 - гибридизации:
а) NН3;
б) Н2О;
в) ВF3;
г) С2Н4.
79. В молекулах каких веществ имеются атомы, находящиеся в состоянии sр-гибридизации?
а) ВеСl2;
б) ССl4;
в)С2Н4;
г) С6Н6.
80. Атомы каких элементов могут являться акцепторами электронных пар?
а) Nе;
б) Аl;
в) F;
г) Сu.
81. Атомы каких элементов могут являться донорами электронных пар?
а) Не;
б) Li;
в) О;
г) Nа.
82. Механизм образования химической связи за счет неподеленной пары электронов одного атома и свободной орбитали другого атома называется:
а) обменным;
б) ионным;
в) донорно-акцепторным;
г) диполь-дипольным.
83. Связи какого типа присутствуют в кристаллической решетке вещества, образованного атомами, имеющими следующие электронные конфигурации – 1s22s22p63s1 и 1s22s22p63s23p5?
а) ионные;
б) ковалентные полярные;
в) ковалентные неполярные;
г) водородные.
84. Минимальная степень окисления в соединениях атома, имеющего следующую электронную конфигурацию – 1s22s22p63s23p4?
а) +2;
б) -1;
в) -2;
г) -4.
85. Сколько ковалентных связей по обменному механизму может образовать атом, имеющий следующую электронную конфигурацию 1s22s2 2p3:
а) 3;
б) 6;
в) 4;
г) 5.
86. Сколько ковалентных связей по обменному механизму может образовать атом, имеющий следующую электронную конфигурацию 1s22s22p4?
а) 2;
б) 3;
в) 4;
г) 7.
87. Какую высшую степень окисления может проявлять атом, имеющий следующую электронную формулу 1s22s22p63s23p1?
а) +5;
б) +4;
в) +3;
г) +2.
88. Какую высшую степень окисления может проявлять атом, имеющий следующую электронную конфигурацию 1s22s22p63s23p4?
а) +2;
б) +4;
в) +6;
г) +7.
89. Какое минимальное число ковалентных связей по обменному механизму может образовать атом, имеющий следующую электронную конфигурацию 1s22s22p63s23p5?
а) 5;
б) 3;
в) 7;
г) 1.
90. Какую максимальную степень окисления может проявлять атом, имеющий следующую электронную конфигурацию 1s22s22p3?
а) +3;
б) +4;
в) +5;
г) +6.
91. Сколько ковалентных связей по обменному механизму может образовывать атом, имеющий следующую электронную конфигурацию 1s22s22p63s23p2?
а) 2;
б) 5;
в) 4;
г) 7.
92. Какую высшую степень окисления может проявлять атом, имеющий следующую электронную конфигурацию 1s22s22p4?
а) +4;
б) –4;
в) +2;
г) –2.
93. Какое максимальное число ковалентных связей по обменному механизму может образовать атом, имеющий следующую электронную конфигурацию 1s22s22p63s23p4?
а) 5;
б) 6;
в) 7;
г) 8.
94. Какую высшую степень окисления может проявлять атом, имеющий следующую электронную конфигурацию 1s22s22p63s23p5?
а) +5;
б) +3;
в) +1;
г) +7.
95. Сколько ковалентных связей по обменному механизму может образовать атом, имеющий следующую электронную конфигурацию …3s23p63d104s24p2?
а) 4;
б) 6;
в) 3;
г) 5.
96. Атомы каких элементов в соединениях с другими атомами всегда проявляют постоянную валентность?
а) О;
б) Н;
в)N;
г) S.
97. Атомы каких элементов проявляют в соединениях с другими элементами постоянную степень окисления?
а) N;
б) H;
в) Ca;
г) Na.
98. Валентность азота в ионе аммония NH4+ равна:
а) 3;
б) 4;
в) 5;
г) 6.
99. Степень окисления кислорода в ионе гидроксония равна:
а) –3;
б) –2;
в) +2;
г) +3.
100. Образование s-связи происходит за счет:
а) перекрывания двух s-электронных облаков;
б) бокового перекрывания двух р-электронных облаков;
в) перекрывания s- и р- электронных облаков;
г) осевого перекрывания двух р- электронных облаков.
101. p-связь образуется за счет:
а) перекрывания двух s-электронных облаков;
б) бокового перекрывания двух р-электронных облаков;
в) перекрывания одного s-электронного и одного р-электронного облаков;
г) бокового перекрывания двух р-электронных облаков, имеющих одинаковое значение ms (спинового квантового числа).
102. Длина связи – это:
а) удвоенная сумма радиусов взаимодействующих атомов;
б) расстояние между ядрами связанных атомов;
в) длина области перекрывания электронных облаков;
г) сумма радиусов взаимодействующих атомов.
103. Энергия связи – это:
а) энергия, выделяющаяся при образовании связи;
б) энергия, необходимая для разрыва связи;
в) энергия, необходимая для отрыва одного электрона с внешнего слоя атома;
г) энергия, необходимая для перевода молекулы в активное состояние.
104. Ионная связь характеризуется:
а) длиной;
б) энергией;
в) направленностью;
г) насыщаемостью.
105. Между атомами, имеющими следующую электронную конфигурацию 1s22s22p63s23p1, образуется химическая связь:
а) ковалентная полярная;
б) ковалентная неполярная;
в) водородная;
г) металлическая.
106. Между атомами, имеющими электронную конфигурацию 1s22s22p5, образуется химическая связь:
а) ковалентная полярная;
б) ковалентная неполярная;
в) водородная;
г) металлическая.
107. Между атомами, имеющими электронную конфигурацию 1s22s22p3 и 1s22s22p5, образуется химическая связь:
а) ковалентная полярная;
б) ковалентная неполярная;
в) водородная;
г) металлическая.
108. В какой молекуле, из перечисленных ниже, длина связи наименьшая?
а) F2;
б) Cl2;
в) Вr2;
г) H2.
109. Молекулы каких перечисленных ниже веществ не могут образовать водородные связи с молекулами воды?
а)метан;
б) аммиак;
в) азот;
г) метиламин.
110. В каком из перечисленных ниже соединений наибольшая длина связи?
а) HF;
б) HCl;
в) HBr;
г) HI.
111. В каких парах веществ между молекулами могут образоваться водородные связи?
а) Н2О и NH3;
б) HF и H2O;
в)СH4иN2;
г) N2 и H2O.
112. Какая связь между атомами в молекуле NH3?
а) ковалентная полярная;
б) водородная;
в) s-связь;
г) ковалентная неполярная.
113. Между молекулами воды образуются:
а) ковалентные полярные связи;
б) ковалентные неполярные связи;
в)s-связи;
г) водородные связи.
114. В какой из перечисленных ниже молекул длина связи наименьшая?
а) Br2;
б) Cl2;
в) I2;
г) HCl.
115. Самая большая длина связи между атомами в молекуле:
а) СН4;
б) SiH4;
в) GeH4;
г) SnH4.
116. Ядра всех атомов лежат на одной прямой в молекуле:
а) воды;
б) этина;
в) аммиака;
г) бериллий хлорида.
117. Молекула аммиака и ион аммония различаются между собой:
а) степенью окисления атома азота;
б) суммарным числом электронов;
в) валентностью атома азота;
г) суммарным числом протонов.
118. Сколько электронов участвует в образовании химических связей в молекуле SО2?
а) 2;
б) 4;
в) 6;
г) 8.
119. Укажите число σ-связей в молекуле высшего оксида элемента, атом которого в возбужденном состоянии имеет электронную конфигурацию внешнего слоя 2s12р3:
а) 0;
б) 4;
в) 3;
г) 2.
120. Укажите число π-связей в молекуле высшего оксида элемента, атом которого в возбужденном состоянии имеет электронную конфигурацию внешнего электронного слоя 3s13р33d2:
а) 0;
б) 1;
в) 2;
г) 3.
121. В каком ряду угол связи между атомами в молекулах последовательно возрастает?
а) Н2О, NН3, СН4, ВеСl2;
б) NН3, ССl4, ВF3, С2Н2;
в) ВСl3, СН4, ВеF2, С2Н4;
г) С2Н4, СН4, С2Н2, С6Н6.
122. В каком ряду молекулы всех веществ могут образовывать водородные связи с молекулами Н2О:
а)СН4,СF4,NН3,РН3?
б) NН2ОН, СН3ОН, НF, N2Н4;
в) Н2, О2, N2, F2;
г) СН2О, РСl5, F2O, СН4.
123. Полярной является молекула:
а) СО2;
б) Н2О;
в) ВF3;
г) NН3.
124. Неполярной является молекула:
а) N2;
б) Р4;
в) НCl;
г) СCl4
125. В молекулах каких веществ все атомы лежат в одной плоскости?
а) ВF3;
б) CF4;
в) NH3;
г) С2Н4.
126. Молекулы каких веществ могут образовывать ковалентные связи по донорно-акцепторному механизму, выступая при этом только в роли донора электронной пары?
а) Н2О;
б) NН3;
в) СО;
г) ВF3.
127. Молекулы каких веществ могут образовывать ковалентные связи по донорно-акцепторному механизму, выступая в роли акцептора электронной пары?
а) F2;
б) BCl3;
в) СО2;
г) СН3NН2.
128. В каком ряду молекулы всех веществ могут образовать водородные связи с молекулами Н2О?
а) NH3, CH3OH, CH3−C(O)−CH3, HCOOH;
б) CH3NH2, C6H5OH, C6H5NH2, НF;
в) COCl2, CBr4, NF3, NH2ОН;
г) Н2, СО2, СН4, C6Н5Cl.
129. Гибридизация – это:
а) перекрывание более двух электронных облаков при образовании химической связи;
б) самопроизвольное изменение формы и взаимного расположения в пространстве атомных орбиталей;
в) процесс образования между двумя атомами кратных связей;
г) процесс выравнивания в молекуле длин связей между атомами.
130. Гибридные электронные облака в отличие от электронных облаков, не подвергнувшихся гибридизации, способны:
а) образовывать более прочные ковалентные связи;
б) образовывать, наряду с σ−связями, и π−связи;
в) участвовать в образовании сопряженных связей;
г) участвовать в образовании неполярных ковалентных связей.
131. В образовании π−связей могут принимать участие:
а) электронные облака, подвергнувшиеся гибридизации;
б) s−электронные облака;
в) р–электронные облака;
г) d−электронные облака.
132. Выберите верные утверждения:
а) межмолекулярные взаимодействия наиболее сильные между полярными молекулами;
б) межмолекулярные взаимодействия между неполярными молекулами не могут иметь электростатическую природу;
в) гибридные электронные облака не способны образовать между собой π−связи;
г) энергия образования химической связи и энергия ее разрыва численно совпадают.
133. Ненаправленной является:
а) ковалентная полярная и ковалентная неполярная связи;
б) ионная связь;
в) металлическая связь;
г) водородная связь.
134. Длины связей в молекулах НF и НВr равны, соответственно, 0,092 и 0,141 нм. Укажите длины связей (нм) в молекулах НСl и НI, соответственно:
а) 0,082 и 0,134;
б) 0,128и0,160;
в) 0,151 и 0,172;
г) 0,092 и 0,145.
135. Энергия связи Э–Н в молекулах SbН3 и РН3 равна, соответственно. 256 и 323 кДж/моль. Укажите энергию связи Э–Н в молекулах NH3 и AsН3, соответственно:
а) 310и240;
б) 280 и 320;
в) 380 и 281;
г) 190 и 450.
136. Максимальный угол между гибридными орбиталями атомов углерода в молекулах:
а) С2Н6;
б) С6Н6;
в) С2Н4;
г) С2Н2.
Ответы
